Kolor osmowy. Jednym z najdroższych metali na świecie jest osm i jego koszt w przeliczeniu na gram
Przeczytaj także
Element porządkowy o liczbie atomów 76 cali układ chemiczny DI. Mendelejew ma na imię osm. W postaci stałej metal ma błyszczący srebrno-biały kolor z niebieskawymi odcieniami. Uważany za metal ciężki, gęstość osmu wynosi 22,6 g/cm3. Ale jednocześnie jest delikatny i można go wykorzystać do produkcji proszku. W tym stanie metal odkrył angielski chemik S. Tennant. Metal przejściowy, należący do grupy platynowców. W stanie małym jest podatny na utlenianie w temp temperatura pokojowa.
Właściwości osmu
Metal szlachetny jest najgęstszy (22,61 g/cm3) i ogniotrwały. Właściwości fizyczne osmu są następujące:
1. Topi się w temperaturze 3047°C, wrze w 5025°C, nie nadaje się do obróbki mechanicznie, nie można rozpuścić w kwasie i wodzie królewskiej.
2. Ma nieprzyjemny zapach przypominający mieszaninę czosnku i wybielacza, który jest dodawany w celu nadania stopowi platyny twardości i elastyczności.
3. Masa atomowa osm wynosi 190,23 g/mol.
4. Izotop 187 powstaje w wyniku rozpadu izotopu renu. Ze względu na swoją obojętność chemiczną stop osmu jest stosowany w agresywnym środowisku kwaśnym.
5. Metal łatwo się kruszy w postaci proszku fioletowy powoli rozpuszcza się w kwasach, reaguje ze związkami takimi jak siarka, selen, tellur i fosfor.
6. W stanie kruchym reaguje z rtęcią, tworząc amalgamat osmu.
7. Podczas interakcji z innymi substancjami wydziela nieprzyjemny zapach.
8. Zewnętrznie kryształy wyglądają pięknie. Pod wpływem wysokich temperatur topi się, tworząc twarde i kruche kryształy. Kolor metalu jest szaroniebieski ze srebrzystym połyskiem.
Jego właściwości zewnętrzne mogą być docenione przez jubilerów, jednak ze względu na toksyczność i interakcję chemiczną z innymi pierwiastkami nie jest stosowany do produkcji biżuterii.
Skorupa ziemska zawiera 0,5% tego metalu, głównie w centrum Ziemi – jądrze. Kawałek metalu, podobnie jak jajko, waży jeden kilogram. Jeśli wlejesz proszek z tej substancji do pojemnika o pojemności 0,5 litra, jego waga wyniesie 16 kg.
Właściwości chemiczne metal szlachetny następujące:
- w stanie stałym utlenia się w temperaturach powyżej 400 C, w proszku reaguje już w temperaturze pokojowej (OsO4);
- po podgrzaniu oddziałuje z siarką, chlorem, fluorem, siarką i innymi pierwiastkami chemicznymi;
- we wrzeniu kwas chlorowodorowy e nie rozpuszcza się, ale w drobno rozdrobnionej formie łączy się z cząsteczkami kwasu azotowego i ulega utlenieniu: Os + 8HNO3 = OsO4 + 4H2O + 8NO2;
- czarny dwutlenek osmu OsO2 uwalnia się podczas odwadniania w atmosferze azotu;
- Hydroksylosm (IV)Os(OH)4 (OsO2 · 2H2O) otrzymuje się w wyniku redukcji soli metali(VI).
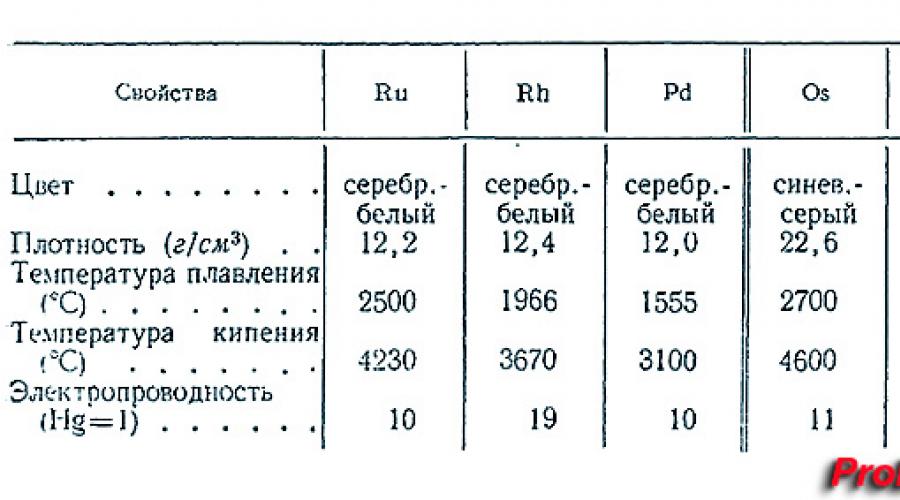
W przyrodzie występuje sześć izotopów, jeden ze 186 izotopów rozpada się na związki z grupy alfa. Osm istnieje najdłużej – 194 z okresem półtrwania wynoszącym dwa lata. Osm niewiele różni się od innych metali z grupy platynowców (ruten, pallad, osm, iryd, platyna), ale przewyższa inne metale ze względu na swoją gęstość i zdolność wrzenia w bardzo wysokich temperaturach.
Występuje w naturze w postaci natywnej w postaci stałego roztworu z irydem (minerały nevyanskite i sysertskite).
Aplikacja
Dodawanie osmu do różne stopy czyni je bardziej stabilnymi, trwałymi, niepodlegającymi mechanizacji i korozji.
- Przemysł elektrochemiczny: stosowany w związkach wolframu, niklu i kobaltu. Wszystkie produkty są odporne na zużycie.
- Wprowadzenie metalu z grupy platynowców do wyrobów metalowych zwiększa ich wytrzymałość. Do wytworzenia ostrych ostrzy, wyrobów medycznych i wyrobów technicznych potrzeba bardzo niewielkiej ilości substancji.
- Pióra wieczne ze stalówkami nie zużywają się przez długi czas.
- W kardiologii: metal znalazł swoje zastosowanie w implantach (rozrusznikach serca) i wymianie zastawek płucnych.
- W połączeniu z wolframem służy do produkcji żarników do lamp elektrycznych.
- Nie ma przyciągania magnetycznego, dlatego znalazł zastosowanie w produkcji części do zegarków.
- Do produkcji wykorzystuje się wykonane z niego katalizatory leki, syntetyzować amoniak. Wyższy tlenek tego metalu wykorzystywany jest do produkcji sztucznych leków oraz w laboratorium – służy do barwienia tkanek pod mikroskopem.
- Twardy metal wykorzystywany jest do produkcji podpór i osi do precyzyjnych przyrządów pomiarowych. Ze względu na swoją twardość metal jest używany do produkcji instrumentów.
- Osm 187 i inne izotopy są wykorzystywane w przemyśle ciężkim: rakietach, samolotach pasażerskich, wyposażenie wojskowe. Dzięki swojej odporności na zużycie pomaga wytrzymać ekstremalne warunki.
Historia odkrycia
Osm jest metalem szlachetnym. Ale to zaprzecza jego statusowi: przetłumaczone z greckiego „osme” oznacza zapach, czyli substancję chemicznie aktywną. A szlachetność implikuje obojętność tej substancji.
Osm został odkryty w 1803 r. Angielski chemik S. Tennant we współpracy z Williamem H. Wollastonem przeprowadził eksperymenty z rozpuszczaniem osmu w wodzie królewskiej, ale nic z tego nie wyszło. Podobne badania przeprowadzili francuscy chemicy Collet-Descoti, Antoine de Fourcroix i Vauquelin. Odkryli w tym pierwiastku nierozpuszczalny osad rudy platyny. Pierwiastkowi chemicznemu nadano nazwę pten, od greckiego słowa oznaczającego latanie. W tym eksperymencie udowodniono obecność dwóch substancje chemiczne- osm i iryd.
Gdzie występuje w przyrodzie i jak się go uzyskuje?
W naturze metal szlachetny nie występuje w bryłkach. Wydobywa się go ze skał: sysertskit, nevyanskit, osmiiride i sarsite. Wchodzi w skład rud miedzi, molibdenu i niklu. Według niektórych danych zawiera związki arsenu i siarki.
Udział materii na planecie wynosi 0,000005% całkowitej masy wszystkiego skały. W naturze osm łączy się z irydem, odsetek który waha się od 10 do 50. Zasoby tego metalu występują w Afryce, Tasmanii, Australii, Stanach Zjednoczonych, Kanadzie, Kolumbii i Rosji. Najbogatszym krajem pod względem zawartości osmu jest Republika Południowej Afryki (kompleks złoża Bushveld). Metal szlachetny występuje w stopach rodzimej platyny, ale częściej w stopach osmu i irydu.
Stan kruchy jest najbardziej akceptowalną formą istnienia. W tej formie lepiej wchodzi w reakcje chemiczne i ulega obróbka cieplna. Metal z grupy platynowców można otrzymać następującymi sposobami:
- wykorzystanie wiązki elektronów;
- ogrzewanie łukowe;
- zastosowanie beztyglowego topienia strefowego.
Otrzymane kryształy ostatni sposób bardzo drogi. Komuś udało się wyhodować kryształy z proszku, ale metoda jest trudna i czasochłonna.
Cena
Metal ten jest dość rzadki w przyrodzie, a wydobycie osmu jest przedsięwzięciem kosztownym, co determinuje jego cenę na rynku. W latach 60. – 70. XX w. metal szlachetny był kilkukrotnie droższy od złota. Sprzedawali go tanio, ale drogo go wyceniono, dlatego oferty na rynku były oszałamiające: gram metalu szacowano na 10 tysięcy, a za 200 tysięcy dolarów. Złoto nie jest tak cenione jak jego odpowiednik z grupy platynowców.
Dlaczego osm jest niebezpieczny?
Związek chemiczny osm uszkadza narządy ludzkie. Wdychanie oparów jest śmiertelne. W przypadku odurzenia zwierząt obserwowano niedokrwistość i upośledzenie funkcji płuc.
Czy wiesz, że tlenek tetraosmu OsO4 jest związkiem dość agresywnym i w przypadku zatrucia na skórze pojawiają się zielone lub czarne bąbelki. Nie jest to łatwe dla danej osoby, ponieważ leczenie zajmie dużo czasu.
Osoby pracujące w niebezpiecznych branżach powinny zachować ostrożność. W tym celu przedsiębiorstwa wydają kombinezony ochronne i maski oddechowe.
Osm to pierwiastek chemiczny o liczbie atomowej 76. W układzie okresowym pierwiastków chemicznych D.I. Mendelejewa jest on oznaczony symbolem Os (łac. Osm). W standardowych warunkach jest to srebrzysto-niebieskawy, kruchy metal przejściowy. Należy do grupy metali platynowych. Ma dużą gęstość, porównywalną pod tym parametrem jedynie z irydem (gęstości Os i Ir są prawie równe, biorąc pod uwagę błąd obliczeniowy).
Fabuła
Osm został odkryty w 1804 roku przez angielskiego chemika Smithsona Tennanta w osadzie pozostałym po rozpuszczeniu platyny w wodzie królewskiej. Podobne badania przeprowadzili francuscy chemicy Collet-Descoti, Antoine Francois de Fourcroy i Vauquelin, którzy również doszli do wniosku, że nierozpuszczalna pozostałość rudy platyny zawiera nieznany pierwiastek. Hipotetycznemu pierwiastkowi nadano nazwę pten (skrzydlaty), jednak eksperymenty Tennanta wykazały, że była to mieszanina dwóch pierwiastków – irydu i osmu.
Nazwa pochodzi od starożytnej Grecji. ὀσμή (zapach) na bazie ostro pachnącego lotnego tlenku OsO 4 (przypominającego ozon).
Paragon
Osm wyodrębnia się ze wzbogaconych surowców platyny poprzez kalcynację tego koncentratu w powietrzu w temperaturze 800-900°C. W tym przypadku pary bardzo lotnego czterotlenku osmu OsO 4 sublimują ilościowo, które następnie są absorbowane przez roztwór NaOH.
Przez odparowanie roztworu wyodrębnia się sól – perosmian sodu, którą następnie redukuje się wodorem w temperaturze 120°C do osmu:
Na2 + 3H2 = 2NaOH + Os + 4H2O.
W tym przypadku osm otrzymuje się w postaci gąbki.
Nieruchomości
Fizyczny
Osm to szaro-niebieskawy, twardy, ale kruchy metal o bardzo wysokim ciężarze właściwym, który zachowuje swój połysk nawet w wysokich temperaturach. Ze względu na swoją twardość, kruchość, niskie ciśnienie opary (najniższy ze wszystkich metali platynowych), a także bardzo wysoka temperatura topnienia, osm metaliczny jest trudny w obróbce. Osm jest uważany za najgęstszy ze wszystkich pierwiastków chemicznych, nieznacznie przewyższając iryd w tym parametrze. Najbardziej wiarygodne gęstości tych metali można obliczyć na podstawie parametrów ich sieci krystalicznych: 22,562 ± 0,009 g/cm3 dla irydu i 22,587 ± 0,009 g/cm3 dla osmu. Porównując różne izotopy tych metali, 192 Os jest najgęstszy. Nadzwyczajny duża gęstość osm można wytłumaczyć skurczem lantanowców.
Chemiczny
Po podgrzaniu proszek osmu reaguje z tlenem, halogenami, parami siarki, selenem, tellurem, fosforem, kwasami azotowymi i siarkowymi. Kompaktowy osm nie reaguje ani z kwasami, ani z zasadami, ale tworzy rozpuszczalne w wodzie osmaty ze stopionymi zasadami. Reaguje powoli z kwasem azotowym i wodą królewską, reaguje ze stopionymi zasadami w obecności środków utleniających (azotan lub chloran potasu) oraz ze stopionym nadtlenkiem sodu. W związkach wykazuje stopnie utlenienia od -2 do +8, z których najczęstsze to +2, +3, +4 i +8.
Osm jest jednym z niewielu metali tworzących związki wielopierścieniowe (lub klasterowe). Do modelowania i badań wykorzystuje się wielopierścieniowy karbonylek osmu Os 3 (CO) 12 reakcje chemiczne węglowodory na centrach metalicznych. Grupy karbonylowe w Os 3 (CO) 12 można zastąpić innymi ligandami, w tym zawierającymi jądra klastra innych metali przejściowych.
To nie złoto czy platyna są najdroższymi metalami ze stołu D.I. Mendelejewa, ale osm. Jest to rzadki i drogi metal o srebrno-białym kolorze z szarym odcieniem niebieskiego odcienia. Chemicy uważają ten metal za szlachetny, należący do grupy platynowców.
Składa się z kilku izotopów. Bardzo trudno je rozdzielić, co przekłada się na cenę. Najpopularniejszym izotopem jest osm-187.
Przyjmuje się, że przy 0,5% mas skorupa Ziemska składa się z osmu i znajduje się w jądrze. Zaskakująca jest proporcja wielkości do wagi. Kilogram związku ma wielkość porównywalną do średniej wielkości kurze jajo. Pojemnik o pojemności 0,5 litra wypełniony proszkiem osmu waży ponad 15 kg. Ale chęć rzucania hantlami z tak wygodnego materiału pod względem stosunku wielkości do masy natychmiast znika nie tylko ze względu na cenę proszku, dla niektórych nie stanowi to problemu, ale ze względu na jego wyjątkową rzadkość i niedostępność.
Nie będziesz w stanie znaleźć sztabek w lasach, górach ani zbiornikach wodnych. Jak dotąd nie odnaleziono ani jednej bryłki. Wydobywany jest ze złóż rud w składzie z rudami irydu, platyny, platyny i palladu, miedzi i niklu. Ale zawartość osmu wynosi 0,001%. Występuje także w meteorytach. To prawda, że izotopy oddzielają się od nich po ponad 9 miesiącach. Dlatego do produkcji przemysłowej z wykorzystaniem osmu wykorzystuje się surowce wtórne, które są niewiele tańsze.
Całkowita produkcja najcięższego metalu rocznie na całym świecie wynosi kilkadziesiąt kilogramów. Wzrasta jednak ekstrakcja platyny, w której występuje i jednocześnie ekstrahuje się osm. Liczby wynoszą już 200 kg rocznie. Powstaje więc zadanie nie tyle szukać osmu, ile znaleźć więcej tani sposób oddzielając ją od „sąsiadów”.
Kombinat Górniczo-Hutniczy Norylsk odniósł w tym zadaniu pewien sukces. Czysty metal otrzymywaliśmy z rud miedzi i niklu. Jego ilość na planecie wynosi 0,000005% całkowitej masy skał. Ale w Rosji tak jest. I w Kazachstanie. Główne rezerwy znajdują się na Tasmanii, Ameryce i Australii. Największe skupiska znajdują się w Republice Południowej Afryki. Ona dyktuje ceny.
Historia odkryć i właściwości przyrodnicze
W latach 1803-1804 w Anglii, podczas prowadzenia doświadczeń na platynie z wodą królewską (mieszaniną kwasu azotowego i kwasu solnego), w powstałym nieznanym osadzie, po rozpuszczeniu platyny, wytrącił się ostry, nieprzyjemny zapach, przypominający chlor. Dzięki temu zapachowi nowo odkryty metal zyskał swoją nazwę. Prawda, dalej grecki. Z greckiego „osm” tłumaczy się jako „zapach”.

Formalnie dzieje się tak dlatego, że zaliczany jest do grupy platynowców. Tu kończy się prawdziwa szlachetność. Właściwości tego metalu, zarówno chemiczne, jak i fizyczne, nie zostały jeszcze w pełni zbadane. Charakterystyka fizyczna mniej więcej wyjaśnione kilka lat temu.
Osm
| Właściwości chemiczne | Właściwości fizyczne |
|---|---|
| Nierozpuszczalny w zasadach i kwasach | Zewnętrznie kryształy są twarde i kruche, mają piękny srebrzysty połysk z odcieniami od szarości do błękitu. Wlewki – ciemny niebieski, proszek jest fioletowy. A wszystko z niesamowitym srebrnym połyskiem. |
| Nie reaguje na piekielną mieszaninę kwasu azotowego i solnego - jedynego metalu na planecie. | Temperatura stopów jest taka, że lepiej jest je stopić na powierzchni Słońca. |
| Obojętny. Możliwe jest stosowanie stopów i powłok osmu w środowiskach agresywnych. | Najwyższa toksyczność nie pozwala na wykorzystanie takiego piękna do wyrobu biżuterii. |
| Wyjątkowo toksyczny, nawet w małych dawkach. Szczególnie lotny tlenek osmu uwalniany z platyny. | Niezwykle kruchy. Obróbka poza kontrolą. |
| Wrze w temperaturze 5500°C, ale nie jest to dokładnie określone - nie ma obliczeń, które można by zweryfikować | Nietopliwość. Mięknie dopiero w temperaturach powyżej 3000 stopni C. |
| Nie posiada właściwości magnetycznych. | |
| Niesamowita twardość. Stop z dodatkiem osmu staje się bardziej odporny na zużycie, trwały, o zwiększonej odporności na korozję i naprężenia mechaniczne. | |
| Najwyższa gęstość wynosi 22,61 g/cm3. |
Cena
Wysoki koszt wynika z ograniczonej ilości. Ponieważ jest on rzadki w przyrodzie, a produkcja jest kosztowna, rynek odpowiednio reaguje. Jeśli porównamy to ze złotem, będzie to tysiące ton złota w porównaniu do kilkudziesięciu kilogramów produkcji. Stąd cena – zaczyna się od 15 tysięcy i sięga 200 tysięcy dolarów za gram. Na rynku światowym złoto jest 7,5 razy tańsze.
Takie liczby wskazują na niepopularność materiału do powszechnego użytku. Wytrzymałość odgrywa główną rolę w zastosowaniu tego metalu ciężkiego w stopach. Produkty stają się niezwykle odporne na zużycie dzięki dodaniu do kompozycji bardzo małych porcji metalu.
Aplikacja
Szeroko produkcja przemysłowa Osm jest rzadko używany ze względu na jego wysoki koszt. Ale tam, gdzie efekt może przewyższać koszty materialne, jest to oczywiście stosowane. Surowiec najczęściej występuje w postaci proszku. Sam metal jest delikatny i łatwo się kruszy. Zdobycie proszku nie jest trudne.
Więcej przypadków użycia:

Nie wszystkie związki osmu nadają się do użycia. Ale naukowcy nad tym pracują.
Niebezpieczeństwo i bezpieczeństwo
Podobnie jak innych metali ciężkich, osm nie ma go najwięcej korzystny wpływ na organizmy żywe, z pominięciem człowieka. Wszelkie związki zawierające osm są szkodliwe narządy wewnętrzne, spowodować utratę wzroku. Zatrucie oparami pierwiastka może również prowadzić do śmierci. Obserwując zwierzęta, zaobserwowano gwałtowny rozwój niedokrwistości, a płuca przestały funkcjonować. Uważa się, że jest to szybko rozwijający się obrzęk.
Co to jest tetratlenek osmu OsO4? I to jest właśnie substancja, dzięki której element nosi swoją nazwę. Niezwykle agresywny. Obok jego zapachu nie można przejść obojętnie. Nie ma w przyrodzie bardziej okropnego i obrzydliwego zapachu. W przypadku zatrucia wpływa to również na skórę. Skóra właściwa zmienia kolor na zielony, staje się czarny, a nawet może stać się martwa. Mogą pojawić się pęcherze i owrzodzenia. Wszystko goi się bardzo długo.
Niebezpieczeństwo zatrucia dotyczy przede wszystkim pracowników pomieszczenia produkcyjne przy najmniejszym stężeniu par w powietrzu. Nic akceptowalne standardy Naukowcy już się nie jąkają. Dlatego zapewnione specjalna odzież, maski oddechowe – częstym zjawiskiem w produkcji przy użyciu tlenku osmu. Wszystko jest szczelnie zamknięte, pojemniki są zaplombowane i przechowywane zgodnie ze sprawdzonymi już zasadami.
Jeśli z jakiegoś nie do pomyślenia powodu związek osmu dostanie się do oczu, należy je płukać przez długi czas, około 20 minut. Czysty bieżącą wodę. I natychmiast udaj się do lekarza. Kiedy wchodzisz do ciała Drogi oddechowe Opary osmu neutralizuje się wodorowęglanem sodu. Dostępny jest w opakowaniach aerozolowych. W środku dużo mleka. I opłucz żołądek.
Niewątpliwe zalety najcięższego metalu
Według angielskich naukowców ten metal ciężki blokuje rozwój komórek nowotworowych. Metody leczenia nowotworów przy użyciu osmu, choć bardzo powoli, już są opracowywane.
W medycynie, przy stymulacji serca, stosuje się go w implantach, do produkcji których wymagane są metale szlachetne, aby zapobiec rozwojowi alergii. Skład implantu zastępującego elementy serca zawiera 10% osmu i 90% platyny. Oczywiście takie urządzenia są odpowiednio wycenione. Tę samą proporcję wykorzystuje się do wykonania zastawek płucnych.

Zastosowanie związków osmu dla potrzeb medycznych jest zauważalne w produkcji szczególnie trwałych, trwałych narzędzi, takich jak skalpele i wszelkiego rodzaju siekacze metalowo-ceramiczne. A potrzeba do tego bardzo mało surowca, a efekt jest niesamowity.
Mikroskopijne dodatki osmu do stali nierdzewnej umożliwiają tworzenie wyjątkowo ostrych ostrzy.
Produkty, których użycie wiąże się z używaniem ciężkiego metalu okazują się niezrównaną odpornością na zużycie.
Zainteresowanie komercyjne
Różne niesamowite właściwości metalicznego osmu budzą niewątpliwe zainteresowanie i prawdziwe zaskoczenie. Ale te same właściwości całkowicie zabijają zainteresowanie komercyjne. I mimo wszystko cena na rynku nie spada.
Hantle i sztangi używane przez kulturystów do pompowania mięśni są wykonane ze stali. Pociski wykonane z ołowiu – lub jeszcze lepiej – straciłyby znaczną objętość. Ale jeszcze lepiej jest użyć osmu do produkcji odważników: Kilogram osmu to mała kulka, która z łatwością zmieści się w zaciśniętej pięści. Półlitrowa butelka sproszkowanego osmu (w takiej postaci metal szlachetny opuszcza ściany zakładu wzbogacania) waży zauważalnie więcej niż wiadro wody.
Ale nie można znaleźć nikogo na tyle odważnego, by rzucić ciężarki z osmu: jest on zbyt ogniotrwały. A koszt metalu jest taki, że klub sportowy musiałby pracować trzysta lat, żeby kupić jeden hantle osmowy...
Za mało osmu!
I to jest zrozumiałe. Kształtować ciężkie elementy natura musi „tworzyć” specjalne warunki, co nie zdarza się zbyt często. Jednakże osm stanowi pół procent masy skorupy ziemskiej. Istnieją podstawy, aby wierzyć, że większość metalu szlachetnego zgromadzonego w ciele naszej planety koncentruje się w jądrze.W naturze osm występuje głównie w postaci związku z irydem, który wchodzi w skład rudy platyny rodzimej lub rudy platynowo-palladowej. Minerały uważane za surowce do wydobycia osmu zawierają średnio jedną tysięczną procenta ciężkiej „względnej” platyny. Przez cały okres badań nie wydobyto ani jednej bryłki osmu, nawet najmniejszej.
Niewielka ilość i trudność uzyskania osmu decyduje o wysokości jego ceny. Pół wieku temu osm szacowano na siedem do ośmiu razy droższe od złota. Spekulacja ostatnie lata doprowadziło do pojawienia się całkowicie szalonych ofert: gram osmu sprzedawano zarówno za 10 tysięcy, jak i 200 tysięcy dolarów. Został sprzedany, ale nie został sprzedany: osm nie jest aktywnie wykorzystywany, chociaż jest używany w niektórych miejscach.
Odkrycie osmu
Osm należy do grupy platynowców i jest formalnie uważany za metal szlachetny. Nazwa pierwiastek chemiczny zaprzecza jednak statusowi: „osme” po grecku oznacza „zapach”; obecność zapachu wskazuje na znaczną aktywność chemiczną - natomiast „szlachetność” substancji oznacza obojętność.Wollaston, który eksperymentował z rudami platyny, był bliski odkrycia osmu. Zachęceni jego sukcesami Francuzi Antoine de Fourcroy i Louis-Nicolas Vauquelin rozpoczęli własne badania i słusznie założyli istnienie nowego pierwiastka, który podczas eksperymentów odparował w postaci czarnego dymu.
Fourcroix i Vauquelin nadali substancji nazwę „ptene”, co oznacza „lotny”, i uspokoili się, czekając na rozpoznanie. Jednak angielski chemik Smithson Tennant podzielił „pten” na dwa pokrewne metale, z których jeden nazwano irydem ze względu na różnorodność kolorów jego związków, a drugi ze względu na drażniący smród nazwano osmem.
Takie rzeczy się zdarzają ważne wydarzenia w roku 1803, hojny w odkryciach.
Właściwości osmu
Badania właściwości fizykochemiczne osmia w całości nie została jeszcze uzyskana. Przez długi czas naukowcy spierali się, który metal jest gęstszy - iryd czy osm. Dokładne pomiary próbek laboratoryjnych w w tym przypadku podawaj tylko przybliżone wyniki - z powodu duża ilość izotopy o różnej gęstości.Do niedawna uważano, że temperatury topnienia i wrzenia są warunkowo równe 3000° i 5000°C: nie było możliwości sprawdzenia obliczeń w pełnej skali. Dopiero kilka lat temu udało się to wyjaśnić parametry fizyczne metal Podobno okazuje się, że lepiej gotować stopy osmu na powierzchni Słońca...
Ciekawy wygląd Osmia. Zestalający się ze stopu osm tworzy twarde i kruche kryształy, których srebrzysty połysk jest cieniowany przez szarawo-niebieski (a nawet niebieski) odcień. Zewnętrzne zalety osmu mogą przyciągnąć jubilerów, ale wysoka aktywność chemiczna metalu i toksyczność jego związków wykluczają możliwość stosowania tej platyny w biżuterii.
Zastosowania osmu
Osm ma bardzo ograniczone zastosowanie różne obszary ludzka aktywność. Stapianie stopów jest jednym z głównych zadań, którego rozwiązanie czasami przypisuje się osmowi. W połączeniu z wolframem, niklem i kobaltem osm staje się „pracownikiem” przemysłu elektrochemicznego. Styki, końcówki i rdzenie wykonane ze stopów osmu słyną z minimalnego zużycia. Włókna żarówek wolframowo-osmowych mają dłuższą żywotność i są bardziej wydajne.Wprowadzenie twardej i ciężkiej platyny do materiału radykalnie zwiększa odporność na zużycie par trących. Aby nóż metalowo-ceramiczny miał szczególną wytrzymałość, potrzeba sporo osmu. Mikroskopijne dodatki osmu do gatunków stali pozwalają na tworzenie najostrzejszych ostrzy noży technicznych, medycznych i przemysłowych.
Katalizatory osmowe stosuje się do uwodornienia związków organicznych, do produkcji leków i do syntezy amoniaku. To prawda, że wysoki koszt metalu zmusza przemysłowców do poszukiwania niedrogich zamienników, a dziś osm staje się coraz mniej powszechny w przemyśle chemicznym.
Osie, podpory i tuleje podporowe wykonane są z litego i niemagnetycznego osmu. urządzenia pomiarowe wysoka precyzja. I chociaż podpory rubinowe są twardsze i tańsze niż osmowe, trwałość metalu jest czasami preferowana w przypadku produkcji instrumentów.
Osm jest niebezpieczny i wymaga ostrożności
Sam osm nie jest bardziej niebezpieczny niż jakikolwiek inny metal ciężki. Jednak tetratlenek osmu OsO4 - właśnie substancja, dzięki której pierwiastek otrzymał swoją niezbyt godną pozazdroszczenia nazwę - jest niezwykle agresywny. Działa drażniąco na drogi oddechowe i błony śluzowe człowieka, objawia się parowaniem z gnijącej rzodkiewki zmieszanej z rozgniecionym czosnkiem i pokrytej wybielaczem.Uniknięcie utleniania osmu jest prawie niemożliwe, jeśli metal wejdzie w kontakt z tlenem atmosferycznym. Dlatego nie należy stosować osmu w