Toplota sagorevanja gasa. Gasno gorivo
Plinsko gorivo dijeli se na prirodno i vještačko i mješavina je zapaljivih i nezapaljivih plinova koja sadrži određenu količinu vodene pare, a ponekad i prašinu i katran. Količina plinsko gorivo izraženo u kubnim metrima u normalnim uslovima (760 mm Hg i 0°C), a sastav je izražen u procentima zapremine. Pod sastavom goriva podrazumijeva se sastav njegovog suhog plinovitog dijela.
Gorivo prirodnog gasa
Najzastupljenije plinsko gorivo je prirodni plin, koji ima visoku kalorijsku vrijednost. Osnova prirodnog gasa je metan, čiji je sadržaj 76,7-98%. Ostala gasovita ugljovodonična jedinjenja čine prirodni gas od 0,1 do 4,5%.
Tečni gas naftni proizvod - sastoji se uglavnom od mješavine propana i butana.
Prirodni gas (CNG, NG): metan CH4 više od 90%, etan C2 H5 manje od 4%, propan C3 H8 manje od 1%
Tečni gas (LPG): propan C3 H8 više od 65%, butan C4 H10 manje od 35%
Sastav zapaljivih gasova uključuje: vodonik H2, metan CH4, druga ugljovodonična jedinjenja CmHn, sumporovodik H2S i nezapaljive gasove, ugljen dioksid CO2, kiseonik O2, azot N2 i malu količinu vodene pare H2O. m I P na C i H karakteriziraju spojeve različitih ugljikovodika, na primjer za metan CH 4 t = 1 i n= 4, za etan C 2 N b t = 2 I n= b, itd.
Sastav suhog plinovitog goriva (volumenski postotak):
CO + H 2 + 2 C m H n + H 2 S + CO 2 + O 2 + N 2 = 100%.
Negorivi dio suhog plinskog goriva - balast - sastoji se od dušika N i ugljičnog dioksida CO 2.
Sastav vlažnog plinovitog goriva izražava se na sljedeći način:
CO + H 2 + Σ C m H n + H 2 S + CO 2 + O 2 + N 2 + H 2 O = 100%.
Toplota sagorevanja, kJ/m (kcal/m3), 1 m3 čistog suvog gasa u normalnim uslovima određuje se na sledeći način:
Q n s = 0,01,
gdje je Qso, Q n 2, Q c m n n Q n 2 s. - toplota sagorevanja individualni gasovi uključeno u smešu, kJ/m 3 (kcal/m 3); CO, H 2, Cm H n, H 2 S - komponente koje čine gasnu mešavinu, % po zapremini.
Kalorična vrijednost 1 m3 suhog prirodnog plina u normalnim uvjetima za većinu domaćih nalazišta iznosi 33,29 - 35,87 MJ/m3 (7946 - 8560 kcal/m3). Karakteristike gasovitog goriva date su u tabeli 1.
Primjer. Odrediti donju kalorijsku vrijednost prirodnog plina (u normalnim uvjetima) sljedećeg sastava:
H 2 S = 1%; CH 4 = 76,7%; C 2 H 6 = 4,5%; C 3 H 8 = 1,7%; C 4 H 10 = 0,8%; C 5 H 12 = 0,6%.
Zamjenom karakteristika gasova iz tabele 1 u formulu (26) dobijamo:
Q ns = 0,01 = 33981 kJ/m 3 ili
Q ns = 0,01 (5585,1 + 8555 76,7 + 15 226 4,5 + 21 795 1,7 + 28 338 0,8 + 34 890 0,6) = 8109 kcal/m3.
Tabela 1. Karakteristike gasovitog goriva
|
Gas |
Oznaka |
Toplota sagorevanja Q n s |
|
|
KJ/m3 |
Kcal/m3 |
||
| Vodonik | N, | 10820 | 2579 |
| Ugljen monoksid | CO | 12640 | 3018 |
| Hidrogen sulfid | H 2 S | 23450 | 5585 |
| Metan | CH 4 | 35850 | 8555 |
| Ethane | C 2 H 6 | 63 850 | 15226 |
| Propan | C 3 H 8 | 91300 | 21795 |
| Butan | C 4 H 10 | 118700 | 22338 |
| Pentane | C 5 H 12 | 146200 | 34890 |
| Etilen | C 2 H 4 | 59200 | 14107 |
| propilen | C 3 H 6 | 85980 | 20541 |
| Butilen | C 4 H 8 | 113 400 | 27111 |
| Benzen | C 6 H 6 | 140400 | 33528 |
Kotlovi tipa DE troše od 71 do 75 m3 prirodnog plina za proizvodnju jedne tone pare. Cena gasa u Rusiji od septembra 2008. iznosi 2,44 rubalja po kubnom metru. Stoga će tona pare koštati 71 × 2,44 = 173 rubalja 24 kopejke. Stvarna cijena tone pare u tvornicama je za DE kotlove ne manje od 189 rubalja po toni pare.
Kotlovi tipa DKVR troše od 103 do 118 m3 prirodnog gasa za proizvodnju jedne tone pare. Minimum procijenjeni trošak tona pare za ove kotlove je 103 × 2,44 = 251 rublje 32 kopejke. Stvarna cijena pare u tvornicama nije manja od 290 rubalja po toni.
Kako izračunati maksimalnu potrošnju prirodnog plina za parni kotao DE-25? Ovo tehničke specifikacije kotao 1840 kocki na sat. Ali možete i izračunati. 25 tona (25 hiljada kg) treba pomnožiti sa razlikom između entalpija pare i vode (666,9-105) i sve to podijeliti sa efikasnošću kotla od 92,8% i toplinom sagorijevanja plina. 8300. i to je to
Vještačko plinsko gorivo
Umjetni zapaljivi plinovi su gorivo od lokalnog značaja jer imaju znatno nižu kalorijsku vrijednost. Njihovi glavni zapaljivi elementi su ugljen monoksid CO i vodonik H2. Ovi plinovi se koriste u proizvodnom području gdje se dobivaju kao gorivo za tehnološke i elektrane.
Svi prirodni i umjetni zapaljivi plinovi su eksplozivni i mogu se zapaliti u otvorenom plamenu ili iskri. Postoje niži i gornja granica eksplozivnost gasa, tj. njegova najveća i najniža procentualna koncentracija u zraku. Donja granica eksplozivnosti prirodni gasovi kreće se od 3% do 6%, a vrh se kreće od 12% do 16%. Svi zapaljivi gasovi mogu izazvati trovanje ljudskog organizma. Glavne toksične supstance zapaljivih gasova su: ugljen monoksid CO, sumporovodik H2S, amonijak NH3.
Prirodni zapaljivi plinovi i umjetni plinovi su bezbojni (nevidljivi) i bez mirisa, što ih čini opasnima ako prodru u unutrašnji prostor kotlarnica kroz curenja u armaturi gasovoda. Da biste izbjegli trovanje, zapaljive plinove treba tretirati odorantom - tvari neugodnog mirisa.
Proizvodnja ugljen monoksida CO u industriji gasifikacijom čvrstog goriva
Za industrijske potrebe, ugljen monoksid se dobija gasifikacijom čvrstog goriva, odnosno pretvaranjem u gasovito gorivo. Na ovaj način možete dobiti ugljični monoksid iz bilo kojeg čvrstog goriva - fosilnog uglja, treseta, drva za ogrjev itd.
Prikazan je proces gasifikacije čvrstog goriva laboratorijsko iskustvo(Sl. 1). Punjenje vatrostalne cijevi komadima ugalj, zagrijmo ga jako i pustimo kiseonik da kroz njega struji iz gasometra. Propustimo gasove koji izlaze iz cevi kroz mašinu za pranje sa krečnom vodom i onda je zapalimo. Krečna voda postaje mutna i gas gori plavkastim plamenom. Ovo ukazuje na prisustvo CO2 dioksida i ugljen monoksida CO u produktima reakcije.
Nastanak ovih tvari može se objasniti činjenicom da kada kisik dođe u kontakt s vrućim ugljem, potonji se prvo oksidira u ugljični dioksid: C + O 2 = CO 2
Zatim, prolazeći kroz vrući ugalj, ugljični dioksid se djelomično reducira u ugljični monoksid: CO 2 + C = 2CO
Rice. 1. Proizvodnja ugljičnog monoksida (laboratorijski eksperiment).
U industrijskim uslovima, gasifikacija čvrstog goriva se vrši u pećima koje se nazivaju gasni generatori.
Dobivena mješavina plinova naziva se generatorski plin.
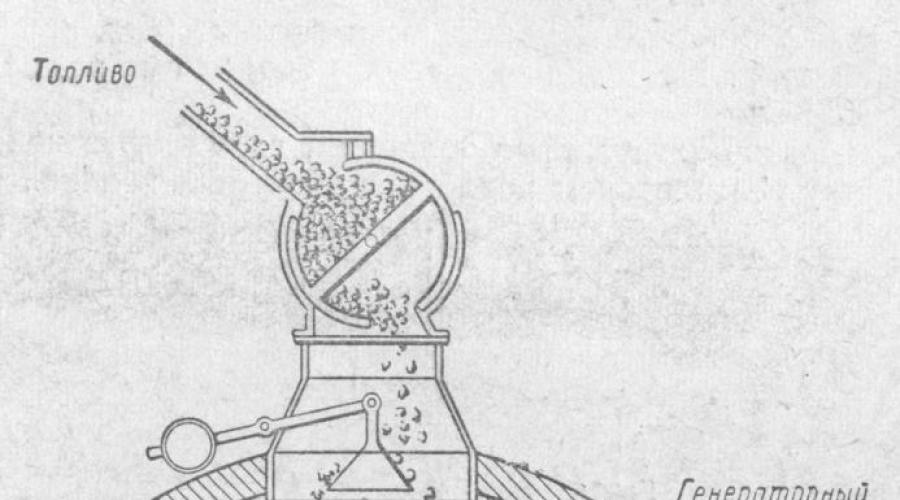
Uređaj generatora plina prikazan je na slici. To je čelični cilindar visine oko 5 m i prečnika od približno 3,5 m, iznutra obložen vatrostalnim ciglama. Plinski generator se puni gorivom odozgo; Odozdo se zrak ili vodena para dovodi ventilatorom kroz rešetku.
Kiseonik u vazduhu reaguje sa ugljenikom u gorivu i formira ugljen-dioksid, koji se, uzdižući se kroz sloj vrućeg goriva, redukuje ugljenikom u ugljen monoksid.
Ako se u generator upuhuje samo zrak, rezultat je plin koji sadrži ugljični monoksid i dušik iz zraka (kao i određenu količinu CO 2 i drugih nečistoća). Ovaj generatorski gas se naziva vazdušni gas.
Ako se vodena para upuhuje u generator s vrućim ugljem, reakcija rezultira stvaranjem ugljičnog monoksida i vodika: C + H 2 O = CO + H 2
Ova mešavina gasova se naziva vodeni gas. Vodeni plin ima veću kalorijsku vrijednost od plina zraka, budući da njegov sastav, uz ugljični monoksid, uključuje i drugi zapaljivi plin - vodonik. Vodeni gas (sintetski gas), jedan od proizvoda gasifikacije goriva. Vodeni gas se sastoji uglavnom od CO (40%) i H2 (50%). Vodeni gas je gorivo (toplota sagorevanja 10.500 kJ/m3, odnosno 2730 kcal/mg) i ujedno je sirovina za sintezu metil alkohola. Vodeni plin, međutim, ne može se proizvoditi dugo vremena, jer je reakcija njegovog stvaranja endotermna (sa apsorpcijom topline), pa se gorivo u generatoru hladi. Da bi se ugalj održao u vrućem stanju, ubrizgavanje vodene pare u generator se izmjenjuje s ubrizgavanjem zraka, za koji je poznato da kisik reagira s gorivom i oslobađa toplinu.
U posljednje vrijeme, parno-kiseonički mlaz se široko koristi za gasifikaciju goriva. Istodobno upuhivanje vodene pare i kisika kroz sloj goriva omogućava kontinuirano odvijanje procesa, značajno povećavajući produktivnost generatora i proizvodnju plina s visokim sadržajem vodonika i ugljičnog monoksida.
Moderni plinski generatori su moćni uređaji kontinuirano djelovanje.
Tako da prilikom dovoda goriva u generator plina, zapaljivo i otrovnih gasova nije prodro u atmosferu, utovarni bubanj je dvostruk. Dok gorivo ulazi u jedan odjeljak bubnja, gorivo se ulijeva u generator iz drugog odjeljka; kada se bubanj rotira, ovi procesi se ponavljaju, ali generator ostaje izolovan od atmosfere cijelo vrijeme. Ravnomjerna raspodjela goriva u generatoru vrši se pomoću konusa, koji se može ugraditi na različite visine. Kada se spusti, ugalj pada bliže centru generatora; kada se konus podigne, ugalj se baca bliže zidovima generatora.
Uklanjanje pepela iz generatora gasa je mehanizovano. Rešetka u obliku konusa se polako okreće pomoću elektromotora. U tom slučaju, pepeo se pomiče prema zidovima generatora i pomoću posebnih uređaja se ubacuje u kutiju za pepeo, odakle se povremeno uklanja.
Prve plinske lampe zapaljene su u Sankt Peterburgu na Aptekarskom ostrvu 1819. godine. Korišteni plin je dobiven gasifikacijom uglja. Zvao se iluminirajući gas.
Veliki ruski naučnik D.I. Mendeljejev (1834-1907) prvi je izrazio ideju da se gasifikacija uglja može izvršiti direktno pod zemljom, bez podizanja. Carska vlada nije cijenila ovaj prijedlog Mendeljejeva.
Ideju podzemne gasifikacije toplo je podržao V. I. Lenjin. On je to nazvao "jednom od velikih pobjeda tehnologije". Podzemnu gasifikaciju je po prvi put izvršila sovjetska država. Već prije Velikog domovinskog rata, podzemni generatori su radili u ugljenim bazenima Donjecka i Moskovske oblasti u Sovjetskom Savezu.
Ideja o jednoj od metoda podzemne gasifikacije data je na slici 3. U ugljeni sloj su položene dvije bušotine koje su ispod povezane kanalom. Ugalj se pali u takvom kanalu u blizini jednog od bunara i tamo se isporučuje eksplozija. Proizvodi izgaranja, krećući se duž kanala, stupaju u interakciju s vrućim ugljem, što rezultira stvaranjem zapaljivog plina kao u konvencionalnom generatoru. Plin izlazi na površinu kroz drugu bušotinu.
Proizvodni plin se široko koristi za grijanje industrijske peći- metalurški, koks i kao gorivo u automobilima (Sl. 4).
Rice. 3. Šema podzemne gasifikacije uglja.
Niz spojeva se sintetizira iz vodonika i ugljičnog monoksida u vodenom plinu organski proizvodi, na primjer tečno gorivo. Sintetičko tečno gorivo je gorivo (uglavnom benzin) dobijeno sintezom iz ugljen monoksida i vodonika na 150-170 stepeni Celzijusa i pri pritisku od 0,7 - 20 MN/m2 (200 kgf/cm2), u prisustvu katalizatora (nikl, gvožđe, kobalt). Prva proizvodnja sintetičkog tečnog goriva organizovana je u Nemačkoj tokom 2. svetskog rata zbog nestašice nafte. Sintetičko tečno gorivo nije postalo široko rasprostranjeno zbog svog visoka cijena. Vodeni plin se koristi za proizvodnju vodonika. Da bi se to postiglo, vodeni plin pomiješan s vodenom parom zagrijava se u prisustvu katalizatora i kao rezultat se dobiva vodik pored onog koji je već prisutan u vodenom plinu: CO + H 2 O = CO 2 + H 2
FIZIČKA I HEMIJSKA SVOJSTVA PRIRODNIH GASOVA
Prirodni gasovi nemaju boju, miris i ukus.
Glavni pokazatelji prirodnih gasova su: sastav, kalorijska vrednost, gustina, temperatura sagorevanja i paljenja, granice eksplozivnosti i pritisak eksplozije.
Prirodni gasovi sa čistih gasnih polja uglavnom se sastoje od metana (82-98%) i drugih ugljovodonika.
Zapaljivi gas sadrži zapaljive i nezapaljive materije. Zapaljivi gasovi uključuju: ugljovodonike, vodonik, vodonik sulfid. Nezapaljivi plinovi uključuju: ugljični dioksid, kisik, dušik i vodenu paru. Njihov sastav je nizak i iznosi 0,1-0,3% C0 2 i 1-14% N 2. Nakon ekstrakcije iz gasa se uklanja otrovni gas sumporovodik, čiji sadržaj ne bi trebalo da prelazi 0,02 g/m3.
Toplota sagorevanja je količina toplote koja se oslobađa kada potpuno sagorevanje 1 m3 plina. Toplota sagorevanja se meri u kcal/m3, kJ/m3 gasa. Kalorična vrijednost suhog prirodnog plina je 8000-8500 kcal/m3.
Vrijednost izračunata omjerom mase tvari i njenog volumena naziva se gustina tvari. Gustina se mjeri u kg/m3. Gustina prirodnog gasa u potpunosti zavisi od njegovog sastava i kreće se u rasponu c = 0,73-0,85 kg/m3.
Najvažnija karakteristika bilo kojeg zapaljivog plina je toplinska snaga, tj. Maksimalna temperatura postiže se potpunim sagorevanjem gasa, ako potrebna količina vazduha za sagorevanje tačno odgovara hemijskim formulama sagorevanja, a početna temperatura gasa i vazduha je nula.
Toplotni učinak prirodnog gasa je oko 2000 -2100 °C, metana - 2043 °C. Stvarna temperatura sagorevanja u pećima je znatno niža od toplotne snage i zavisi od uslova sagorevanja.
Temperatura paljenja je temperatura mješavine zraka i goriva pri kojoj se smjesa zapali bez izvora paljenja. Za prirodni plin je u rasponu od 645-700 °C.
Svi zapaljivi gasovi su eksplozivni i mogu se zapaliti ako su izloženi otvorenom plamenu ili varnici. Razlikovati donji i gornji granica koncentraciješirenje plamena , tj. donja i gornja koncentracija pri kojoj je moguća eksplozija smjese. Donja granica eksplozivnosti gasova je 3÷6%, gornja 12÷16%.
Granice eksplozivnosti.
Mješavina plina i zraka koja sadrži sljedeću količinu plina:
do 5% - ne svijetli;
od 5 do 15% - eksplodira;
više od 15% - gori kada se dovodi zrak.
Pritisak tokom eksplozije prirodnog gasa je 0,8-1,0 MPa.
Svi zapaljivi gasovi mogu izazvati trovanje ljudskog organizma. Glavne toksične supstance su: ugljen monoksid (CO), sumporovodik (H 2 S), amonijak (NH 3).
Prirodni gas nema miris. Da bi se utvrdilo curenje, gas se odorizira (tj. daje se specifičan miris). Odorizacija se vrši upotrebom etil merkaptana. Odorizacija se vrši na gasnim distributivnim stanicama (GDS). Kada 1% prirodnog gasa uđe u vazduh, on počinje da smrdi. Praksa pokazuje da bi prosječna količina etil merkaptana za odorizaciju prirodnog plina koji ulazi u gradsku mrežu trebala biti 16 g na 1.000 m3 gasa.
U poređenju sa čvrstim i tečno gorivo Prirodni plin pobjeđuje na mnogo načina:
Relativna jeftinost, što je više objašnjeno lakši način rudarstvo i transport;
Nema pepela ili ispuštanja čvrstih čestica u atmosferu;
Visoka kalorijska vrijednost;
Nije potrebna priprema goriva za sagorevanje;
Uslužnim radnicima je olakšan rad i poboljšani sanitarno-higijenski uslovi njihovog rada;
Uslovi za automatizaciju radnih procesa su pojednostavljeni.
Zbog mogućih curenja kroz nepropusnost na gasovodnim priključcima i spojevima, upotreba prirodnog plina zahtijeva posebnu pažnju i oprez. Prodor više od 20% gasa u prostoriju može dovesti do gušenja, a ako je prisutan u zatvorenoj zapremini, od 5 do 15% može izazvati eksploziju mešavine gasa i vazduha. Nepotpuno sagorijevanje proizvodi otrov ugljen monoksid CO, koji i u malim koncentracijama dovodi do trovanja servisera.
Prema poreklu prirodni gasovi se dele u dve grupe: suvi i masni.
Suha gasovi su gasovi mineralnog porekla i nalaze se u područjima povezanim sa sadašnjom ili prošlom vulkanskom aktivnošću. Suhi plinovi se sastoje gotovo isključivo od metana sa neznatnim sadržajem balastnih komponenti (dušik, ugljen-dioksid) i imaju kalorijsku vrijednost Qn=7000÷9000 kcal/nm3.
Debeo plinovi prate naftna polja i obično se akumuliraju u gornjim slojevima. Po svom poreklu vlažni gasovi su bliski nafti i sadrže mnogo ugljovodonika koji se lako kondenzuju. Kalorična vrijednost tečni gasovi Qn=8000-15000 kcal/nm3
Prednosti plinovitog goriva uključuju lakoću transporta i sagorijevanja, odsustvo pepela i vlage i značajnu jednostavnost kotlovske opreme.
Zajedno sa prirodni gasovi koriste se i veštački zapaljivi gasovi dobijeni tokom obrade čvrsta goriva, ili kao rezultat rada industrijske instalacije kao otpadni gasovi. Veštački gasovi se sastoje od zapaljivih gasova nepotpuno sagorevanje goriva, balastnih gasova i vodene pare i dele se na bogate i siromašne, sa prosečnom toplotnom vrednošću od 4500 kcal/m3 i 1300 kcal/m3, respektivno. Sastav gasova: vodonik, metan, druga ugljovodonična jedinjenja CmHn, sumporovodik H 2 S, nezapaljivi gasovi, ugljen-dioksid, kiseonik, azot i mala količina vodene pare. Balast – dušik i ugljični dioksid.
Dakle, sastav suhog plinovitog goriva može se predstaviti kao sljedeća mješavina elemenata:
CO + H 2 + ∑CmHn + H 2 S + CO 2 + O 2 + N 2 =100%.
Sastav vlažnog plinovitog goriva izražava se na sljedeći način:
CO + H 2 + ∑CmHn + H 2 S + CO 2 + O 2 + N 2 + H 2 O = 100%.
Toplota sagorevanja suho gasovito gorivo kJ/m3 (kcal/m3) po 1 m3 gasa u normalnim uslovima određuje se na sledeći način:
Qn= 0,01,
Gdje je Qi toplina sagorijevanja odgovarajućeg plina.
Kalorična vrijednost plinovitog goriva data je u tabeli 3.
Eksplozivni gas nastala tokom topljenja livenog gvožđa u visokim pećima. Njegov prinos i hemijski sastav zavise od svojstava punjenja i goriva, načina rada peći, načina intenziviranja procesa i drugih faktora. Učinak gasa se kreće od 1500-2500 m 3 po toni livenog gvožđa. Udio negorivih komponenti (N 2 i CO 2) u visokopećnom plinu iznosi oko 70%, što određuje njegove niske termičke karakteristike (niža kalorijska vrijednost plina je 3-5 MJ/m 3).
Prilikom sagorevanja visokopećnog gasa maksimalna temperatura produkata sagorevanja (bez uzimanja u obzir toplotnih gubitaka i potrošnje toplote za disocijaciju CO 2 i H 2 O) je 400-1500 0 C. Ako se gas i vazduh zagreju pre sagorevanja , temperatura produkata sagorevanja može se značajno povećati.
Ferolegirani gas nastaje tokom topljenja ferolegura u pećima za redukciju rude. Plin dolazi iz zatvorene pećnice, može se koristiti kao gorivo SER (sekundarni energetski resursi). U otvorenim pećima, zbog slobodnog pristupa zraka, plin gori na vrhu. Prinos i sastav ferolegiranog gasa zavise od kvaliteta istopljenog
legura, sastav punjenja, način rada peći, njena snaga itd. Sastav gasa: 50-90% CO, 2-8% H2, 0,3-1% CH4, O2<1%, 2-5% CO 2 , остальное N 2 . Максимальная температура продуктов сгорания равна 2080 ^0 C. Запылённость газа составляет 30-40 г/м^3 .
Konverter gas nastaje tokom taljenja čelika u pretvaračima kiseonika. Gas se sastoji uglavnom od ugljen monoksida, njegov prinos i sastav značajno variraju tokom topljenja. Nakon prečišćavanja, sastav gasa je otprilike sljedeći: 70-80% CO; 15-20% CO 2 ; 0,5-0,8% O 2; 3-12% N 2. Toplota sagorevanja gasa je 8,4-9,2 MJ/m 3. Maksimalna temperatura sagorevanja dostiže 2000 0 C.
Koks gas nastaje tokom koksovanja mešavine uglja. U crnoj metalurgiji se koristi nakon ekstrakcije hemijskih proizvoda. Sastav koksnog gasa zavisi od svojstava uglja i uslova koksovanja. Zapreminski udjeli komponenti u gasu su u sljedećim granicama,%: 52-62H 2 ; 0,3-0,6 O 2; 23,5-26,5 CH 4; 5,5-7,7 CO; 1,8-2,6 CO 2 . Toplota sagorevanja je 17-17,6 MJ/m^3, maksimalna temperatura produkata sagorevanja je 2070 0 C.
Supstance organskog porijekla uključuju goriva koja pri sagorijevanju oslobađaju određenu količinu toplinske energije. Proizvodnja toplote mora biti okarakterisana visokom efikasnošću i odsustvom nuspojava, posebno supstanci štetnih po zdravlje ljudi i životnu sredinu.
Radi lakšeg utovara u ložište, drveni materijal se reže na pojedinačne elemente dužine do 30 cm.Da bi se povećala efikasnost njihove upotrebe, drvo za ogrev mora biti što suvo, a proces sagorevanja mora biti relativno spor. U mnogim aspektima, drvo od tvrdog drveta kao što su hrast i breza, lijeska i jasen, te glog pogodno je za grijanje prostorija. Zbog visokog sadržaja smole, povećane brzine gorenja i niske kalorijske vrijednosti, stabla četinara su u tom pogledu znatno inferiornija.
Treba shvatiti da na vrijednost kalorijske vrijednosti utiče gustina drveta.
To je prirodni materijal biljnog porijekla, ekstrahovan iz sedimentnih stijena.
Ova vrsta čvrstog goriva sadrži ugljenik i druge hemijske elemente. Postoji podjela materijala na vrste u zavisnosti od starosti. Mrki ugalj se smatra najmlađim, zatim kamenim ugljem, a antracit je stariji od svih ostalih vrsta. Starost zapaljive tvari također određuje njenu vlažnost, koja je prisutnija u mladom materijalu.
Prilikom sagorijevanja uglja dolazi do zagađivanja okoliša, a na rešetkama kotla se stvara šljaka koja u određenoj mjeri stvara prepreku normalnom sagorijevanju. Prisustvo sumpora u materijalu je takođe nepovoljan faktor za atmosferu, jer se u vazdušnom prostoru ovaj element pretvara u sumpornu kiselinu.
Međutim, potrošači se ne bi trebali bojati za svoje zdravlje. Proizvođači ovog materijala, vodeći računa o privatnim kupcima, nastoje da smanje sadržaj sumpora u njemu. Toplotna vrijednost uglja može varirati čak i unutar iste vrste. Razlika zavisi od karakteristika podvrste i njenog mineralnog sadržaja, kao i geografije proizvodnje. Kao čvrsto gorivo nalazi se ne samo čisti ugalj, već i nisko obogaćena ugljena šljaka, utisnuta u brikete.
Peleti (granule goriva) su čvrsta goriva proizvedena industrijski od drvnog i biljnog otpada: strugotine, kore, kartona, slame.
Sirovina usitnjena u prah se suši i sipa u granulator odakle izlazi u obliku granula određenog oblika. Za dodavanje viskoznosti masi koristi se biljni polimer, lignin. Složenost procesa proizvodnje i velika potražnja određuju cijenu peleta. Materijal se koristi u posebno opremljenim kotlovima.
Vrste goriva određuju se u zavisnosti od materijala od kojeg se prerađuju:
- oblo drvo bilo koje vrste;
- slama;
- treset;
- ljuska suncokreta.
Među prednostima koje imaju peleti za gorivo, vrijedi istaknuti sljedeće kvalitete:
- ekološka prihvatljivost;
- nemogućnost deformacije i otpornost na gljivice;
- lako skladištenje čak i na otvorenom;
- ujednačenost i trajanje sagorevanja;
- relativno niska cijena;
- Mogućnost korištenja za razne uređaje za grijanje;
- odgovarajuće veličine granula za automatsko punjenje u posebno opremljeni kotao.
Briketi
Briketi su čvrsta goriva koja su po mnogo čemu slična peletima. Za njihovu proizvodnju koriste se identični materijali: drvna sječka, strugotine, treset, ljuske i slama. U procesu proizvodnje sirovine se drobe i kompresijom formiraju u brikete. Ovaj materijal je i ekološki prihvatljivo gorivo. Pogodan je za skladištenje čak i na otvorenom. Glatko, ravnomjerno i sporo sagorijevanje ovog goriva može se primijetiti kako u kaminima i pećima, tako i u kotlovima za grijanje.
Vrste ekološki prihvatljivih čvrstih goriva o kojima smo gore govorili su dobra alternativa za proizvodnju topline. U poređenju sa fosilnim izvorima toplotne energije, koji sagorevanjem imaju negativan uticaj na životnu sredinu i koji su, osim toga, neobnovljivi, alternativna goriva imaju jasne prednosti i relativno nisku cenu, što je važno za određene kategorije potrošača.
U isto vrijeme, opasnost od požara takvih goriva je mnogo veća. Stoga je potrebno poduzeti određene sigurnosne mjere u pogledu njihovog skladištenja i upotrebe vatrootpornih materijala za zidove.
Tečna i gasovita goriva
Što se tiče tečnih i gasovitih zapaljivih materija, ovde je situacija sledeća.
Šta je gorivo?
Ovo je jedna komponenta ili mješavina tvari koje su sposobne za kemijske transformacije povezane s oslobađanjem topline. Različite vrste goriva razlikuju se po kvantitativnom sadržaju oksidatora koji se koristi za oslobađanje toplinske energije.
U širem smislu, gorivo je nosilac energije, odnosno potencijalna vrsta potencijalne energije.
Klasifikacija
Trenutno se vrste goriva dijele prema stanju agregacije na tečne, čvrste i plinovite.
Prirodni tvrdi materijali uključuju kamen, ogrevno drvo i antracit. Briketi, koks, termoantracit su vrste vještačkog čvrstog goriva.
Tečnosti obuhvataju supstance koje sadrže supstance organskog porekla. Njihove glavne komponente su: kiseonik, ugljenik, azot, vodonik, sumpor. Umjetno tekuće gorivo bit će razne smole i lož ulje.
To je mješavina raznih plinova: etilena, metana, propana, butana. Osim njih, plinovito gorivo sadrži ugljični dioksid i ugljični monoksid, sumporovodik, dušik, vodenu paru i kisik.

Indikatori goriva
Glavni indikator sagorevanja. Formula za određivanje kalorijske vrijednosti razmatra se u termohemiji. ispuštaju “standardno gorivo”, što podrazumijeva kaloričnu vrijednost od 1 kilograma antracita.
Lož ulje za domaćinstvo je namenjeno za sagorevanje u uređajima za grejanje male snage, koji se nalaze u stambenim prostorijama, generatorima toplote koji se koriste u poljoprivredi za sušenje stočne hrane, konzerviranje.
Specifična toplota sagorevanja goriva je vrednost koja pokazuje količinu toplote koja nastaje pri potpunom sagorevanju goriva zapremine 1 m 3 ili mase od jednog kilograma.
Za mjerenje ove vrijednosti koriste se J/kg, J/m3, kalorija/m3. Za određivanje topline sagorijevanja koristi se kalorimetrijska metoda.
Sa povećanjem specifične topline sagorijevanja goriva, specifična potrošnja goriva se smanjuje, a efikasnost ostaje nepromijenjena.
Toplota sagorevanja supstanci je količina energije koja se oslobađa tokom oksidacije čvrste, tečne ili gasovite supstance.
Određuje se hemijskim sastavom, kao i stanjem agregacije zapaljive supstance.

Karakteristike proizvoda sagorevanja
Više i niže kalorijske vrijednosti povezane su sa stanjem agregacije vode u tvarima dobivenim nakon sagorijevanja goriva.
Veća kalorijska vrijednost je količina topline koja se oslobađa tokom potpunog sagorijevanja tvari. Ova vrijednost uključuje i toplinu kondenzacije vodene pare.
Najmanja radna toplota sagorevanja je vrednost koja odgovara oslobađanju toplote tokom sagorevanja bez uzimanja u obzir toplote kondenzacije vodene pare.
Latentna toplota kondenzacije je količina energije kondenzacije vodene pare.

Matematički odnos
Više i niže kalorijske vrijednosti povezane su sljedećim odnosom:
QB = QH + k(W + 9H)
gdje je W količina po težini (u %) vode u zapaljivoj tvari;
H je količina vodonika (% po masi) u zapaljivoj tvari;
k - koeficijent jednak 6 kcal/kg

Metode za izvođenje proračuna
Više i niže kalorijske vrijednosti određuju se pomoću dvije glavne metode: proračunske i eksperimentalne.
Kalorimetri se koriste za izvođenje eksperimentalnih proračuna. Prvo se u njemu sagorijeva uzorak goriva. Toplina koja će se osloboditi voda u potpunosti apsorbira. Imajući ideju o masi vode, po promjeni njene temperature možete odrediti vrijednost topline sagorijevanja.
Ova tehnika se smatra jednostavnom i efikasnom; za nju je potrebno samo poznavanje podataka tehničke analize.
U metodi proračuna, više i niže kalorijske vrijednosti izračunavaju se pomoću formule Mendelejeva.
Q p H = 339C p +1030H p -109(O p -S p) - 25 W p (kJ/kg)
Uzima u obzir sadržaj ugljenika, kiseonika, vodonika, vodene pare, sumpora u radnom sastavu (u procentima). Količina toplote tokom sagorevanja određuje se uzimajući u obzir ekvivalentno gorivo.
Toplota sagorevanja gasa omogućava da se izvrše preliminarni proračuni i da se utvrdi efikasnost korišćenja određene vrste goriva.

Osobine porijekla
Da bismo razumjeli koliko se topline oslobađa prilikom sagorijevanja određenog goriva, potrebno je imati predstavu o njegovom porijeklu.
U prirodi postoje različite verzije čvrstih goriva, koje se razlikuju po sastavu i svojstvima.
Njegovo formiranje odvija se kroz nekoliko faza. Prvo se formira treset, zatim mrki i kameni ugalj, zatim antracit. Glavni izvori stvaranja čvrstog goriva su lišće, drvo i borove iglice. Kada dijelovi biljaka uginu i budu izloženi zraku, gljivice ih uništavaju i formiraju treset. Njegova akumulacija se pretvara u smeđu masu, a zatim se dobija smeđi gas.
Pri visokom pritisku i temperaturi smeđi gas se pretvara u ugalj, a zatim se gorivo akumulira u obliku antracita.
Pored organske materije, gorivo sadrži dodatni balast. Organskim se smatra onaj dio koji nastaje od organskih tvari: vodonika, ugljika, dušika, kisika. Pored ovih hemijskih elemenata, sadrži balast: vlagu, pepeo.
Tehnologija sagorevanja podrazumeva odvajanje radne, suve i zapaljive mase sagorelog goriva. Radna masa je gorivo u svom izvornom obliku koje se isporučuje potrošaču. Suva masa je sastav u kojem nema vode.

Compound
Najvrednije komponente su ugljenik i vodonik.
Ovi elementi se nalaze u bilo kojoj vrsti goriva. U tresetu i drvetu udio ugljika dostiže 58 posto, u kamenom i mrkom uglju - 80 posto, au antracitu 95 posto po težini. U zavisnosti od ovog indikatora, količina toplote koja se oslobađa tokom sagorevanja goriva se menja. Vodonik je drugi najvažniji element svakog goriva. Kada se veže s kisikom, stvara vlagu, što značajno smanjuje toplinsku vrijednost bilo kojeg goriva.
Njegov procenat se kreće od 3,8 u uljnim škriljcima do 11 u lož ulju. Kiseonik sadržan u gorivu djeluje kao balast.
Nije kemijski element koji stvara toplinu, stoga negativno utječe na vrijednost svoje topline sagorijevanja. Sagorijevanje dušika, sadržanog u slobodnom ili vezanom obliku u produktima sagorijevanja, smatra se štetnim nečistoćama, stoga je njegova količina strogo ograničena.
Sumpor je uključen u gorivo u obliku sulfata, sulfida, a također i kao plinovi sumpor-dioksida. Kada su hidrirani, oksidi sumpora stvaraju sumpornu kiselinu, koja uništava kotlovsku opremu i negativno utiče na vegetaciju i žive organizme.
Zbog toga je sumpor hemijski element čije je prisustvo u prirodnom gorivu krajnje nepoželjno. Ako jedinjenja sumpora dospeju u radni prostor, izazivaju značajno trovanje operativnog osoblja.
Postoje tri vrste pepela u zavisnosti od porekla:
- primarni;
- sekundarni;
- tercijarni
Primarna vrsta se formira od minerala koji se nalaze u biljkama. Sekundarni pepeo nastaje kao rezultat ulaska biljnih ostataka u pijesak i tlo tokom formiranja.
Tercijarni pepeo se pojavljuje u sastavu goriva tokom ekstrakcije, skladištenja i transporta. Sa značajnim taloženjem pepela dolazi do smanjenja prijenosa topline na grijaćoj površini kotlovske jedinice, smanjujući količinu prijenosa topline na vodu iz plinova. Ogromna količina pepela negativno utječe na rad kotla.
Konačno
Isparljive supstance imaju značajan uticaj na proces sagorevanja bilo koje vrste goriva. Što je njihova snaga veća, to će biti veća zapremina fronta plamena. Na primjer, ugljen i treset se lako zapale, proces je praćen manjim gubicima topline. Koks koji ostaje nakon uklanjanja isparljivih nečistoća sadrži samo mineralne i ugljične spojeve. U zavisnosti od karakteristika goriva, količina toplote se značajno menja.
U zavisnosti od hemijskog sastava, postoje tri faze formiranja čvrstog goriva: treset, lignit i ugalj.
Prirodno drvo se koristi u malim kotlovskim instalacijama. Uglavnom koriste sečku, piljevinu, ploče, koru, a samo ogrevno drvo se koristi u malim količinama. U zavisnosti od vrste drveta, količina proizvedene toplote značajno varira.
Kako se toplina sagorijevanja smanjuje, drvo za ogrjev stječe određene prednosti: brzu zapaljivost, minimalan sadržaj pepela i odsutnost tragova sumpora.
Pouzdane informacije o sastavu prirodnog ili sintetičkog goriva, njegovoj kalorijskoj vrijednosti, odličan su način za izvođenje termohemijskih proračuna.
Trenutno postoji prava prilika da se identifikuju one glavne opcije za čvrsta, gasovita, tečna goriva koja će biti najefikasnija i najjeftinija za upotrebu u određenoj situaciji.
U tablicama su prikazane masene specifične topline sagorijevanja goriva (tečnog, čvrstog i plinovitog) i nekih drugih zapaljivih materijala. Razmatrana su sledeća goriva: ugalj, ogrevno drvo, koks, treset, kerozin, nafta, alkohol, benzin, prirodni gas itd.
Lista tabela:
Tokom egzotermne reakcije oksidacije goriva, njegova hemijska energija se pretvara u toplotnu energiju uz oslobađanje određene količine toplote. Rezultirajuća toplinska energija se obično naziva toplinom sagorijevanja goriva. Zavisi od njegovog hemijskog sastava, vlažnosti i glavni je. Toplina sagorevanja goriva po 1 kg mase ili 1 m 3 zapremine čini masu ili zapreminsku specifičnu toplotu sagorevanja.
Specifična toplota sagorevanja goriva je količina toplote koja se oslobađa tokom potpunog sagorevanja jedinice mase ili zapremine čvrstog, tečnog ili gasovitog goriva. U Međunarodnom sistemu jedinica, ova vrijednost se mjeri u J/kg ili J/m3.
Specifična toplota sagorevanja goriva može se odrediti eksperimentalno ili izračunati analitički. Eksperimentalne metode za određivanje kalorijske vrijednosti zasnivaju se na praktičnom mjerenju količine topline koja se oslobađa pri sagorijevanju goriva, na primjer u kalorimetru s termostatom i bombom za sagorijevanje. Za gorivo poznatog hemijskog sastava, specifična toplota sagorevanja može se odrediti pomoću periodične formule.
Postoje veće i niže specifične toplote sagorevanja. Veća kalorijska vrijednost jednaka je maksimalnoj količini topline koja se oslobađa tijekom potpunog sagorijevanja goriva, uzimajući u obzir toplinu koja se troši na isparavanje vlage sadržane u gorivu. Najmanja toplota sagorevanja manja je od najveće vrednosti za količinu toplote kondenzacije, koja nastaje od vlage goriva i vodonika organske mase, koja se tokom sagorevanja pretvara u vodu.
Za određivanje pokazatelja kvaliteta goriva, kao iu termičkim proračunima obično koriste nižu specifičnu toplotu sagorevanja, što je najvažnija termička i performansna karakteristika goriva i prikazana je u tabelama ispod.
Specifična toplota sagorevanja čvrstih goriva (ugalj, ogrevno drvo, treset, koks)
U tabeli su prikazane vrijednosti specifične topline sagorijevanja suhog čvrstog goriva u dimenziji MJ/kg. Gorivo u tabeli je poredano po nazivima po abecednom redu.
Od razmatranih čvrstih goriva, najvišu toplotnu vrijednost ima koksni ugalj - njegova specifična toplina sagorijevanja je 36,3 MJ/kg (ili u SI jedinicama 36,3·10 6 J/kg). Osim toga, visoka kalorična vrijednost karakteristična je za kameni ugalj, antracit, drveni i mrki ugalj.
Goriva sa niskom energetskom efikasnošću uključuju drvo, ogrevno drvo, barut, mleveni treset i uljni škriljac. Na primjer, specifična toplina sagorijevanja drva za ogrjev je 8,4...12,5, a baruta samo 3,8 MJ/kg.
| Gorivo | |
|---|---|
| Antracit | 26,8…34,8 |
| Drveni peleti (peleti) | 18,5 |
| Suvo ogrevno drvo | 8,4…11 |
| Ogrevno drvo od suhe breze | 12,5 |
| Gasni koks | 26,9 |
| Eksplozija koksa | 30,4 |
| Polukoks | 27,3 |
| Puder | 3,8 |
| Slate | 4,6…9 |
| Uljni škriljci | 5,9…15 |
| Čvrsto raketno gorivo | 4,2…10,5 |
| Treset | 16,3 |
| Vlaknasti treset | 21,8 |
| Mljeveni treset | 8,1…10,5 |
| Tresetna mrvica | 10,8 |
| Mrki ugalj | 13…25 |
| Mrki ugalj (briketi) | 20,2 |
| Mrki ugalj (prašina) | 25 |
| Donjeck ugalj | 19,7…24 |
| Ugalj | 31,5…34,4 |
| Ugalj | 27 |
| Koksni ugalj | 36,3 |
| Kuznjecki ugalj | 22,8…25,1 |
| Čeljabinsk ugalj | 12,8 |
| Ekibastuski ugalj | 16,7 |
| Frestorf | 8,1 |
| Šljaka | 27,5 |
Specifična toplota sagorevanja tečnih goriva (alkohol, benzin, kerozin, ulje)
Data je tabela specifične toplote sagorevanja tečnog goriva i nekih drugih organskih tečnosti. Treba napomenuti da goriva kao što su benzin, dizel gorivo i ulje imaju veliko oslobađanje toplote tokom sagorevanja.
Specifična toplota sagorevanja alkohola i acetona je znatno niža od tradicionalnih motornih goriva. Osim toga, tečno raketno gorivo ima relativno nisku kaloričnu vrijednost i, uz potpuno sagorijevanje 1 kg ovih ugljovodonika, oslobodit će se količina topline jednaka 9,2 odnosno 13,3 MJ.
| Gorivo | Specifična toplota sagorevanja, MJ/kg |
|---|---|
| Aceton | 31,4 |
| Benzin A-72 (GOST 2084-67) | 44,2 |
| Avio-benzin B-70 (GOST 1012-72) | 44,1 |
| Benzin AI-93 (GOST 2084-67) | 43,6 |
| Benzen | 40,6 |
| Zimsko dizel gorivo (GOST 305-73) | 43,6 |
| Ljetno dizel gorivo (GOST 305-73) | 43,4 |
| Tečno raketno gorivo (kerozin + tečni kiseonik) | 9,2 |
| Avijacijski kerozin | 42,9 |
| Kerozin za rasvjetu (GOST 4753-68) | 43,7 |
| Xylene | 43,2 |
| Lož ulje sa visokim sadržajem sumpora | 39 |
| Lož ulje sa niskim sadržajem sumpora | 40,5 |
| Lož ulje sa niskim sadržajem sumpora | 41,7 |
| Sumporno lož ulje | 39,6 |
| metil alkohol (metanol) | 21,1 |
| n-butil alkohol | 36,8 |
| Ulje | 43,5…46 |
| Metansko ulje | 21,5 |
| Toluen | 40,9 |
| Vajt špirit (GOST 313452) | 44 |
| Etilen glikol | 13,3 |
| etil alkohol (etanol) | 30,6 |
Specifična toplota sagorevanja gasovitih goriva i zapaljivih gasova
Prikazana je tabela specifične toplote sagorevanja gasovitog goriva i nekih drugih zapaljivih gasova u dimenziji MJ/kg. Od gasova koji se razmatraju, on ima najveću masenu specifičnu toplotu sagorevanja. Potpuno sagorevanje jednog kilograma ovog gasa će osloboditi 119,83 MJ toplote. Takođe, gorivo kao što je prirodni gas ima visoku toplotnu vrednost - specifična toplota sagorevanja prirodnog gasa je 41...49 MJ/kg (za čisti gas je 50 MJ/kg).
| Gorivo | Specifična toplota sagorevanja, MJ/kg |
|---|---|
| 1-Buten | 45,3 |
| Amonijak | 18,6 |
| Acetilen | 48,3 |
| Vodonik | 119,83 |
| Vodik, mješavina s metanom (50% H 2 i 50% CH 4 po težini) | 85 |
| Vodik, mješavina s metanom i ugljičnim monoksidom (33-33-33% po težini) | 60 |
| Vodik, mješavina s ugljičnim monoksidom (50% H 2 50% CO 2 po težini) | 65 |
| Plin iz visoke peći | 3 |
| Koksni plin | 38,5 |
| Tečni ugljikovodični plin LPG (propan-butan) | 43,8 |
| izobutan | 45,6 |
| Metan | 50 |
| n-butan | 45,7 |
| n-heksan | 45,1 |
| n-pentan | 45,4 |
| Povezani gas | 40,6…43 |
| Prirodni gas | 41…49 |
| Propadiene | 46,3 |
| Propan | 46,3 |
| propilen | 45,8 |
| Propilen, mješavina sa vodonikom i ugljičnim monoksidom (90%-9%-1% po težini) | 52 |
| Ethane | 47,5 |
| Etilen | 47,2 |
Specifična toplota sagorevanja nekih zapaljivih materijala
Data je tabela specifične toplote sagorevanja nekih zapaljivih materijala (drvo, papir, plastika, slama, guma itd.). Treba obratiti pažnju na materijale sa visokim oslobađanjem toplote tokom sagorevanja. Takvi materijali uključuju: gumu raznih vrsta, ekspandirani polistiren (pjena), polipropilen i polietilen.
| Gorivo | Specifična toplota sagorevanja, MJ/kg |
|---|---|
| Papir | 17,6 |
| Leatherette | 21,5 |
| Drvo (šipke sa 14% sadržaja vlage) | 13,8 |
| Drvo u hrpama | 16,6 |
| Hrastovo drvo | 19,9 |
| Drvo smreke | 20,3 |
| Drvo zeleno | 6,3 |
| Borovo drvo | 20,9 |
| Capron | 31,1 |
| Karbolit proizvodi | 26,9 |
| Karton | 16,5 |
| Stiren butadien guma SKS-30AR | 43,9 |
| Prirodna guma | 44,8 |
| Sintetička guma | 40,2 |
| Rubber SKS | 43,9 |
| Hloroprenska guma | 28 |
| Linoleum od polivinilklorida | 14,3 |
| Dvoslojni polivinilhloridni linoleum | 17,9 |
| Linoleum od polivinilklorida na bazi filca | 16,6 |
| Polivinilhloridni linoleum na toploj bazi | 17,6 |
| Linoleum od polivinil hlorida na platnu | 20,3 |
| Gumeni linoleum (Relin) | 27,2 |
| Parafin parafin | 11,2 |
| Polistirenska pjena PVC-1 | 19,5 |
| Pjenasta plastika FS-7 | 24,4 |
| Pjenasta plastika FF | 31,4 |
| Ekspandirani polistiren PSB-S | 41,6 |
| Poliuretanska pjena | 24,3 |
| Vlaknaste ploče | 20,9 |
| polivinil hlorid (PVC) | 20,7 |
| Polikarbonat | 31 |
| Polipropilen | 45,7 |
| Polistiren | 39 |
| Polietilen visokog pritiska | 47 |
| Polietilen niskog pritiska | 46,7 |
| Guma | 33,5 |
| Ruberoid | 29,5 |
| Kanalska čađ | 28,3 |
| Hay | 16,7 |
| Slama | 17 |
| Organsko staklo (pleksiglas) | 27,7 |
| Tekstolit | 20,9 |
| Tol | 16 |
| TNT | 15 |
| Pamuk | 17,5 |
| Celuloza | 16,4 |
| Vuna i vunena vlakna | 23,1 |
Izvori:
- GOST 147-2013 Čvrsto mineralno gorivo. Određivanje veće toplotne vrednosti i izračunavanje niže toplotne vrednosti.
- GOST 21261-91 Naftni proizvodi. Metoda za određivanje veće toplotne vrednosti i izračunavanje niže toplotne vrednosti.
- GOST 22667-82 Prirodni zapaljivi gasovi. Metoda proračuna za određivanje kalorijske vrijednosti, relativne gustine i Vobeovog broja.
- GOST 31369-2008 Prirodni gas. Proračun kalorijske vrijednosti, gustine, relativne gustine i Vobeovog broja na osnovu sastava komponenti.
- Zemsky G. T. Zapaljiva svojstva neorganskih i organskih materijala: referentna knjiga M.: VNIIPO, 2016 - 970 str.