Normalna brzina širenja plamena. Uticaj različitih faktora na brzinu plamena Maksimalna brzina plamena sagorevanja propana
Iznad površine tekućine ili čvrste tvari na bilo kojoj temperaturi nalazi se mješavina para-vazduh, čiji je pritisak u stanju ravnoteže određen pritiskom zasićenih para ili njihovom koncentracijom. Sa povećanjem temperature, pritisak zasićene pare će se povećati, ali eksponencijalno (Clapeyron - Clausis jednadžba):
gdje je P n „ - pritisak zasićene pare, Pa; Q„ C11 - toplota isparavanja, kJ/mol; T - temperatura tečnosti, K.
Za svaku tečnost postoji temperaturni opseg u kojem će koncentracija zasićenih para iznad ogledala (površine tečnosti) biti u području paljenja, tj. NKPV
Da bi se stvorio LCVV para, dovoljno je zagrijati ne cijelu tekućinu, već samo njen površinski sloj, na temperaturu jednaku LTPV.
U prisustvu izvora paljenja, takva mješavina će se moći zapaliti. U praksi se češće koriste koncepti "tačka paljenja" i "temperatura paljenja".
Tačka paljenja - minimalna temperatura tečnosti pri kojoj se koncentracija pare formira iznad njene površine, koja se može zapaliti od izvora paljenja, ali brzina stvaranja pare nije dovoljna za održavanje sagorevanja.
Dakle, i na tački paljenja i na donjoj temperaturnoj granici paljenja iznad površine tečnosti, formira se donja granica koncentracije paljenja, međutim, u poslednjem slučaju, LEL se stvara zasićenim parama. Stoga je tačka paljenja uvijek nešto viša od LTLW. Iako na tački paljenja dolazi do kratkotrajnog paljenja pare, koja se ne može pretvoriti u stabilno sagorevanje tečnosti, ipak, pod određenim uslovima, bljesak može izazvati požar.
Tačka paljenja je uzeta kao osnova za klasifikaciju tečnosti na zapaljive (zapaljive tečnosti) i zapaljive tečnosti (FL). Zapaljive tečnosti uključuju tečnosti sa tačkom paljenja u zatvorenoj posudi od 61°C i niže, zapaljive tečnosti sa tačkom paljenja većom od 61°C.
Eksperimentalno se određuje tačka paljenja u otvorenim i zatvorenim uređajima. U zatvorenim posudama, tačke paljenja su uvijek niže nego u otvorenim posudama, jer u tom slučaju tečne pare imaju priliku da difundiraju u atmosferu i potrebna je viša temperatura da bi se stvorila zapaljiva koncentracija iznad površine.
U tabeli. 2.4 prikazana je tačka paljenja nekih tečnosti, određena uređajima otvorenog i zatvorenog tipa.
Tabela 2.4
Tačka paljenja različitih vrsta tečnosti sa različitim metodama određivanja
Temperatura paljenja - minimalna temperatura tečnosti na kojoj se, nakon paljenja para iz izvora paljenja, uspostavlja stacionarno sagorevanje.
U zapaljivim tečnostima temperatura paljenja je viša od tačke paljenja za 1-5°, dok što je niža tačka paljenja, to je manja razlika između tačaka paljenja i paljenja.
Za zapaljive tekućine s visokom tačkom paljenja, razlika između ovih temperatura doseže 25-35 °. Postoji korelacija između tačke paljenja u zatvorenom lončiću i donje granice temperature paljenja, opisane formulom
Ova relacija vrijedi za G V(.
Značajna zavisnost temperature bljeska i paljenja od eksperimentalnih uslova uzrokuje određene poteškoće u kreiranju proračunske metode za procjenu njihovih vrijednosti. Jedna od najčešćih od njih je poluempirijska metoda koju je predložio V. I. Blinov:
gdje je G sunce - tačka paljenja (paljenja), K; R np - parcijalni pritisak zasićene pare tečnosti na tački paljenja (paljenja), Pa; D()- koeficijent difuzije tečnih para, s/m 2 ; b- broj molekula kisika potrebnih za potpunu oksidaciju jednog molekula goriva; AT - konstanta metode definicije.
Prilikom izračunavanja tačke paljenja u zatvorenoj posudi, preporučljivo je uzeti AT= 28, u otvorenoj posudi AT= 45; za izračunavanje temperature paljenja, uzmite AT = 53.
Granice zapaljive temperature mogu se izračunati:
Prema poznatim vrijednostima tačke ključanja
gde je ^n(v)' 7/ip - donja (gornja) temperaturna granica paljenja i tačke ključanja, respektivno, °C; k, ja- parametri, čije vrijednosti ovise o vrsti zapaljive tekućine;
Prema poznatim vrijednostima graničnih koncentracija. Da biste to učinili, prvo odredite koncentraciju zasićenih para iznad površine tekućine
gdje je (r„ n koncentracija zasićenih para, %; R n p - pritisak zasićene pare, Pa; P 0 - vanjski (atmosferski) pritisak, Pa.
Iz formule (2.41) slijedi
Odredivši tlak zasićene pare vrijednošću donje (gornje) granice paljenja, nalazimo temperaturu na kojoj se ovaj tlak postiže. To je donja (gornja) temperaturna granica paljenja.
Koristeći formulu (2.41), može se riješiti i inverzni problem: izračunati granice koncentracije paljenja iz poznatih vrijednosti temperaturnih granica.
Svojstvo plamena na spontano širenje uočeno je ne samo pri sagorijevanju mješavine zapaljivih plinova s oksidacijskim sredstvom, već i prilikom sagorevanja tečnosti i čvrste materije. Pod lokalnom izloženošću izvoru toplote, na primer, otvorenom plamenu, tečnost će se zagrejati, brzina isparavanja će se povećati, a kada površina tečnosti dostigne temperaturu paljenja, mešavina para i vazduha će se zapaliti na mestu izlaganjem izvoru toplote uspostaviće se stabilan plamen koji će se potom određenom brzinom širiti po površini i hladnom delu tečnosti.
Koja je pokretačka sila širenja procesa sagorevanja, koji je njegov mehanizam?
Širenje plamena preko površine tečnosti odvija se kao rezultat prenosa toplote usled zračenja, konvekcije i molekularne provodljivosti toplote od zone plamena do površine ogledala tečnosti.
Prema savremenim konceptima, glavna pokretačka snaga za širenje procesa sagorevanja je toplotno zračenje iz plamena. Poznato je da plamen, koji ima visoku temperaturu (više od 1000 °C), može zračiti toplotnu energiju. Prema Stefan-Boltzmannovom zakonu, intenzitet toplotnog fluksa zračenja koji daje zagrijano tijelo određen je relacijom
gdje c i- intenzitet toplotnog toka zračenja, kW/m 2 ; 8 0 - stepen crnila tijela (plamen) (e 0 = 0,75-H.0); a = = 5,7 10 11 kJ / (m 2 s K 4) - Stefan-Boltzmannova konstanta; G g - temperatura tijela (plamena), K; G 0 - temperatura medija, K.
Toplina, koja zrači u svim smjerovima, djelomično ulazi u područja površine tekućine koja se još nisu zapalila, zagrijavajući ih. Sa povećanjem temperature površinskog sloja iznad zagrijanog područja, proces isparavanja tekućine se intenzivira i formira se mješavina para i zraka. Čim koncentracija tečne pare pređe NKVP, ona će se zapaliti iz plamena. Zatim, ovaj dio površine tekućine počinje intenzivno zagrijavati susjedni dio površine tekućine i tako dalje. Brzina širenja plamena kroz tečnost zavisi od brzine zagrevanja površine tečnosti zračenjem toplotnog toka iz plamena, tj. o brzini formiranja zapaljive mješavine para-vazduh iznad površine tečnosti, koja zauzvrat zavisi od prirode tečnosti i početne temperature.
Svaka vrsta tečnosti ima sopstvenu toplotu isparavanja i tačku paljenja. Što su njihove vrijednosti veće, što je duže vrijeme potrebno za njegovo zagrijavanje da se formira zapaljiva smjesa para-vazduh, to je manja brzina širenja plamena. S povećanjem molekularne mase tvari unutar istog homolognog niza, tlak pare elastičnosti se smanjuje, toplina isparavanja i plamenište se povećavaju, a brzina širenja plamena se shodno tome smanjuje.
Povećanjem temperature tečnosti povećava se brzina širenja plamena, jer se smanjuje vreme potrebno da se tečnost zagreje do tačke paljenja ispred zone sagorevanja.
Prilikom bljeska, brzina širenja plamena duž tečnog ogledala biće (po fizičkom smislu) jednaka brzini širenja plamena kroz mešavinu para-vazduh sastava bliskog LCV, tj. 4-5 cm/s. Sa povećanjem početne temperature tečnosti iznad tačke paljenja, brzina širenja plamena zavisiće (slično kao i brzina širenja plamena) od sastava zapaljive smeše. Zaista, kako temperatura tečnosti poraste iznad tačke paljenja, koncentracija mešavine para i vazduha iznad površine ogledala će se povećati sa NKVP na 100% (tačka ključanja).
Stoga, u početku, kako temperatura tečnosti raste od tačke paljenja do temperature na kojoj se zasićene pare formiraju iznad površine, sa koncentracijom jednakom stehiometrijskoj (tačnije, nešto višoj od stehiometrijske), brzina širenja plamena će se povećati. U zatvorenim posudama, kako temperatura tekućine dalje raste, brzina širenja plamena počinje opadati, sve do brzine koja odgovara gornjoj temperaturnoj granici paljenja, pri kojoj širenje plamena i mješavine para i zraka više neće biti moguća zbog nedostatka kiseonika u mešavini para i vazduha iznad površine tečnosti. Iznad površine otvorenog rezervoara, koncentracija para na različitim nivoima će biti različita: na površini će biti maksimalna i odgovarati koncentraciji zasićene pare na datoj temperaturi, kako se rastojanje od površine povećava, koncentracija će postupno se smanjuju zbog konvektivne i molekularne difuzije.
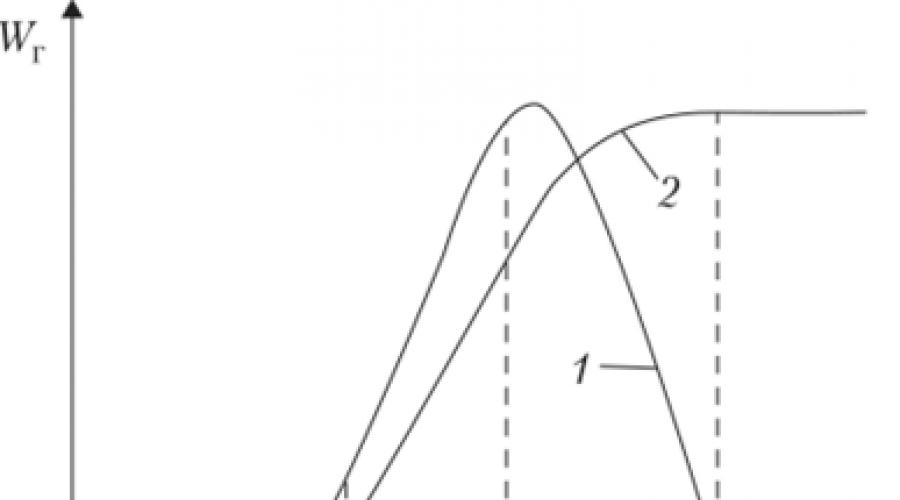
Pri temperaturi tečnosti blizu tačke paljenja, brzina širenja plamena po površini tečnosti biće jednaka brzini njegovog širenja kroz smešu para u vazduhu na LIP, tj. 3-4 cm/s. U ovom slučaju, front plamena će se nalaziti blizu površine tečnosti. Daljnjim povećanjem početne temperature tekućine, brzina širenja plamena će se povećati slično rastu normalne brzine širenja plamena u mješavini para i zraka s povećanjem njene koncentracije. Pri maksimalnoj brzini, plamen će se širiti kroz smjesu s koncentracijom bliskom stehiometrijskoj. Shodno tome, sa povećanjem početne temperature tečnosti iznad G stx, brzina širenja plamena će ostati konstantna, jednaka maksimalnoj vrednosti brzine širenja sagorevanja u stehiometrijskoj smeši ili nešto veća od nje (slika 2.5). dakle,

Rice. 25.
1 - goruća tečnost u zatvorenoj posudi; 2 - sagorijevanje tekućine u otvorenom spremniku s promjenom početne temperature tekućine u otvorenom spremniku u širokom temperaturnom rasponu (do tačke ključanja), brzina širenja plamena će varirati od nekoliko milimetara do 3-4 m / s.
Pri maksimalnoj brzini, plamen će se širiti kroz smjesu s koncentracijom bliskom stehiometrijskoj. Sa povećanjem temperature tečnosti iznad Gstx, rastojanje iznad tečnosti će se povećati, pri čemu će se formirati stehiometrijska koncentracija, a brzina širenja plamena će ostati ista (vidi sliku 2.5). Ovu okolnost treba uvijek imati na umu, kako pri organizaciji preventivnog rada, tako i pri gašenju požara, kada, na primjer, može postojati opasnost od usisavanja zraka u zatvoreni spremnik - njegovo smanjenje tlaka.
Nakon paljenja tečnosti i širenja plamena se uspostavlja njegova površina difuzijski način njegovog sagorevanja, koju karakteriše specifična masa WrM i linearne W V Jl brzine.
Specifična brzina mase - masa tvari koja izgori iz jedinice površine tekućeg ogledala u jedinici vremena (kg / (m 2 * s)).
Linearna brzina - udaljenost na kojoj se nivo ogledala tečnosti kreće u jedinici vremena zbog njegovog sagorevanja (m / s).
Masovna i linearna stopa sagorevanja su međusobno povezane preko gustine tečnosti p:
Nakon paljenja tekućine, temperatura njene površine raste od temperature paljenja do ključanja i formira se zagrijani sloj. Tokom ovog perioda, brzina izgaranja tečnosti postepeno se povećava, visina plamena raste u zavisnosti od prečnika rezervoara i vrste zapaljive tečnosti. Nakon 1-10 minuta izgaranja, proces se stabilizuje: brzina izgaranja i dimenzije plamena ostaju nepromijenjene u budućnosti.
Visina i oblik plamena pri difuzionom sagorevanju tečnosti i gasa podležu istim zakonima, jer je u oba slučaja proces sagorevanja određen međusobnom difuzijom goriva i oksidatora. Međutim, ako tokom difuzionog sagorevanja gasova brzina gasnog mlaza ne zavisi od procesa koji se odvijaju u plamenu, tada se tokom sagorevanja tečnosti uspostavlja određena brzina sagorevanja, koja zavisi i od termodinamičkih parametara plamena. tečnosti i o uslovima difuzije kiseonika vazduha i tečne pare.
Između zone sagorevanja i površine tečnosti uspostavlja se određeni prenos toplote i mase (slika 2.6). Dio toplotnog toka koji dolazi na površinu tečnosti q 0y troši se na zagrijavanje do tačke ključanja q ucn . Osim toga, toplo q CT za zagrijavanje tekućina dolazi iz baklje plamena kroz zidove spremnika zbog provodljivosti topline. Sa dovoljno velikim prečnikom q CT onda se može zanemariti q() = K „ n +
Očigledno je da
gde je c toplotni kapacitet tečnosti, kJDkg-K); p je gustina tečnosti, kg / m 3; Wnc- brzina rasta zagrijanog sloja, m/s; W Jl- linearna brzina sagorevanja, m/s; 0i SP - toplota isparavanja, kJ/kg; G kip - tačka ključanja tečnosti, K.

Rice. 2.6.
G () - početna temperatura; G kip - tačka ključanja;
T g- temperatura sagorevanja; q KUW q Jl - konvektivni i radijantni toplotni tokovi; q 0 - toplotni tok koji ulazi na površinu tečnosti
Iz formule (2.45) slijedi da intenzitet toplotnog toka iz zone plamena određuje određenu brzinu dovoda goriva u ovu zonu, čija kemijska interakcija s oksidantom, zauzvrat, utječe na vrijednost # 0 . U tome se sastoji odnos mase i izmjena toplote između zone plamena i kondenzovane faze tokom sagorevanja tečnosti i čvrstih materija.
Procjena udjela topline iz ukupnog oslobađanja topline pri sagorijevanju tečnosti, koja se troši na njenu pripremu za sagorevanje q 0 , može se izvesti u sljedećem redoslijedu.
Uzimajući za jednostavnost wrijl= W nx , dobijamo
Brzina oslobađanja topline po jedinici površine tekućeg ogledala (specifična toplina vatre qll7K) može se odrediti formulom
gdje je Q H najniža kalorijska vrijednost supstance, kJ/kg; P p - koeficijent potpunog sagorevanja.
Zatim, uzimajući u obzir stanje (2.44) i dijeljenje izraza (2.45) formulom (2.46), dobijamo
Proračuni pokazuju da se oko 2% ukupnog oslobađanja toplote pri sagorevanju tečnosti troši na formiranje i dopremanje tečne pare u zonu sagorevanja. Kada se uspostavi proces sagorijevanja, temperatura površine tekućine raste do točke ključanja, koja nakon toga ostaje nepromijenjena. Ova izjava se odnosi na pojedinačnu tečnost. Ako, međutim, uzmemo u obzir mješavine tekućina koje imaju različite točke ključanja, tada u početku dolazi do oslobađanja frakcija laganog ključanja, a zatim - onih sa sve većim ključanjem.
Na brzinu sagorijevanja značajno utječe zagrijavanje tekućine u dubini kao rezultat prijenosa topline iz tekućine zagrijane zračenjem q0 površine tečnosti do njene dubine. Ovaj prijenos topline vrši toplotna provodljivost i konvencije.
Zagrijavanje tečnosti zbog toplotne provodljivosti može se predstaviti eksponencijalnom zavisnošću oblika
gdje T x - temperatura sloja tečnosti na dubini X, TO; G kip - temperatura površine (tačka ključanja), K; k- koeficijent proporcionalnosti, m -1 .
Ova vrsta temperaturnog polja se zove raspodjela temperature prve vrste(Sl. 2.7).
Laminarna konvencija nastaje kao rezultat različitih temperatura tečnosti na zidovima rezervoara iu njegovom centru, kao i zbog frakcione destilacije u gornjem sloju tokom sagorevanja smeše.
Dodatni prijenos topline sa zagrijanih zidova rezervoara na tekućinu dovodi do zagrijavanja njegovih slojeva u blizini zidova na višu temperaturu nego u centru. Tečnost zagrijana u blizini zidova (ili čak mjehurići pare ako se zagrije u blizini zidova iznad tačke ključanja) se diže, što doprinosi intenzivnom miješanju i brzom zagrijavanju tekućine na velikoj dubini. tzv homotermalni sloj, one. sloj sa praktično konstantnom temperaturom, čija se debljina povećava tokom sagorevanja. Takvo temperaturno polje se naziva distribucija temperature druge vrste.

Rice. 2.7.
1 - raspodjela temperature prve vrste; 2 - raspodjela temperature druge vrste
Formiranje homotermalnog sloja moguće je i kao rezultat frakcijske destilacije pripovršinskih slojeva mješavine tekućina s različitim tačkama ključanja. Kako takve tečnosti sagorevaju, sloj blizu površine obogaćuje se gušćim frakcijama visokog ključanja, koje tonu nadole, doprinoseći najkonvektivnijem zagrevanju tečnosti.
Utvrđeno je da što je niža tačka ključanja tečnosti (dizel gorivo, transformatorsko ulje), to je teže formiranje homotermnog sloja. Kada izgore, temperatura zidova rezervoara retko prelazi tačku ključanja. Međutim, pri spaljivanju vlažnih naftnih proizvoda visokog ključanja, vjerojatnost stvaranja homotermalnog sloja je prilično visoka. Kada se zidovi rezervoara zagreju na 100°C i više, formiraju se mjehurići vodene pare koji, jureći prema gore, uzrokuju intenzivno kretanje cjelokupne tekućine i brzo zagrijavanje u dubini. Ovisnost debljine homotermalnog sloja o vremenu gorenja opisana je relacijom
gdje X - debljina homotermnog sloja u određenom trenutku vremena sagorevanja, m; x pr - granična debljina homotermnog sloja, m; t je vrijeme koje se računa od početka formiranja sloja, s; p - koeficijent, s -1.
Mogućnost stvaranja dovoljno debelog homotermalnog sloja tokom sagorijevanja vlažnih naftnih proizvoda prepuna je pojave ključanja i izbacivanja tekućine.
Brzina sagorijevanja značajno ovisi o vrsti tekućine, početnoj temperaturi, vlažnosti i koncentraciji kisika u atmosferi.
Iz jednačine (2.45), uzimajući u obzir izraz (2.44), moguće je odrediti stopu sagorijevanja mase:

Očigledno je iz formule (2.50) da na brzinu izgaranja utiče intenzitet toplotnog fluksa koji dolazi od plamena do tečnog ogledala i termofizički parametri goriva: tačka ključanja, toplotni kapacitet i toplota isparavanja.
Iz tabele. 2.5 očigledno je da postoji određena korespondencija između stope sagorevanja i troškova toplote za zagrevanje i isparavanje tečnosti. Dakle, u seriji benzenksilenglicerola, s povećanjem potrošnje topline za grijanje i isparavanje, stopa sagorijevanja opada. Međutim, pri prelasku iz benzena u dietil eter, troškovi topline se smanjuju. Ova očigledna razlika je zbog razlike u intenzitetu toplotnih tokova koji dolaze od plamena do površine tečnosti. Fluks zračenja je dovoljno velik za zadimljeni plamen benzena i mali za relativno proziran plamen dietil etera. U pravilu je omjer stope sagorijevanja tečnosti sa najbržim sagorevanjem i najsporije gorućih tečnosti prilično mali i iznosi 3,0-4,5.
Tabela 25
Ovisnost brzine sagorijevanja o potrošnji topline za grijanje i isparavanje
Iz izraza (2.50) proizilazi da sa povećanjem G 0 stopa sagorijevanja raste, jer se troškovi topline za zagrijavanje tekućine do točke ključanja smanjuju.
Sadržaj vlage u smjesi smanjuje brzinu sagorijevanja tekućine, prvo, zbog dodatne potrošnje topline za njeno isparavanje, a drugo, kao rezultat flegmatizirajućeg efekta vodene pare u plinskoj zoni. Ovo posljednje dovodi do smanjenja temperature plamena, pa se prema formuli (2.43) smanjuje i njegova snaga zračenja. Strogo govoreći, brzina izgaranja vlažne tekućine (tečnost koja sadrži vodu) nije konstantna, povećava se ili smanjuje tokom procesa sagorijevanja ovisno o tački ključanja tekućine.
Mokro gorivo se može predstaviti kao mešavina dve tečnosti: gorivo + voda, pri čijem sagorevanju frakciona disperzija. Ako je tačka ključanja zapaljive tekućine manja od točke ključanja vode (100°C), tada gorivo prvenstveno izgara, smjesa se obogaćuje vodom, brzina izgaranja se smanjuje i, konačno, izgaranje prestaje. Ako je točka ključanja tekućine veća od 100 ° C, tada, naprotiv, vlaga prvenstveno isparava i njena koncentracija se smanjuje. Kao rezultat, povećava se stopa sagorijevanja tekućine, sve do brzine sagorijevanja čistog proizvoda.
U pravilu, s povećanjem brzine vjetra, stopa izgaranja tekućine se povećava. Vjetar intenzivira proces miješanja goriva sa oksidantom, čime se podiže temperatura plamena (tabela 2.6) i približava plamen površini sagorijevanja.
Tabela 2.6
Utjecaj brzine vjetra na temperaturu plamena
Sve to povećava intenzitet toplotnog toka koji se dovodi do zagrijavanja i isparavanja tekućine, stoga dovodi do povećanja stope sagorijevanja. Pri većim brzinama vjetra plamen se može prekinuti, što će dovesti do prestanka sagorijevanja. Tako, na primjer, kada je traktorski kerozin izgorio u rezervoaru prečnika 3 m, došlo je do izbijanja plamena pri brzini vjetra od 22 m/s.
Većina tekućina ne može izgorjeti u atmosferi s manje od 15% kisika. Sa povećanjem koncentracije kiseonika iznad ove granice, brzina sagorevanja se povećava. U atmosferi znatno obogaćenoj kiseonikom, sagorevanje tečnosti se odvija uz oslobađanje velike količine čađi u plamenu, a primećuje se intenzivno ključanje tekuće faze. Za višekomponentne tečnosti (benzin, kerozin, itd.), površinska temperatura raste sa povećanjem sadržaja kiseonika u okolini.
Povećanje brzine izgaranja i temperature površine tekućine s povećanjem koncentracije kisika u atmosferi uzrokovano je povećanjem emisivnosti plamena kao rezultat povećanja temperature izgaranja i visokog sadržaja čađi u njoj. .
Brzina sagorijevanja također se značajno mijenja sa smanjenjem razine zapaljive tekućine u spremniku: brzina izgaranja se smanjuje, sve do prestanka sagorijevanja. Budući da je opskrba kisikom zraka iz okoline unutar rezervoara otežana, kada se nivo tekućine smanji, udaljenost h np između zone plamena i površine sagorevanja (slika 2.8). Smanjuje se fluks zračenja prema ogledalu tečnosti, a samim tim i brzina sagorevanja, sve do slabljenja. Kod sagorevanja tečnosti u rezervoarima velikog prečnika, granična dubina /g pr na kojoj je sagorevanje prigušeno je veoma velika. Dakle, za rezervoar prečnika 5 m, to je 11 m, a prečnika Im - oko 35 m.

Normalna brzina širenja plamena je brzina kretanja fronta plamena u odnosu na neizgoreli gas u pravcu okomitom na njegovu površinu.
Vrijednost normalne brzine širenja plamena treba koristiti za izračunavanje brzine porasta tlaka eksplozije mješavine plina i pare u zatvorenoj, nepropusnoj opremi i prostorijama, kritičnog (gašenja) promjera u razvoju i stvaranju plamena. odvodnici, područje lako padajućih konstrukcija, sigurnosne membrane i drugi uređaji za smanjenje pritiska; prilikom izrade mjera za osiguranje požarne i eksplozivne sigurnosti tehnoloških procesa u skladu sa zahtjevima GOST 12.1.004 i GOST 12.1.010.
Suština metode za određivanje normalne brzine širenja plamena je da se unutar reakcione posude pripremi zapaljiva mješavina poznatog sastava, da se smjesa zapali u centru tačkastim izvorom, zabilježi promjena tlaka u posudi s vremenom i obraditi eksperimentalnu ovisnost tlak-vrijeme korištenjem matematičkog modela procesa sagorijevanja plina u zatvorenoj posudi i optimizacijskih postupaka. Matematički model omogućava dobijanje izračunate zavisnosti „pritisak-vreme“, čija optimizacija prema sličnoj eksperimentalnoj zavisnosti rezultira promenom normalne brzine tokom razvoja eksplozije za određeni test.
Normalna brzina gorenja je brzina kojom se front plamena širi u odnosu na neizgorele reaktante. Brzina sagorevanja zavisi od brojnih fizičko-hemijskih svojstava reagensa, posebno od toplotne provodljivosti i brzine hemijske reakcije, i ima dobro definisanu vrednost za svako gorivo (u uslovima konstantnog sagorevanja). U tabeli. 1 pokazuje stope sagorevanja (i granice paljenja) nekih gasovitih smeša. Koncentracije goriva u mješavinama određivane su na 25°C i normalnom atmosferskom tlaku. Granice zapaljivosti, uz navedene izuzetke, dobivene su širenjem plamena u cijevi promjera 0,05 m zatvorenoj s obje strane. Koeficijenti viška goriva definirani su kao omjer zapreminskog sadržaja goriva u stvarnoj smjesi prema stehiometrijskoj smjesi (j1) i prema smjesi pri maksimalnoj brzini sagorijevanja (j2).
Tabela 1
Brzine sagorevanja kondenzovanih mešavina (anorganski oksidans + magnezijum)
| List |
| br. dokumenta |
| Potpis |
| datum |
| List |
| TGIV 20.05.01.070000.000 PZ |
Kao što se vidi, tokom sagorevanja vazdušnih gasnih smeša na atmosferskom pritisku u max leži unutar 0,40-0,55 m/s, a - unutar 0,3-0,6 kg/(m2-s). Samo za neke niskomolekularne nezasićene spojeve i vodonik u max leži unutar 0,8-3,0 m/s, a dostiže 1-2 kg/(m2s). Povećanjem i max ispitivana goriva u smjesama sa zrakom mogu biti
rasporediti u sljedeći red: benzin i tečna raketna goriva - parafini i aromati - ugljični monoksid - cikloheksan i ciklopropan - etilen - propilen oksid - etilen oksid - acetilen - vodonik.
| Promjena |
| List |
| br. dokumenta |
| Potpis |
| datum |
| List |
| TGIV 20.05.01.070000.000 PZ |
Linearna brzina izgaranja mješavina kisika je mnogo veća od mješavine zraka (za vodonik i ugljični monoksid - 2-3 puta, a za metan - više od reda veličine). Masovna brzina sagorijevanja ispitivanih smjesa kisika (osim smjese CO + O2) je u rasponu od 3,7–11,6 kg/(m2 s).
U tabeli. U tabeli 1 prikazane su (prema podacima N. A. Silina i D. I. Postovskog) brzine sagorevanja zbijenih mešavina nitrata i perhlorata sa magnezijumom. Za pripremu smeša korišćene su praškaste komponente sa veličinom čestica nitrata 150–250 μm, perhlorata 200–250 μm i magnezijuma 75–105 μm. Smjesa je punjena u kartonske ljuske promjera 24-46 mm do faktora zbijanja 0,86. Uzorci su spaljeni na vazduhu pri normalnom pritisku i početnoj temperaturi.
Iz poređenja podataka u tabeli. 1 i 1.25 proizilazi da su kondenzirane mješavine superiorne u odnosu na mješavine plinova u smislu mase i inferiorne u odnosu na njih u smislu linearne brzine gorenja. Brzina sagorevanja mešavina sa perhloratima je manja od brzine sagorevanja mešavina sa nitratima, a mešavine sa nitratima alkalnih metala gore sa višom brzinom od smeša sa nitratima zemnoalkalnih metala.
tabela 2
Granice zapaljivosti i brzine gorenja mješavina sa zrakom (I) i kiseonik (II) pri normalnom pritisku i sobnoj temperaturi
| List |
| br. dokumenta |
| Potpis |
| datum |
| List |
| TGIV 20.05.01.070000.000 PZ |
| Promjena |
Metode za izračunavanje brzine sagorevanja tečnosti
| Promjena |
| List |
| br. dokumenta |
| Potpis |
| datum |
| List |
| TGIV 20.05.01.070000.000 PZ |
![]() ; (16)
; (16)
gdje M je bezdimenzionalna stopa sagorevanja;
 ; (17)
; (17)
M F- molekulska težina tečnosti, kg mol -1;
d- karakteristična veličina ogledala goruće tečnosti, m. Određuje se kao kvadratni koren površine sagorevanja; ako područje sagorijevanja ima oblik kruga, tada je karakteristična veličina jednaka njegovom promjeru. Prilikom izračunavanja brzine turbulentnog sagorevanja može se uzeti d= 10 m;
T to je tačka ključanja tečnosti, K.
Procedura izračuna je sljedeća.
Način sagorijevanja određen je vrijednošću Galilejevog kriterija Ga, izračunato po formuli
gdje g- ubrzanje slobodnog pada, m·s -2 .
U zavisnosti od načina sagorevanja, izračunava se bezdimenzionalna stopa sagorevanja M. Za laminarni način sagorijevanja:
Za prolazni način sagorijevanja:
ako onda ![]() , (20)
, (20)
ako , onda , (21)
Za turbulentni režim sagorevanja:
; ![]() , (22)
, (22)
M0- molekulska težina kiseonika, kg mol -1;
n 0- stehiometrijski koeficijent kiseonika u reakciji sagorevanja;
n F- stehiometrijski koeficijent tečnosti u reakciji sagorevanja.
B- bezdimenzionalni parametar koji karakterizira intenzitet prijenosa mase, izračunat po formuli
![]() , (23)
, (23)
gdje Q- niža kalorijska vrijednost tečnosti, kJ·kg -1 ;
| Promjena |
| List |
| br. dokumenta |
| Potpis |
| datum |
| List |
| TGIV 20.05.01.070000.000 PZ |
c- izobarični toplotni kapacitet produkata sagorevanja (pretpostavlja se da je jednak toplotnom kapacitetu vazduha c = 1), kJ·kg -1 ·K -1 ;
T0- temperatura okoline, uzeta jednaka 293 K;
H- toplota isparavanja tečnosti na tački ključanja, kJ·kg -1;
c e je prosječni izobarični toplinski kapacitet tekućine u rasponu od T0 prije T to.
Ako su poznati kinematička viskoznost pare ili molekulska težina i tačka ključanja ispitivane tečnosti, tada se turbulentna brzina sagorevanja izračunava korišćenjem eksperimentalnih podataka po formuli
gdje m i- eksperimentalna vrijednost brzine sagorijevanja u prolaznom režimu sagorijevanja, kg·m -2 ·s -1 ;
d i- prečnik gorionika u kome se dobija vrednost m i, m. Preporučuje se korištenje baklje promjera 30 mm. Ako se u gorioniku prečnika 30 mm posmatra laminarni režim sagorevanja, treba koristiti gorionik većeg prečnika.
3. ŠIRENJE PLAMA U GASNIM SMEŠAMA
Brzina širenja plamena pri sagorevanju čvrstih, tečnih i gasovitih materija je od praktičnog interesa u smislu sprečavanja požara i eksplozija. Razmotrite brzinu širenja plamena u mješavinama zapaljivih plinova i para sa zrakom. Poznavajući ovu brzinu, moguće je odrediti sigurnu brzinu strujanja gasa i vazduha u cevovodu, rudniku, ventilacionoj instalaciji i drugim eksplozivnim sistemima.
3.1. FLAME SPEED
Kao primjer, na sl. 3.1 prikazuje dijagram izduvne ventilacije u rudniku uglja. Iz nanosa rudnika 1 kroz cjevovod 2 uklanja se prašnjava mješavina zraka i ugljene prašine, au nekim slučajevima i metan koji se oslobađa u ugljenim slojevima. Kada dođe do požara, front plamena 3 će se proširiti prema nanosima 1. Ako brzina zapaljive mješavinew bit će manja od brzine širenja fronta plamenai u odnosu na zidove cijevi, plamen će se proširiti u rudnik i dovesti do eksplozije. Stoga je za normalan rad ventilacijskog sistema potrebno pridržavati se uvjeta
w>u.
Brzina uklanjanja eksplozivne smjese mora biti veća od brzine širenja fronta plamena. Ovo će spriječiti da plamen uđe u nanose okna.
Rice. 3.1. Šema širenja plamena u rudniku:
1 - moj; 2 - cjevovod; 3 - prednji dio plamena
Teorija širenja plamena razvijena je u radovima Ya.B. Zeldovich i D.A. Frank-Kamenetsky, temelji se na jednadžbama provodljivosti topline, difuzije i kemijske kinetike. Paljenje zapaljive mješavine uvijek počinje u jednom trenutku i širi se po cijeloj zapremini koju zauzima zapaljiva smjesa. Razmotrimo jednodimenzionalni slučaj - cijev ispunjenu zapaljivom mješavinom (slika 3.2).
Ako se smjesa zapali s jednog kraja cijevi, tada će se duž cijevi širiti uski front plamena, odvajajući produkte sagorijevanja (iza prednjeg dijela plamena) od svježe zapaljive smjese. Prednja strana plamena ima oblik kape ili konusa čiji je konveksni dio okrenut prema kretanju plamena. Front plamena je tanak gasoviti sloj širine 10 -4 ÷10 -6 m. U ovom sloju, koji se naziva zona sagorevanja, odvijaju se hemijske reakcije sagorevanja. Temperatura fronta plamena, u zavisnosti od sastava smeše, je T= (1500 ÷ 3000) K. Oslobođena toplota sagorevanja troši se na zagrevanje proizvoda sagorevanja sveže zapaljive smeše i zidova cevi usled procesa provođenja toplote i zračenja.

Rice. 3.2. Šema širenja fronta plamena u cijevi
Kada se front plamena kreće u cijevi, u zapaljivoj smjesi nastaju valovi kompresije koji stvaraju vrtložna kretanja. Vrtlozi plina savijaju front plamena bez promjene njegove debljine i prirode procesa koji se u njemu odvijaju. Na jediničnoj površini fronta plamena uvijek gori ista količina tvari po jedinici vremena. ![]() . Vrijednost je konstantna za svaku zapaljivu smjesu i naziva se masena brzina gorenja .
Poznavanje površine fronta plamenaS, možete izračunati masu supstance M, zapaljiv na cijelom frontu sagorijevanja u jedinici vremena:
. Vrijednost je konstantna za svaku zapaljivu smjesu i naziva se masena brzina gorenja .
Poznavanje površine fronta plamenaS, možete izračunati masu supstance M, zapaljiv na cijelom frontu sagorijevanja u jedinici vremena:
Svaki element fronta plamena dSkreće se u odnosu na svježu smjesu uvijek u smjeru normale na front plamena u datoj tački (slika 3.2), a brzina tog kretanja:
gdje je gustina svježe zapaljive smjese.
Vrijednost naziva se normalnom brzinom širenja plamena i ima dimenziju m/s. To je konstantna vrijednost procesa sagorijevanja date smjese i ne ovisi o hidrodinamičkim uvjetima koji prate proces sagorijevanja. Normalna brzina širenja plamena je uvijek manja od uočene brzine i, odnosno brzina fronta sagorevanja u odnosu na zidove cevi:
u n< u .
Ako je front plamena ravna i usmjerena okomito na os cijevi, tada će u ovom slučaju promatrana i normalna brzina širenja plamena biti ista
u n = u .
Područje konveksnog fronta plamenaS issueuvijek veća od površine ravne fronteS pl, Zbog toga
> 1.
Normalna brzina plamenau nza svaku zapaljivu mešavinu zavisi od primesa inertnih gasova, temperature smeše, vlažnosti i drugih faktora. Konkretno, predgrijavanje zapaljivog plina povećava brzinu širenja plamena. Može se pokazati da je brzina širenja plamenau nproporcionalan je kvadratu apsolutne temperature smjese:
u n .= const T 2.
Na sl. 3.3 prikazana je ovisnost brzine širenja plamena u zapaljivoj smjesi "vazduh - ugljični monoksid" ovisno o koncentraciji CO. Kao što slijedi iz gornjih grafikona, brzina širenja plamena raste sa povećanjem temperature smjese. Za svaku temperaturnu vrijednost, brzina širenja plamena ima maksimum u području koncentracije ugljičnog monoksida CO od ~40%.
Toplotni kapacitet inertnog gasa utiče na brzinu širenja plamena. Što je veći toplinski kapacitet inertnog plina, to više smanjuje temperaturu izgaranja i više smanjuje brzinu širenja plamena. Dakle, ako se mješavina metana i zraka razrijedi ugljičnim dioksidom, tada se brzina širenja plamena može smanjiti za 2-3 puta. Na brzinu širenja plamena u mješavinama ugljičnog monoksida sa zrakom u velikoj mjeri utječu vlaga sadržana u smjesi, prisustvo čestica čađi i nečistoća inertnih plinova.

Rice. 3.3. Ovisnost brzine širenja plamena
na koncentraciju ugljičnog monoksida u smjesi
Raspodjela zone hemijskih transformacija u otvorenom zapaljivom sistemu
Sagorevanje počinje paljenjem zapaljive smeše u lokalnoj zapremini zapaljivog sistema, a zatim se širi u pravcu mešavine koja se kreće. Zona gorenja u kojoj se odvijaju redoks hemijske reakcije vidljive posmatraču naziva se plamen. Površina koja razdvaja plamen i mešavinu koja još ne gori služi kao prednja strana plamena. Priroda širenja plamena ovisi o mnogim procesima, ali proces zagrijavanja zapaljive smjese je odlučujući. U zavisnosti od načina zagrijavanja zapaljive smjese do temperature paljenja, razlikuju se normalno, turbulentno i detonacijsko širenje plamena.
Normalno širenje plamena se posmatra tokom sagorevanja u zapaljivom sistemu sa laminarnom pokretnom smešom. Tokom normalnog širenja plamena, toplotna energija se prenosi sa gorućeg sloja na hladni uglavnom toplotnom provodljivošću, kao i molekularnom difuzijom. Toplotna provodljivost u gasovima karakteriše nizak intenzitet, pa je brzina normalnog širenja plamena mala.
Pri turbulentnom kretanju zapaljive mješavine, prijenos toplinske energije sa gorućeg sloja na hladni odvija se uglavnom molarnom difuzijom, kao i toplotnom provodljivošću. Molarni prijenos je proporcionalan skali turbulencije, koja je određena brzinom smjese. Brzina širenja turbulentnog plamena zavisi od svojstava smeše i od gasne dinamike strujanja.
Širenje plamena u zapaljivoj mješavini iz zone sagorijevanja u hladne slojeve kroz molekularne i molarne procese naziva se deflagracija.
Fizički i hemijski procesi sagorevanja su praćeni povećanjem temperature i pritiska u plamenu. U zapaljivim sistemima, pod određenim uvjetima, mogu nastati zone visokog pritiska koje mogu komprimirati susjedne slojeve, zagrijavajući ih do stanja zapaljenja. Širenje plamena brzim sabijanjem hladne smjese do temperature paljenja naziva se detonacija i uvijek je eksplozivno.
U zapaljivim sistemima može doći do vibracionog sagorevanja, pri čemu se front plamena kreće brzinom koja varira i po veličini i po pravcu.
Brzina širenja fronta izgaranja u laminarno pokretnoj ili stacionarnoj smjesi naziva se normalna ili osnovna brzina širenja plamena. Numerička vrijednost normalne brzine određena je brzinom smjese koja se još nije zapalila, normalno usmjerene prema frontu sagorijevanja.
Vrijednost u n za ravnu frontu sagorijevanja može se odrediti iz uvjeta dinamičke ravnoteže između brzine zagrijavanja mješavine toplotnom provodljivošću do temperature paljenja i brzine kemijske reakcije. Rezultat je sljedeća formula
gde je l koeficijent toplotne provodljivosti gasne mešavine, sr koeficijent toplotnog kapaciteta smeše pri konstantnom pritisku, Tin je početna temperatura smeše, Ta je adijabatska temperatura sagorevanja, Arr je Arrheniusov kriterijum, k 0 je koeficijent Arrheniusovog zakona.
Normalna brzina se može eksperimentalno odrediti iz brzine fronta u cijevi sa stacionarnom smjesom ili iz visine konusa sagorijevanja u Bunsenovom plameniku. Bunsenov plamenik je laboratorijski plamenik s djelimičnim premiksom gasa i vazduha. Na izlazu iz gorionika formira se plamen sa frontom sagorevanja u obliku stošca pravilnog oblika (sl.).
Fig.7. Prednje sagorijevanje u Bunsenovom plameniku
Sa stabilnim položajem fronta sagorevanja, brzina širenja plamena u n je uravnotežena komponentom W n normalno na površinu konusa sagorevanja i brzinom mešavine gasa i vazduha W, tj.
gdje je j ugao između vektora brzine mješavine plina i zraka i vektora njene komponente normalne na površinu konusa sagorijevanja.
Vrijednost brzine kretanja mješavine plina i zraka na izlazu mlaznice sa konusom za sagorijevanje pravilnog oblika određena je formulom
gdje je d 0 prečnik mlaznice gorionika, V je brzina protoka mješavine plina i zraka kroz gorionik.
Vrijednost cos j može se izraziti u smislu visine konusa sagorijevanja
Uzimajući u obzir činjenicu da je površina izgaranja bočna površina pravilnog konusa
utvrđuje se vrijednost normalne brzine
Na vrijednost normalne brzine širenja plamena utiču:
1. Početna temperatura smjese. Na niskim temperaturama, u n je direktno proporcionalan kvadratu apsolutne temperature smjese koja ulazi u sagorijevanje. Na temperaturi iznad temperature paljenja, koncept normalne brzine gubi smisao, jer smjesa postaje sposobna za samozapaljenje.
2. Temperatura zidova kanala, pod uslovom da se plamen širi unutar ovog kanala. Hladni zidovi prekidaju lančane reakcije i usporavaju širenje plamena.
3. Prečnik kanala. Za svaku zapaljivu smjesu postoji kritična vrijednost prečnika d cr, počevši od koje je širenje plamena unutar kanala nemoguće. Vrijednost kritičnog prečnika može se odrediti formulom
gdje je a cm toplinska difuzivnost smjese.
4. Pritisak. Sa povećanjem pritiska, u n opada.
5. Sastav smjese. Za mješavinu sastava blizu stehiometrijskog, normalna brzina ima maksimalnu vrijednost. Osim toga, postoje donje i gornje granice u smislu koncentracije goriva, preko kojih se plamen ne može širiti.
Maziva
Glavni cilj u razvoju ekološki prihvatljivih maziva je stvaranje proizvoda visoke biorazgradljivosti i niske ekotoksičnosti. U razvijenim zemljama Zapada,
Trenutno, javne i privatne kompanije počinju stvarati tržište za ekološki prihvatljiva maziva. Većina studija je fokusirana na hemijski sastav proizvoda i procenu njegove biorazgradivosti. Prilikom stvaranja ekološki prihvatljivih maziva razmatraju se dva glavna područja: proizvodnja baznih ulja čija kemijska priroda određuje prirodu utjecaja na okoliš i sinteza novih aditiva koji su ekološki prihvatljivi, biorazgradivi i efikasni.
Trenutno, a vjerovatno i u budućnosti, od posebne su važnosti tri grupe baznih ulja dobivenih iz različitih izvora sirovina: hidrokrekovana naftna ulja (HA), polialfaolefini (PAO) i estri, koji su brzo biorazgradivi u okolišu. Od velike važnosti za neograničeno dugo razdoblje nesumnjivo će ostati bazna naftna ulja tradicionalnih shema toka, posebno uzimajući u obzir faktor koji maziva dobijaju na bazi PAO. estri polialkohola, polialkilen glikola i diestera koštaju 2-10 puta više od naftnih derivata. Povećana biorazgradivost nije poticaj za prevazilaženje razlika u cijenama.
Visoke performanse i ekološka prihvatljivost mineralnih ulja obezbeđuju se nizom određenih kvaliteta. Prije svega, to je njihov uski frakcijski i povoljan grupni kemijski sastav s minimalnom količinom sumpornih i dušičnih spojeva u baznim uljima. Izbor sirovina, sortiranje ulja koje se koriste u proizvodnji visokoindeksnih ulja i njihova odvojena prerada su od najveće važnosti. U dobijanju baznih mineralnih ulja koja zadovoljavaju ekološke zahteve, selektivno prečišćavanje igra važnu ulogu,
značajnu kancerogenost proizvoda. Trenutno se u SAD-u i Kanadi više od 70% baznih ulja dobiva selektivnom rafinacijom. Upotreba modernih procesa kao što su hidrokreking, hidrodeparatizacija, hidroizomerizacija otvara široke mogućnosti. Ove tehnologije su detaljno opisane u radu. Upotreba hidrokatalitičkih procesa u kombinaciji s tradicionalnim metodama rafiniranja naftnih sirovina selektivnim otapalima poboljšava performanse i ekološka svojstva baznih ulja.
U tabeli. U tabeli 1.4 prikazani su uporedni podaci o kemijskom sastavu baznih ulja dobivenih selektivnim rafiniranjem i hidroobradom. Ovo posljednje značajno smanjuje sadržaj arena, sumpora i dušika u uljima.
Tabela 14
Utjecaj hidrotretiranja na hemijski sastav
bazna ulja
Uvođenje procesa hidrokrekinga i hidroizomerizacije u proizvodnju baznih mineralnih ulja omogućava dobijanje proizvoda povećane biorazgradljivosti i bez arena. Ulja za hidrokreking, prema rezultatima dobivenim korištenjem savremenih metoda ispitivanja, nisu toksična, praktično odsustvo arena u njima ukazuje na vrlo nisku kancerogenost i neznatnu vjerojatnost njegovog rasta kroz stvaranje i akumulaciju policikličkih arena tijekom rada; odsustvo arena i prevlast
Davanje izoparafina obezbeđuje prilično visoku biorazgradljivost.
Hidrokrekirana bazna ulja proizvode se u SAD od kraja 1996. godine. . Za puštanje u rad pripremljena je instalacija u Finskoj.
U Rusiji, VNIINP, zajedno sa naučnim i inženjerskim centrom OAO LUKOIL i AO LUKOIL - Volgogradneftepererabotka, provode istraživački rad na organizovanju proizvodnje niza deficitarnih ulja i baza korišćenjem tehnologija hidrogenacije, posebno avionskog ulja MS-8 i vazduhoplovna hidraulična tečnost AMG -ten.
U poređenju sa mineralnim uljima, sintetička ulja u nekim slučajevima imaju bolje ekološke karakteristike. Najvažnije klase sintetičkih ulja u pogledu ekološke sigurnosti su ulja proizvedena na bazi sintetičkih estera, polialfao-lefina i polibutena. Netoksični su, nisu kancerogeni, karakteriziraju niska emisija štetnih tvari.
Sintetička ulja na bazi estera sa aditivima se široko koriste u gasnoturbinskim motorima civilnih i vojnih aviona od 1960-ih godina. U CIAM-u, zajedno sa VNIINP i 25. državnim istraživačkim institutom Ministarstva odbrane Ruske Federacije, u toku je rad na stvaranju visoko termički stabilnog (do 240 ° C) estarskog ulja koristeći efikasne kompozicije aditiva koji nisu inferiorni u kvaliteti. do najboljih stranih ulja. Analiza naučnih, tehničkih i patentnih informacija o uljima za vazduhoplovne gasnoturbinske motore pokazuje da poliol estri ostaju glavna klasa jedinjenja koja se koriste kao bazne materije [PO]. Međutim, situacija se mijenja sa sljedećom generacijom avionskih motora, jer poboljšanja dizajna i potreba za smanjenjem potrošnje goriva dovode do povećanja pritiska, temperature i opterećenja ulja.
Ovo posljednje doprinosi opasnosti od lokalnih ugljičnih formacija. Stoga je za vojno zrakoplovstvo u budućnosti potrebno odustati od upotrebe ulja na bazi estera. U tu svrhu najviše obećavaju ulja novog tipa - na bazi jednostavnih perfluoroalkilpolietera. Prema savremenim podacima, ova jedinjenja su netoksična i čak se koriste u inostranstvu u parfimeriji i za konzervaciju mermernih spomenika umetnosti i arhitekture.
Aditivi imaju veliki uticaj na ekološka svojstva maziva. U avio-uljima se kao aditivi široko koriste tradicionalni antioksidansi i inhibitori korozije kao što su dioktildifenilamin, fenil-p-naftilamin, benzotriazol, aditiv K-51 sukcinimidnog tipa i drugi koji su se dokazali.
U cijelom svijetu se već dugo radi na stvaranju novih netoksičnih i biorazgradivih proizvoda. Konkretno, od 90-ih godina razvijene su zamjene za aditive koji sadrže klor. Važno pitanje je zamjena jedinjenja olova. Zamjene za olovo su jedinjenja bizmuta. Počeo je razvoj bizmutditiokarbamatnog aditiva.
Aditivi kao što su Mif-1 (aditiv benzenskog tipa složenog sastava), Irganox L-57 (antioksidativni aditiv iz Sibe, oktilirani i butilirani difenilamin), aditiv X (jedinjenje koje sadrži fluor sa funkcionalnim grupama oksisulfita i hidroksikarbamata) i drugi imaju razvijeno.
Poboljšana su svojstva poznatih aditiva. Tako je u trikrezil fosfatu sadržaj neutrotoksičnog ortoizomera smanjen na 3% (Rusija), a u SAD se proizvodi trikrezil fosfat koji ne sadrži ortoizomer.
Opasnost od požara i eksplozije avna goriva i maziva
Trenutno korišćena avio goriva i maziva su zapaljivi proizvodi. U pogledu požara, gasovita goriva su posebno opasna. Ugljovodonična goriva (mlazna goriva, benzini, itd.) su zapaljive tečnosti (zapaljive tečnosti). Odlikuje ih visoka proizvodnja toplote (-2000°C) i isparljivost, lako stvaraju zapaljive smjese sa zrakom, koje pri sagorijevanju stvaraju veliku količinu produkata izgaranja (veliki stehiometrijski koeficijent), koji su dobri dielektrici i, stoga, mogu akumulirati naboje statičkog elektriciteta.
Prema opasnosti od požara, zapaljive tečnosti se dele u tri kategorije. Tačka paljenja se koristi kao određujući indikator (određuje se prema GOST 12.1.044-89):
Ovisno o temperaturi samozapaljenja (određenoj prema GOST 12.1.044-89), ugljikovodična goriva pripadaju jednoj ili drugoj grupi eksplozivne mješavine para sa zrakom:
Usuđujemo se da pare ugljovodoničnih goriva sa vazduhom pripadaju kategoriji TTA eksploziva: određuje se prema GOST 12.1.011-78. Ovaj indikator se koristi pri odabiru vrste električne opreme otporne na eksploziju i pri dizajniranju aparata za gašenje požara.
Zapaljiva svojstva goriva određuju se i graničnom koncentracijom paljenja (CIL) - minimalnim i maksimalnim sadržajem para goriva u mješavini sa zrakom (oksidator), pri kojem je širenje plamena kroz smjesu moguće na bilo kojoj udaljenosti od mjesta paljenja. izvor (GOST 12.1.044-89). Važna karakteristika goriva su granice temperature paljenja - temperature na kojima su zasićene pare goriva u zraku u koncentracijama jednakim donjem, odnosno gornjem CPV-u. Od velike važnosti je minimalna energija električnog pražnjenja potrebna za paljenje mješavine para i zraka.
Prilikom procjene opasnosti od požara pri rukovanju gorivima utvrđuje se i stopa sagorijevanja - količina goriva koja sagorijeva u jedinici vremena sa površine jedinice; minimalna energija paljenja - kako bi se osigurala elektrostatička sigurnost varnica. Procjenjuje se interakcija gorućeg goriva sa sredstvima za gašenje vodene pjene (prema GOST 12.1.044-89).
Požaru često prethodi eksplozija mešavine gasa i vazduha. Eksplozijom zračnih mješavina u cijevima velikog promjera i dužine može doći do detonacijskog sagorijevanja koje se širi brzinom od 1100-1400 m/s. U tom slučaju pritisak može porasti do 0,8 MPa ili više. Udarni val velike brzine uzrokuje nagli porast tlaka, temperature i gustoće zapaljive smjese, što zauzvrat ubrzava kemijske reakcije izgaranja i pojačava destruktivni učinak.
Eksplozivne koncentracije isparenja goriva sa vazduhom mogu se formirati u širokom rasponu temperatura, a posebno u zatvorenim prostorima i kontejnerima. Priroda i sadržaj mjera opreza uređuju se posebnim resornim uputstvima. Suština mjera opreza je spriječiti pojavu izvora grijanja na mjestima gdje se stvaraju eksplozivne smjese, posebno izvora otvorene vatre. Jedan od najopasnijih izvora otvorene vatre je pražnjenje elektrostatičkih potencijala kroz parno-vazdušni medij i stvaranje iskre pri udaru čvrstih tijela. Pojava visokih električnih potencijala u gorivu objašnjava se njegovim elektrofizičkim svojstvima. Mogu se okarakterizirati sposobnošću akumuliranja naboja u volumenu (elektrolitičnost) i svojstva opuštanja naboja (električna žica do njih).
U tabeli. 1.5. dati su indikatori koji karakterišu požarno opasna svojstva avio goriva.
Tabela 1.5
Zapaljiva svojstva avio goriva
1 Izračunato aditivnošću.
^ Izračunato prema jednadžbi (47) i (48) GOST 12.1.044-89 na osnovu početne tačke ključanja od -10/-4°C.
° U brojiocu - u zatvorenom lončiću, u nazivniku - u otvorenom. a „Granice širenja plamena prema GOST 10277-89.
Normalna brzina plamena
Brzina širenja plamena u zapaljivoj smeši zavisi od uslova za njeno određivanje i brojanje. Za uporednu procjenu goriva prema ovoj karakteristici usvojena je normalna brzina širenja plamena - to je linearna brzina kretanja zone sagorijevanja u odnosu na svježu homogenu zapaljivu smjesu u smjeru normalnom na front plamena. Brzina širenja plamena u takvim uslovima za dati sastav zapaljive smeše može se smatrati fizičko-hemijskom karakteristikom koja zavisi samo od pritiska i temperature.
Eksperimentalno, normalna brzina širenja plamena određena je prema GOST 12.1.044-89.
Pri temperaturi od 20 °C i pritisku od 0,101 MPa u mješavinama ugljovodonik-vodonik-vazduh, maksimalna brzina u se postiže pri koncentraciji goriva u mješavini od C ^ ~ 1,15 C st x (slika 1.24), tj.
sa a - 0,87 i sa brojem atoma ugljika u ugljovodoniku n\u003e 7, to je -39-40 cm / s (slika 1.25). Minimalna normalna brzina širenja plamena i brzina masenog sagorevanja postignuta na granicama koncentracije širenja plamena u normalnim uslovima su 4–6 cm/s i (5–7) 10° g/(cm 2 s) respektivno.
U nedostatku eksperimentalnih podataka, normalnu brzinu širenja plamena treba odabrati interpolacijom iz vrijednosti u za mješavine sa sličnim fizičko-hemijskim svojstvima ili treba koristiti empirijske jednadžbe. Jednostavne i pogodne jednačine predložio je A.S. Prije vožnje:
- (1.3)
t \u003d t p + B (St-C ^ (C u -C t),
gdje je u brzina širenja u cm/s; m je masa izgaranja smjese, g/(cm 2 s); i 11P, tn - granične (minimalne) vrijednosti brzine širenja plamena; S„ i C n su koncentracija goriva u smjesi na donjoj i gornjoj koncentracijskoj granici širenja plamena; A i B su koeficijenti određeni iz jedne eksperimentalne točke.

Rice. 1.24.
širenje plamena ovisno o molarnom stehiometrijskom koeficijentu viška zraka bm:
- - parafin; * - olefinski; ° - acetilen; D - ulje; © - dipolarni; ° ugljovodonici sa C p 11 2 „ ciklusima
- 1 2 3 4 5 b 7 str

Rice. 1.25. Maksimalna normalna brzina širenja plamena u mješavini goriva i zraka u zavisnosti od broja atoma ugljika u molekuli ugljovodonika (P=0,101 MPa, 1=20°C, otvorena staklena cijev: dužina 57 cm, prečnik 2,5 cm): - parafin; * - olefinski;
° - acetilen; D - naftenski; in - dnolsfipovye; o ciklički (C P P2 ");
1 - benzin [ 116]; 2 - benzen
Funkcionalni odnos između brzine širenja plamena i koncentracije goriva C t na C t C * t (ali dat EMIN-om) može se predstaviti jednadžbom:
- - = 11 str
/ s r -s; l
"s t -s "t"
gdje je m i i n- normalna brzina širenja plamena
pri koncentracijama goriva u smjesi C t i C*t, cm/s; i pp- također,
na donjoj granici koncentracije širenja plamena, cm/s.
Približan tok krivulje i n - /(C t) u mešavini kompleksa
kompozicija se može graditi na tri referentne tačke koje odgovaraju donjoj i gornjoj granici koncentracije i maksimalnoj brzini širenja plamena. Za ove tačke moraju biti poznate koncentracije goriva i brzine širenja plamena.
Vrijednosti C t i i i za navedene bodove se računaju
sljedećom metodom. Svaka složena mješavina zapaljivih plinova je predstavljena kao sastavljena od odgovarajućeg broja jednostavnih mješavina. Proračun sastava na granicama koncentracije i na tački maksimalnih brzina vrši se prema pravilu miješanja, na osnovu granica koncentracije i sastava "maksimalnih smjesa". Odgovarajuća računska jednačina ima oblik:
C] + C* 2 + Su uh...
- -ja---g...
- (1.5)
gdje b- koncentracija goriva na CPRP ili u mješavini sa maksimalnom brzinom širenja plamena, % (vol.); C, C 2, C 3, ... - koncentracija jednostavnih gasova u složenoj smeši,
(s, + C 2 + C 3 + ... = 100%); b|, b 2 , b 3> ... - koncentracija gasova u jednostavnim smešama na KPRP ili u smešama sa i i, % (vol.).
Vrijednost maksimalne normalne brzine širenja plamena u smjesi izračunava se jednadžbom;
C, r/, + C2u2 + C3u3 +
C, + C 2 + c 3 4-...
- (1.6)
gdje je C*, C 2 , C 3 - sadržaj jednostavnih smjesa u složenoj smjesi sa maksimalnom brzinom širenja plamena, % (vol.); i*, i 2 , i 3 su maksimalne brzine širenja plamena u jednostavnim smjesama, cm/s.
Za izračunavanje drugih tačaka krivulje i i= /(C; .) treba postaviti nekoliko proizvoljnih vrijednosti brzine plamena, pronaći koncentraciju b u složenoj smjesi prema jednačini (1.5), u kojoj su C, C 2 , C 3 date sastavom smjesu.
Ova metoda proračuna je primjenjiva na mješavine plinova srodne prirode (npr. metan-propan). Ova tehnika nije primjenjiva na mješavinu S P N W sa H3 i CO.
Brzina izgaranja mase je direktno proporcionalna apsolutnoj temperaturi predgrijavanja smjese i može se izračunati iz jednadžbe:

gdje je w, zatim i t „ R eo- masena brzina sagorevanja smeše na temperaturi T, To i T P r e d, odnosno g/(cm -s).
Ako T»T pr e D, onda

Zavisnost maksimalne normalne brzine širenja plamena od temperature i pritiska približno je opisana jednadžbom:
i' =u1(T/273) 2 ?(/’/10 5)", (19)
gdje je u'o maksimalna normalna brzina širenja plamena na temperaturi od 293 K i pritisku od 0,101 MPa, cm/s; T je temperatura l plamena, u K; P - pritisak, u Pa; p - eksponent, ns u zavisnosti od pritiska u opsegu MO 4 + 5-10 5 Pa; za mješavinu zraka i goriva n = -0,3 -*? -0,4; za mješavine ugljovodonika i kiseonika P = -0,1 -5-0.
Maksimalna normalna brzina širenja plamena kao funkcija koncentracije kisika u oksidantu P R P Wu P
giil = \%ig" 0 + B-
gdje je G „Ja! Ali - na y, str y^ 0 , cm 2 /s; B - koeficijent određen iz eksperimentalnih podataka (za propan B ~ 0,22); u/ t- izuzetno niska koncentracija kiseonika u oksidantu.
Vrijednost u*n pri različitim koncentracijama kisika u oksidantu 1 //"P kada se temperatura predgrijavanja smjese promijeni sa 310 na 422 K, to se može odrediti jednadžbom:
":=at; (u,-s), (MO
gdje je u*n - u cm/s; T - u K; A, S ip - nalaze se prema eksperimentalnim podacima, njihove vrijednosti za propan, izooktan i etilen su date u nastavku:
Granice koncentracije i temperature širenja plamena
Granice koncentracije širenja plamena (KPRP) u zapaljivoj mješavini su granične minimalne i maksimalne koncentracije goriva u smjesi pri kojima je širenje plamena još uvijek moguće (donja i gornja granica). One zavise od hemijske aktivnosti goriva, koncentracije oksidatora i inertnih nečistoća, toplotne provodljivosti i toplotnog kapaciteta smeše, temperature i pritiska. KPPR za suspenzijska goriva, na osnovu njihovih fizičkih i hemijskih svojstava, određuju se disperzionim medijumom. Određivanje KPRP-a za homogene zapaljive mješavine vrši se prema GOST 12.1.044-89: prema tački 4.11 eksperimentalno i prema tački 4.12 - proračunom.
Prema GOST 12.1.044-84, granice koncentracije širenja plamena su definisane kao

gdje je Cn (i) - donji (gornji) CPRP,% (vol.); R- stehiometrijski koeficijent (broj molova kiseonika po molu goriva); a i b- univerzalne konstante, njihove vrijednosti su date u nastavku:
Za goriva C P N W
P \u003d n + t / 4.
Greška u proračunu: za donju granicu 0,12; za gornjih 0,40 at (3 p > 7.5. Podaci o KIRP-u u zavisnosti od R(% vol.) date su u tabeli. 1.6 (GOST 12.1.044-84).
Tabela 1.6
Koncentracione granice širenja plamena (donje i gornje) para i gasova u vazduhu
Postoje i druge jednadžbe za izračunavanje CPRP-a, i to:
- 4.76-(N-1) + ! '
- (1.14)
- 4.76/Y +4'
- (1.15)
gdje je S„ i Od do - u oko.); N je broj atoma kisika potrebnih za potpunu oksidaciju goriva.
Za gorivo S„N t
- (1.17)
- 3,74 10 5
gdje je Cn - u % (vol.); () n je najniža molarna kalorijska vrijednost, kJ/kmol.
Za ugljovodonična goriva SpN t na 3 p 10, greška proračuna je ±15%.
Ako je poznat KRI za pojedinačne komponente goriva, onda se preporučuje da se njegov niži KRI izračuna pomoću jednadžbe:
gdje su C i Cn koncentracije 1. komponente u smjesi i na donjoj granici, % (vol.).
Za C p N t goriva u prvoj aproksimaciji a k ~ a p - 1.42. Preračunavanje, i od u do a n i a n proizvedeno:

gdje je Cn (d) koncentracija goriva na donjem (gornjem)
KPRP, % (vol.); Mt i Mo su molekulska težina goriva i oksidatora; Bo - u kg oksidatora/kg goriva; bm je molarni stehiometrijski koeficijent, mol goriva/mol goriva.
Ponovno izračunavanje donjeg KPPR-a za različite temperature može se izvršiti prema jednadžbi:
L II l
T - 293
gde je Tn temperatura (u K) produkta sagorevanja smeše u kojoj koncentracija goriva na 293 K odgovara nižoj KPP (u prvoj aproksimaciji, Tn za mešavinu ugljovodonika i vazduha je 1600-1650 K); C „ i C „ - koncentracije goriva koje odgovaraju donjoj granici koncentracije na temperaturama T i 293 K, % (oko.).
Jednačina (1.20) vrijedi za širok raspon temperatura, ali se ne može koristiti na temperaturama bliskim temperaturi samozapaljenja.
Temperatura produkata sagorevanja na nižoj KPRP se takođe može izračunati pomoću jednačine
- (A. + 1) -s_s
- (1.21)
steh
gdje je Tn u K; T sa temperaturom smjese prije sagorijevanja, K; Sstsh - koncentracija goriva u mješavini stehiometrijskog sastava, % (vol.);
Srš je srednji izobarični toplotni kapacitet produkata sagorevanja na temperaturi T, „ kJ / (kg ° C).
CRP je praktično nezavisan od dimenzija cilindrične reakcione posude ako je njen prečnik veći od 50 mm, a za sferni, ako je zapremina veća od 2000 cm 3 .
Za određivanje KPPR-a i optimalnog sastava mješavine ugljovodonika i zraka, grafici prikazani na sl. 1.26.
S„,s,%(ov.)

Rice. 1.26. Granice koncentracije širenja plamena u mješavinama ugljovodonika i zraka (Cb i C") i koncentracije ugljovodonika u mješavinama stehiometrijskog sastava (Cc, ") ovisno o molarnom stehiometrijskom koeficijentu 1^ m pri H20 °C P = 0,101 MPa:
- - parafin; a - olefin;
- ? - naftenski; ? - aromatično
Zapaljive mješavine para goriva sa zrakom u prostoru iznad goriva mogu se formirati samo u određenom temperaturnom rasponu. Minimalna temperatura na kojoj se zapaljiva smjesa sposobna za stacionarno sagorijevanje kada se zapali iz vanjskog izvora još uvijek može formirati u zatvorenom volumenu prostora za prekomjerno gorivo naziva se donja granica temperature; odgovara donjem KPP. Najviša temperatura pri kojoj mješavina para sa zrakom u prostoru iznad goriva i dalje zadržava sposobnost stacionarnog sagorijevanja naziva se gornja temperaturna granica; odgovara gornjoj KPRP Eksperimentalno određivanje temperaturnih granica za formiranje eksplozivnih smeša vrši se u skladu sa GOST 12.1.044-89 (str. 4.12), izračunato - prema primeni istog standarda.
Temperatura na kojoj se postiže donja temperaturna granica za stvaranje eksplozivne smjese pri atmosferskom tlaku obično se poistovjećuje sa tačkom paljenja. Na tački paljenja gori samo nastala mješavina para i zraka, ali se proces sagorijevanja ne stabilizira.
Proračun temperaturnih granica za stvaranje zapaljivih smjesa svodi se na sljedeće operacije. U početku, pri datom ukupnom pritisku P i poznatim vrijednostima koeficijenta viška oksidatora (vazduha) koji odgovaraju donjem i gornjem KPRP-u (a n i a c), prema jednačini (1.22) odrediti
parcijalni pritisci para goriva R t :
X | 0,232 o? 0 M t " ?« -
gdje je P ukupni pritisak, Pa; C - stehiometrijski koeficijent, kg oksidatora/kg goriva; a - faktor viška oksidansa; Mt je masa mola goriva, kg/kmol; Mo je masa mola oksidacijskog sredstva, za zrak Mo = 28,966 kg/kmol; at/ 0 - masena koncentracija kisika u oksidansu.

Rice. 1.27.
Zatim, prema tabelama ili grafikonima, Pc.p. = ^ (0 (gdje je P, pritisak zasićenih para goriva) pronađite temperature koje odgovaraju izračunatim vrijednostima Pt-
Ako su granice koncentracije za stvaranje zapaljivih smjesa nepoznate, tada se granice temperature mogu približno izračunati pomoću jednadžbe:
1,15 1*(7,5 R d) - 0,239 3,31
gde je I - na 0 C; 15% - tačka ključanja 5% frakcije, 0 C; Rt - pritisak para goriva na KPP (R„ ili R„), kPa; 8 „ sa „ - entropija isparavanja pri temperaturi od 15% i atmosferskom pritisku (preuzeto prema grafikonu na slici 1.28).

Rice. 1.28.
60 80 100 120 140 160 180 1,°S
Zapaljiva energija i granice koncentracije zapaljive
Zapaljivost homogene zapaljive mješavine vanjskim izvorom topline karakteriziraju granice koncentracije i energija potrebna za njeno paljenje.
Granice koncentracijskog paljenja (CFL) su takve granične koncentracije goriva u mješavini pri kojima lokalni izvor paljenja (električno pražnjenje, zagrijano tijelo, plamen) može osigurati širenje procesa izgaranja na cijelu zapreminu smjese. Po analogiji sa KG1RP, razlikuju se donji i gornji CPV. One zavise od fizičko-hemijskih svojstava goriva i oksidatora, energije i vrste izvora paljenja, njegove lokacije itd.
Prema Ya.B. Zeldovich, energija potrebna za paljenje homogene zapaljive smjese određena je:
R1-T sa r (T 2 -T c)
gdje su pc i T c gustina i temperatura smjese; T g je temperatura produkata sagorevanja u početnoj komori za sagorevanje; L 7 - koeficijent toplotne provodljivosti produkata sagorevanja na Tg; u - normalna brzina širenja plamena; C rt - srednji
maseni izobarični toplotni kapacitet gasa u sfernom sloju 8 T koji okružuje sfernu početnu komoru za sagorevanje; 5, - termička širina fronta plamena.
Jednačina (1.24) je primjenjiva i za slučaj paljenja pokretne smjese, ako je koeficijent toplotne provodljivosti L 7 biti zamijenjen koeficijentom turbulentne razmjene IV/"(/ - skala
turbulencija, V/*- pulsirajuća brzina), i vrijednost n - brzina širenja plamena u turbulentnom strujanju.
Sastav smjese odgovara minimumu krivulje O = KS,), naziva se optimalnim. Za normalne parafinske ugljikovodike, koncentracija goriva u mješavini optimalnog sastava na 25°C može se odrediti iz omjera:
- 1 - metan; 2 - etan; 3 - propan;
- 4 - n-butan; 5 - n-heksan; 6 - n-heptan;
- 7 - ciklopropan: 8 - dietil etar;
- 9 - benzen
Sa povećanjem koncentracije kisika u oksidantu, optimalni sastav zapaljive smjese se pomiče u područje niže koncentracije goriva.
Ovisnost optimalne (minimalne) energije paljenja od pritiska i temperature zapaljive smjese opisana je jednadžbom [114]:
O-opt


gdje je Oopt energija paljenja na P i T, J; Cb - energija paljenja pri T = 273 K i P = 10 5 Pa.
Jednačina (1.26) ima dobru korelaciju sa eksperimentalnim podacima.
Odnos između optimalne energije paljenja i koncentracije kisika u oksidantu opisan je jednadžbom

gdje je (S? 0 „„,) y / = / - optimalna vrijednost energije paljenja smjese goriva i kisika; ~ zapreminska koncentracija
kiseonik u oksidantu; n je eksponent, on je blizu jedinice (n ~ 0,8).
Eksperimentalni podaci za metan, etan i propan prilikom izmjene c/ x, od 0,1 do 0,21 i pritisci od 0,98 do 19,6 kPa potvrđuju jednačinu (1.27). Očigledno, ona ostaje važeća za mješavine ugljovodonika.
Koncentracije goriva na granicama paljenja mogu se izračunati ako su KPRP i vrijednosti () ref i C opt poznate prema jednadžbama

o.5 (s; + s;) \u003d C_ + 0,15 (C. (1,29)
Jednačine (1.28) i (1.29) vrijede za --
Označavajući prave dijelove ovih jednačina, respektivno, B i 0.5A, dobijamo
SA" - SA" = B i C"+ C" = ALI . (1.30)
C" = 0,5 (L-B) i C; =0,5 (A + B). (1.31)
U gornjim jednačinama: C in i C n - koncentracije goriva u smjesi na gornjem i donjem KPRP; C in i C" - koncentracija goriva u smjesi na gornjoj i donjoj CPV sa energijom paljenja kapacitivnog električnog naboja; C opt - koncentracija goriva u smjesi koja odgovara O ref.
Jednačine (1.28) i (1.29) su zasnovane na rezultatima eksperimentalnih studija prikazanih na sl. 1.30.
- (s;-s>;)-2s opt

Rice. 1.30. Područje paljenja smjese C p N P1 + 02 + ^ ovisno o energiji paljenja
Granice koncentracije paljenja zavise od brzine protoka, približavajući se jedna drugoj sa povećanjem (sl. 1.31 i 1.32).
Utjecaj brzine strujanja na energiju paljenja ispravno je opisan jednadžbom:
(2 = (?o + Au "do (1,32))
gdje je (Zo - energija paljenja stacionarne smjese, 10 "3 J; XV - brzina protoka, m / s; A - koeficijent utvrđen eksperimentalno.

Rice. 1.31.

Rice. 1.32. Koeficijent viška zraka a na CPV mješavine benzina i zraka u zavisnosti od brzine protoka? i pritisak R [ 114]:
Tačka paljenja i temperatura samopaljenja
Tačka paljenja je minimalna temperatura na kojoj se nastala mješavina para i zraka može zapaliti vanjskim izvorom topline, ali proces sagorijevanja nije stabiliziran. Eksperimentalno, tačka paljenja se određuje u otvorenom ili zatvorenom lončiću prema GOST 12.1.044-84 (tačke 4.3 i 4.4). Izračunato određivanje tačke paljenja vrši se u skladu sa GOST 12.1.044.84 (tačka 4.5).
Tačka paljenja je 10-15°C ispod temperaturne granice za formiranje zapaljive mješavine sposobne za širenje plamena.
Za približno određivanje tačke paljenja može se koristiti zavisnost prikazana na slici 1. 1.33.

Rice. 1.33. Tačka paljenja 1 V cp mlaznog goriva i benzina B-70 u zavisnosti od pritiska zasićene pare Pn p na 1=40°C u zatvorenom lončiću (62]: o - goriva različitog sastava; - generalizujuća kriva
Samozapaljenje je proces paljenja zapaljive smjese bez kontakta s plamenom ili vrućim tijelom. Minimalna početna temperatura dovoljna za samozapaljenje zapaljive mješavine naziva se temperatura samozapaljenja. Zavisi od hemijske prirode goriva, sastava mešavine vazduh-gorivo, pritiska, adijabatske prirode procesa samozapaljenja, prisustva katalizatora i inhibitora oksidacije i drugih faktora.
Vremenski interval između trenutka kada zapaljiva smjesa dostigne temperaturu samozapaljenja i pojave plamena naziva se period odgode samozapaljenja. Prilikom snabdijevanja tečnim gorivom pokriva proces atomizacije, zagrijavanja i isparavanja kapljica goriva, difuziju isparenja goriva i kisika i, konačno, kemijske reakcije.
Temperatura i period kašnjenja samopaljenja su međusobno povezani relacijom:

gdje E- efektivna energija aktivacije, kJ/kmol; E\u003d 8,31419 kJ / (kmol K) - univerzalna plinska konstanta; t- period kašnjenja samozapaljenja na temperaturi T.
Sklonost ugljovodonika i njihovih smeša ka samozapaljenju karakteriše minimalna temperatura samozapaljenja dobijena u adijabatskim uslovima, kada vreme izlaganja zapaljive smeše pod datim početnim uslovima ne ograničava proces samozapaljenja.
Minimalna temperatura samozapaljenja je jedinstveno određena strukturom molekula. Tako, na primjer, za parafinske ugljovodonike, 1 st je u direktnoj vezi sa efektivnom dužinom ugljikovog lanca Lc, koja se izračunava jednadžbom:
- 21>GLG,
- (1.34)
gdje je r broj CH 3 grupa u molekulu; k je broj ugljikovih lanaca koji počinju i završavaju grupom CH3, m* je broj mogućih lanaca koji sadrže b^-atome ugljika. Zavisnost 1 sv =A(bc) prikazana je na sl. 1.34.

Rice. 1.34.
- 1 - CH 4; 2 - C 2 H 6; 3 - C 3 H "; 10 - n - C 4 H 10; 11 - n - C 5 H 12;
- 14 - n - S L N M; 15 - n - C7H16; 16 - n - SkNsch; 17 - n - SdN 2 o;
- 18 - n - C| 0 H 22; 19 - n - C, 2 H 2I; 21 - n - C14H30; 22 - n - C|^H 3 4
Temperatura samozapaljenja mješavine ugljovodonika ne poštuje pravilo aditivnosti, obično je niža od izračunate na osnovu ovog pravila.
Podaci o temperaturi samozapaljenja mješavine zraka i goriva optimalnog sastava u zavisnosti od broja atoma ugljika u molekuli ugljovodonika (za mlazna goriva u gornjoj formuli) prikazani su na slici 2. 1.35. Utjecaj tlaka i koncentracije kisika u oksidantu ilustruju podaci prikazani na sl. 1.36.

Rice. 1.35. Zavisnost temperature samopaljenja mješavine zraka i goriva optimalnog sastava od broja atoma ugljikovodika n u molekulu na R=0,101 MPa [124]; t je period odgode samozapaljenja; t L - "oko; R.T. - mlazna goriva (p-u gornjoj formuli) - parafin; a- olefin; ? - naftenski ugljovodonici

Rice. 1.36. Ovisnost temperature samozapaljenja goriva T-6 o tlaku P i koncentraciji kisika u oksidantu f 0 2 (prema V.V. Malyshevu):
2 = 0 2/(°2+L, d)
Temperatura samozapaljenja određena je sposobnošću goriva da formira zapaljive smjese u parnoj fazi. Iz ovoga slijedi da je temperatura samozapaljenja suspenzije
goriva određuje disperzioni medij i zgušnjivač. Disperzovana faza učestvuje u procesu samozapaljenja samo u smislu apsorpcije toplote kada se suspenzija zagreje do temperature samozapaljenja tečne faze.
Eksplozijski pritisak u zatvorenoj zapremini
Eksplozijski pritisak - najviši pritisak koji se javlja tokom deflagracione eksplozije mešavine pare i vazduha u zatvorenoj zapremini pri početnom pritisku od 0,101 MPa. Brzina povećanja pritiska tokom eksplozije je derivat pritiska eksplozije u odnosu na vreme (s1R/(1t) na uzlaznom dijelu zavisnosti P=Y t).
Eksperimentalno, maksimalni pritisak eksplozije i brzina povećanja pritiska tokom eksplozije mešavine pare i vazduha određuju se prema GOST 12.1.044-89 (Dodatak 8). Proračunato određivanje brzine povećanja pritiska tokom eksplozije vrši se u skladu sa GOST 12.1.044-89 (Dodatak 12).
Pritisak eksplozije određuje se:

gdje je Pvzr - tlak eksplozije, Pa; Pn - početni pritisak, Pa; T „, i T p.s. - početna temperatura i temperatura produkata sagorevanja. TO; šiljak - broj molova produkata izgaranja i početne smjese.
Maksimalna brzina porasta pritiska (u Pa/s) se izračunava iz jednačine

gdje je Ro početni pritisak. Pa; u - normalna brzina širenja plamena na Po i To m/s; To je početna temperatura smjese, K; r radijus bombe, m; P - R m /P 0 - smanjeni maksimalni pritisak eksplozije; k je adijabatski indeks za smjesu koja se ispituje; e- termokinetički indikator, u zavisnosti od i n, pritiska i temperature; ako vrijednost e nepoznato, uzima se jednakim 0,4.
Prosječna brzina porasta pritiska (u Pa/s) izračunava se iz jednačine:
"s1R _ ZR 0 i '(i-)-i k * e ^m) sa g / (l, k, e)
gdje ^m,k 7 e)-funkcija, njena vrijednost se nalazi prema nomogramu sl. 1.37.

Rice. 1.37. Funkcionalna zavisnost /(n, c.s) od sniženog pritiska n=P/P K,„ adijabatski eksponent to i termokinetički indeks sa ispitna smjesa (dodatak GOST 12.1.044-84)
Vrijednosti tg a k se nalazi termodinamičkim proračunom ili. u slučaju nemogućnosti obračuna, prihvatiti to= 9,0 i k=1,4.
Hitni i hitni slučajevi
Nesreća je opasan događaj izazvan čovjekom koji stvara prijetnju po život i zdravlje ljudi na objektu, određenoj teritoriji ili akvatoriju i dovodi do uništenja zgrada, objekata, opreme i vozila, ometanja procesa proizvodnje ili transporta. , kao i oštećenja prirodnog okoliša (GOST R 22.0 .05-94).
Nesreća je destruktivno nekontrolisano oslobađanje energije ili hemijski (biološki, radijacioni) aktivnih komponenti. U zavisnosti od izvora nastanka, razlikuju se vanredne situacije (ES) prirodne, veštačke i prirodno izazvane čovekom. Na sl. 1.38 pokazuje relativni rast broja prirodnih nesreća i katastrofa uzrokovanih ljudskim djelovanjem i prirodnim djelovanjem u Rusiji. Na sl. 1.39 prikazuje dinamiku broja svih nesreća izazvanih ljudskim djelovanjem u Rusiji za period 1990-94. Iz slike se vidi da se porast broja hitnih slučajeva ne odvija glatko, već naglo, pri čemu se rafali javljaju u periodima neposredno nakon društvenih previranja (avgust 1991., oktobar 1993.).
Broj vanrednih situacija koje je izazvao čovjek posebno je naglo porastao posljednjih godina, uključujući i zrakoplovstvo.
Potencijalni objekti udesa su avioni, kao i skladišta i skladišta za eksplozivne i zapaljive naftne derivate koja se nalaze na teritoriji aerodroma, punjenja i servisa, kao i mesta za popravku. Uzrok hitnih slučajeva može biti curenje ulja.
proizvodi kroz zaptivne jedinice zapornih ventila, prenosnih pumpi, cjevovoda i uređaja za punjenje; kroz ventilaciju gasnog prostora rezervoara; prelivanje rezervoara, cisterni i rezervoara; čišćenje rezervoara; korozijsko uništavanje rezervoara i komunikacija.
Za skladištenje i transport naftnih derivata koriste se različiti kontejneri. Bezbedan rad kontejnera određuje njihova čvrstoća. Međutim, do havarija na ovakvim objektima može doći zbog nedostataka u postojećem sistemu praćenja i praćenja stanja objekata, kao i nepostojanja regulatorne i tehničke dokumentacije.
Prilikom projektovanja, izgradnje i eksploatacije mora se osigurati sigurnost rada skladišta naftnih derivata. Ovakav pristup diktiran je analizom prijemne i operativne dokumentacije, kao i uzrocima vanrednih situacija. Važan zadatak čije će se rješavanje poboljšati pouzdanost eksploatiranih skladišnih objekata je izvođenje njihovih naučno utemeljenih sveobuhvatnih tehničkih pregleda i opremanje sistemom za dijagnostiku i operativno praćenje stanja metala, temelja, toplotnoizolacionih konstrukcija i procesna oprema.
Za sigurno upravljanje tokovima naftnih derivata od velike je važnosti ispravnost tehnološke armature cevovoda: zatvarača, prigušnice, sigurnosnih uređaja; Kontrolni ventili; ventili obrnutog djelovanja (kako bi se spriječila mogućnost pomicanja proizvoda, obrnuto od radnika); armature za hitne slučajeve i prekidne armature (za automatsko zatvaranje protoka u hitni dio ili njegovo gašenje), odvodi kondenzata itd.
Broj nesreća

Rice. 1.38.
- 1 - pg "rođaci;
- 2 - prirodno-tehnološki;
- 3 - tehnogeni

Rice. 1.39.
Kada je oprema bez tlaka, proizvod izlazi i brzo isparava uz stvaranje koncentracije
eksplozivnih i zapaljivih smeša gas-para-vazduh. Slučajne emisije ili curenje mješavine para i plina dovode do stvaranja oblaka koji mogu detonirati. U radu se razmatra detonacija parno-gasnih i aerodisperznih sistema. Pojava detonacije u velikim oblacima objašnjava se sljedećim mehanizmima. Prvi od njih uzima u obzir mogući efekat intenzivnog toplotnog zračenja dugog plamena u oblacima koji su prethodno pomešani turbulentnim tokovima gasa.
Drugi mehanizam za nastanak detonacije uključuje ubrzanje plamena u velikim oblacima zbog razlike u ubrzanjima elementarnih zapremina izgorjelog plina i svježe smjese u turbulentnom plamenu. Ova razlika nastaje pod dejstvom prosečnih gradijenata pritiska u plamenu usled različitog uzgona elementarnih zapremina gasa različite gustine, što dovodi do dodatne turbulencije strujanja i povratne sprege. Ovaj mehanizam pozitivne povratne sprege, određen razlikom gustoće u različitim područjima oblaka, može značajno intenzivirati ubrzanje plamena.
Paljenje je praćeno jakim bljeskom visoke temperature. Najprihvatljivija geometrijska figura bljesnute mješavine pare i plina je figura nepravilne lopte ili elipse (vatrena lopta). Vatrena kugla (OS) se podrazumijeva kao proizvod iznenadnog isparavanja ili curenja gasificiranog goriva (ili plina), praćenog njihovim bljeskom i naknadnim normalnim ili deflagracijskim sagorijevanjem. Za brojna zapaljiva linearna i ciklička pražnjenja ugljovodonika u rasponu gustine od 700 do 1000 kg / m 3, dati su omjeri za prečnik vatrene lopte:
gdje je M masa goriva u OH, kg;
Tf - stvarna temperatura u OR (u oblaku), 0 S;
Trep - referentna (referentna) temperatura, °C.
Raspon koeficijenta 4.2n-5.3 zavisi od vrste goriva i uslova formiranja oblaka.
Za životni vek oblaka tokom njegovog prirodnog sagorevanja, izraz ima oblik:
m = 0M-*1m-1±.
Ove zavisnosti su prikazane na sl. 1.40 i 1.41.

Rice. 1.40.

Rice. 1.41.
Postoji velika opasnost od eksplozije mješavine para-gas-vazduh u zatvorenoj zapremini. U tabeli. 1.7 prikazane su granice detonacije ugljovodonika u vazduhu u zatvorenoj zapremini i otvorenom prostoru, koje ukazuju na veću opasnost od eksplozije gasa ili mešavine gasa i pare u zatvorenoj zapremini. To se objašnjava kako procesima ubrzanja reakcije zbog pojačane autokatalize, tako i pojačavanjem reflektiranih valova tokom početka arijanskog procesa i nizom uvijek postojećih kinetičkih razloga. Povećana lakoća pobuđivanja detonacije u posudama je zbog sposobnosti zidova da stvaraju turbulenciju u strujanju ispred plamena, što ubrzava prijelaz iz sagorijevanja u detonaciju.
Granice detonacije za ugljikovodike u zraku
Eksplozija akumulirane mješavine plina može nastati pod djelovanjem slučajne iskre. Kod otvorenog punjenja naftnog proizvoda moguća je i eksplozija zbog statičkog pražnjenja, posebno u nedostatku uređaja za uzemljenje. Najčešći uzrok eksplozije je iskra, uključujući i rezultat nakupljanja statičkog elektriciteta. Električna iskra može nastati bez ikakvih vodiča i mreže. Opasno je jer se javlja na najneočekivanijim mestima: na zidovima rezervoara, na automobilskim gumama, na odeći, na udaru, na trenju itd. Drugi uzrok eksplozije je nemar i nedisciplina radnika.
Tamo gdje je moguće stvaranje mješavine para-gas-vazduh, potrebno je obezbijediti pouzdanu zaštitu od groma, zaštitu od statičkog elektriciteta, te predvidjeti mjere protiv varničenja električnih uređaja i druge opreme.
U slučaju nesreća povezanih s eksplozijama, dolazi do uništavanja okolnih objekata i ozljeda ljudi. Uništenje je posljedica duhovitog djelovanja produkata eksplozije i zračnog udarnog vala. U ovom slučaju, glavni štetni faktori su udarni val, svjetlosno-termalno zračenje i toksična opterećenja (ugljični monoksid). Osobe koje se nalaze na udaljenosti od 5 m dobijaju opekotine 1. stepena i druge povrede.
Eksplozivne nezgode često su praćene požarima, koji mogu uzrokovati katastrofalne posljedice i naknadne snažnije eksplozije i veća razaranja. Uzroci požara su obično isti kao i eksplozije. U ovom slučaju, eksplozija može biti uzrok ili posljedica požara, i obrnuto, požar može biti uzrok ili posljedica eksplozije.
Požar je spontano nastajajući grad renijuma, koji nije predviđen tehnološkim procesima. Do sagorijevanja naftnih derivata može doći u rezervoarima, proizvodnoj opremi i izlijevanja na otvorenim prostorima. U slučaju požara naftnih derivata u rezervoarima može doći do eksplozija, ključanja i njihovog oslobađanja, a kao posljedica toga i izlijevanja vruće tekućine. Emisije i ključanje naftnih derivata predstavljaju veliku opasnost, što je povezano s prisustvom vode u njima, a karakterizira brzo sagorijevanje pjenaste mase proizvoda. Prilikom ključanja, temperatura se naglo povećava (do 1500 °C) i visina plamena.
Za procjenu stepena oštećenja objekta obično se koristi takozvana kriva praga, koja povezuje tok toplinske i svjetlosne energije q (toplotni tok) i ukupnu energiju O, koja pada po jedinici površine (slika 1.42).

Rice. 1.42.
Za duga vremena termičkog izlaganja, koja prelaze vrijeme mogućeg neoštećenog postojanja objekta, prag oštećenja će biti određen isključivo toplotnim (toplinskim svjetlosnim) fluksom n. Pod impulsima kratke ekspozicije, prag će biti određen uglavnom energijom O. Vrijednosti R i O koje prelaze prag uzrokovat će bezuvjetno oštećenje objekta.
Ako su I ili O manji od njihovih graničnih vrijednosti, tada nema tipične lezije i moguća je samo blaga nelagoda. Na primjer, s povećanjem trajanja zračenja od 0,5 na 2 s, i smanjuje se sa 120 na 30 jedinica, tj. sa blagim povećanjem O čak i sa povećanjem vremena izlaganja za 4 puta, što utiče na povrede
su odsutni, a osoba može osjetiti samo blagu nelagodu.
Međutim, vrijednost ukupne energije O koja pada na objekt uništenja u istom vremenskom periodu raste sa oko 10 na 25 jedinica. (^.
Dakle, linija K, koja odgovara na međusobno povezane promjene u I i O, formira zonu (područje) lezije, naznačenu na slici desno od linije K.
Jedna od najneugodnijih posljedica oštećenja zračnom energijom je opekotine „šipića” i „čepića” oka.
Na sl. 1.43 pokazuje zavisnost i od m, kao i T od m, što određuje područja podnošljive i nepodnošljive boli tokom formiranja toplotnih svjetlosnih opekotina različitog stepena. Kriterijum prikazan na slici zasniva se na činjenici da se kod termičkog zračenja javlja nepodnošljiv bol kada temperatura sloja kože debljine oko 0,14-0,15 mm (ispod površine gornjeg epitelnog sloja) dostigne ili pređe temperaturu od 45° C.
Nakon eliminacije zračenja (ali ne više od 20-30 s), oštar bol se smanjuje, a zatim, u pravilu, potpuno nestaje. Povećanje temperature navedenog sloja za 4-10 stupnjeva ili više uzrokuje šok boli i očite opekotine kože.
Područje podnošljive boli prikazano na grafikonu određeno je činjenicom da se u trenutku izlaganja zračenju javlja biološki zaštitni refleks koji uzrokuje povećanje protoka krvi iz perifernih dijelova tijela, što sprječava lokalno povećanje temperature do graničnog nivoa. Kada je izložen visokoj dozi toplotnog pritiska, ovaj fiziološki mehanizam više ne može da obezbedi potrebno odvođenje toplote, a telo je podvrgnuto patološkim i ponekad previsokim toplotnim opterećenjima. Iz prirode linija na sl. 1.42 pokazuje da postoji određena kvantitativna
doza zračenja q i temperatura T, što uzrokuje termičko oštećenje i pojavu nepodnošljive boli kada se ovoj dozi obezbijedi potrebno vrijeme izlaganja.
Trajanje ekspozicije, s Slika 1.43. Granice termičkih i lakih ozljeda
Nesreće sa avionima (LA) nastaju uglavnom zbog kvara jedinica, na prvom mestu - kvara motora, terorističkih napada, požara, a praćene su eksplozijama. Eksplozija se može dogoditi u zraku ili pri udaru o tlo. Prilikom pada aviona na stambene prostore mogu doći do oštećenja ljudi, objekata i sl. U radu se daju primjeri vanrednih situacija u vazduhoplovstvu, njihova analiza.
Jedna od glavnih opasnosti u vazduhoplovstvu je mogućnost požara prilikom prinudnog sletanja. Gorivo koje izlazi iz oštećenih rezervoara može se zapaliti varnicama koje izazivaju trenje
površinama ili otvorenim plamenom. U ovom slučaju, rezultirajući centar sagorijevanja brzo se širi po svim zonama u kojima su omjeri para/gorivo i zrak unutar raspona zapaljivosti. Jedna od metoda smanjenja rizika od požara je korištenje želatinih goriva, koja se sporije šire i manje su hlapljiva od konvencionalnih tekućih goriva. Kada je rezervoar sa zgusnutim gorivom oštećen, i brzina širenja goriva i brzina stvaranja zapaljivih aerosola se naglo smanjuju. Ovo vam omogućava da produžite vremenski period tokom kojeg putnici mogu biti evakuisani.
Vanredne situacije i vanredne situacije uzrokuju veliku materijalnu štetu i pogoršavaju ekološke probleme. U slučaju udesa praćenih eksplozijama i požarima, dolazi do snažnog mehaničkog, termičkog i hemijskog uticaja na životnu sredinu. Istovremeno, emisije zagađujućih materija naglo rastu; površina zemlje je posuta fragmentima LL, ostacima goriva, produktima sagorevanja; pričinjena je značajna šteta prirodnom krajoliku, flori, fauni; pašnjaci i plodna tla umiru.
Mehanički učinak karakterizira kršenje gornjeg (plodnog) sloja tla zbog njegove površine i dubokog razaranja, utjecaja energije eksplozije (udarni val); narušavanje travnatog pokrivača, oštećenje ili odumiranje žbunja, drveća i drugog rastinja. Struktura gornjeg plodnog sloja, izmjena plina i vode, te kapilarna struktura se mijenjaju.
Mjere koje imaju za cilj poboljšanje sigurnosti u vanrednim situacijama obično se dijele u dvije kategorije. Prvi uključuje aktivnosti koje se provode nakon pojave
vanredna situacija. Aktivnosti El1 obično se nazivaju operativnim, a u suštini se svode na zaštitu stanovništva i otklanjanje posljedica vanrednih situacija. Druga grupa mjera uključuje aktivnosti koje se sprovode unaprijed. To uključuje povećanje pouzdanosti procesne opreme, smanjenje zaliha opasnih materija u objektima, uklanjanje opasnog objekta i poduzimanje ranih mjera za zaštitu ljudi.
Od velikog značaja je sistem aktivne bezbednosti letenja (ASOSPS), koji je element "inteligentnog" sistema podrške pilotu u avionu, poznatog u vazduhoplovnoj praksi kao "pilotski pomoćnik", dizajniran da radi i u normalnom i u nenormalnom letu. situacije. ASOBP izdaje signale upozorenja o prijetnji po sigurnost letenja, kao i blagovremeno savjetodavne informacije u obliku „savjeta“ za upravljanje avionom i njegovim kompleksom kako bi se spriječilo da avion uđe u kritične režime leta. Kako bi spriječio sudare sa zemljinom površinom i između aviona, ASOBP generiše prostorne putanje "razdvajanja".
Jedno od efikasnih oblasti rada na prevenciji vazduhoplovnih nesreća je potpuno, duboko i objektivno istraživanje događaja koji su se već desili i izrada preporuka na osnovu toga za sprečavanje njihovog ponavljanja.
Efikasnost takvog rada zavisi ne samo od dovoljnog nivoa resursa, već i od iscrpnih ovlašćenja tela koje sprovodi nezavisnu istragu, omogućavajući mu da utiče na bilo koju oblast sistema vazdušnog saobraćaja (proizvodnja, projektovanje, ispitivanje, sertifikacija , rad, popravak, regulatorni okvir, itd.) .
Standard 5.4. Aneks 13 Konvencije o međunarodnom civilnom vazduhoplovstvu kaže: „Ovlašćenju za istragu nesreća daće se nezavisnost u sprovođenju istrage i neograničena ovlašćenja za njeno sprovođenje“. Ovaj zahtjev je također implementiran u Ruskim istražnim pravilima koje je odobrila Vlada Ruske Federacije. Međudržavni vazduhoplovni komitet (IAC) formiran na osnovu Sporazuma dobio je od šefova država i vlada ZND pravo da samostalno istražuje vazduhoplovne nesreće. Od 1992. godine, stručnjaci IAC-a istražili su više od 270 zrakoplovnih nesreća, uključujući više od 50 međunarodnih, uključujući istrage o događajima sa avionima zapadne proizvodnje.
Trenutno u svijetu postoji sedam takvih specijalizovanih centara za istraživanje nesreća (SAD, Francuska, Velika Britanija, Kanada, Njemačka, Australija i IAC).
Ne mali značaj je i informisanje država sa podacima o kvarovima i kvarovima vazduhoplovne opreme i pogrešnim postupcima posada. Koristeći ove podatke, vazduhoplovne vlasti svake države mogu preduzeti preventivne mere.