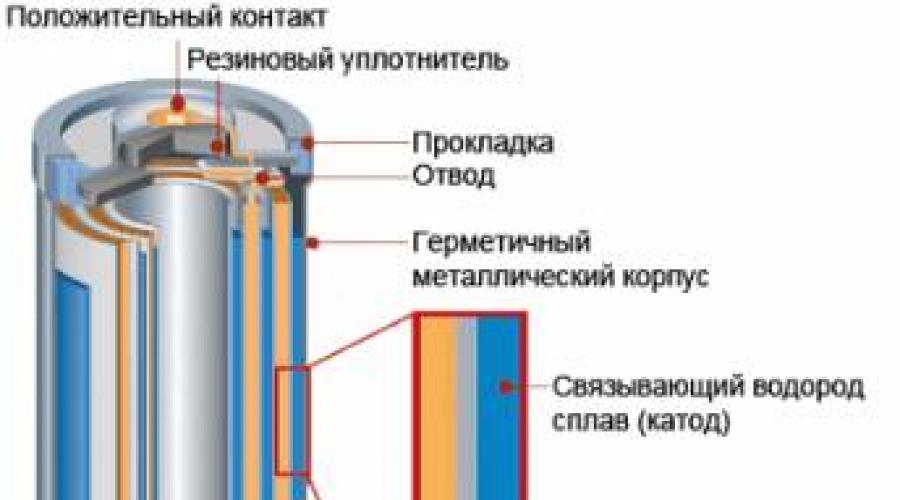
Quruq galvanik hujayra. Kimyoviy oqim manbalari - galvanik elementlar
Shuningdek o'qing
IN zamonaviy sharoitlar Tokning eng keng tarqalgan kimyoviy manbalari galvanik hujayralardir. Ularning shaxsiy kamchiliklariga qaramay, ular elektronikada keng qo'llaniladi, amalga oshiriladi doimiy ish ularni yaxshilash uchun. Galvanik hujayraning ishlash printsipi juda oddiy. Mis va sink plitalari sulfat kislotaning suvli eritmasiga botiriladi, keyin esa ijobiy va salbiy qutblar vazifasini bajaradi.
Galvanik elementning ishlash printsipi
Qutblar o'tkazgich yordamida ulanganda oddiy elektr davri paydo bo'ladi. Element ichidagi oqim oqimi manfiy zaryaddan musbat zaryadga, ya'ni sink plastinkasidan misga o'tadi. Zaryadlangan zarrachalarning tashqi kontur bo'ylab harakati teskari yo'nalishda bo'ladi.
Ta'sir qilinganda elektr toki sulfat kislota qoldiqlarining, shuningdek, vodorod ionlarining harakati turli yo'nalishlarda sodir bo'ladi. Shu bilan birga, vodorod zaryadni mis plastinkaga o'tkazadi, qolgan kislota esa sink plastinkasiga o'tadi. Shunday qilib, terminallarda kuchlanish saqlanib qoladi. Shu bilan birga, vodorod pufakchalari mis plastinkaga joylashib, elementning umumiy ta'sirini zaiflashtiradi va qo'shimcha kuchlanish hosil qiladi. Ushbu kuchlanish qutblanishning elektromotor kuchi sifatida tanilgan. Ushbu hodisaning oldini olish uchun tarkibga vodorod atomlarini o'zlashtira oladigan va depolarizatsiya funktsiyasini bajaradigan modda kiritiladi.
Galvanik hujayralar: afzalliklari va kamchiliklari
Zamonaviy galvanik hujayralarni ishlab chiqarish uchun eng ko'p turli materiallar. Eng keng tarqalgan - barmoq tipidagilar uchun ishlatiladigan uglerod-sink elementlariga asoslangan materiallar.
Ularning asosiy ijobiy sifat nisbatan ko‘rib chiqiladi arzon. Biroq, bunday elementlar kam quvvat va qisqa raf muddatiga ega. Ko'pchilik eng yaxshi variant ishqoriy elementlardan foydalanishga xizmat qiladi. Bu erda elektrolit ko'mir emas, balki gidroksidi eritmadir. Bo'shatish vaqtida gaz chiqmaydi, bu esa to'liq muhrlanishni ta'minlaydi. Ishqoriy elementlar ko'proq farq qiladi yuqori muddatli saqlash

Galvanik elementning umumiy ishlash printsipi barcha turlar uchun mutlaqo bir xil. Masalan, simob oksidi asosidagi elementlar tuzilish jihatidan ishqoriy elementlarga o'xshaydi. Ular yuqori haroratga chidamliligi, yuqori mexanik kuch va barqaror kuchlanish qiymatlari bilan tavsiflanadi. Kamchilik simobning toksikligi bo'lib, u chiqindi elementlarga ehtiyotkorlik bilan munosabatda bo'lishni talab qiladi.
Bugungi kunda galvanik hujayralar eng keng tarqalgan kimyoviy hujayralardan biri bo'lib, ularning kamchiliklariga qaramay, ular elektrotexnika sohasida faol qo'llaniladi va doimiy ravishda takomillashtiriladi.
Ishlash printsipi
Galvanik hujayra qanday ishlashining eng oddiy misoli shunday ko'rinadi. Ikkita plastinka sulfat kislotaning suvli eritmasi bilan shisha idishga botiriladi: biri mis, ikkinchisi sink. Ular elementning ijobiy va salbiy qutblariga aylanadi. Agar bu qutblar o'tkazgich bilan bog'langan bo'lsa, siz eng oddiy narsani olasiz element ichida, oqim salbiy zaryadga ega bo'lgan sink plitasidan musbat zaryadlangan mis plastinkaga oqib o'tadi. Tashqi zanjirda zaryadlangan zarrachalarning harakati teskari yo'nalishda sodir bo'ladi.
Oqim ta'sirida vodorod ionlari va sulfat kislotaning kislotali qoldig'i ichkariga kiradi turli yo'nalishlar. Vodorod o'z zaryadlarini mis plastinkaga, kislota qoldig'i esa sink plastinkasiga o'z zaryadini beradi. Bu element terminallarida kuchlanishni saqlab qoladi. Shu bilan birga, vodorod pufakchalari mis plastinka yuzasiga joylashadi, bu galvanik hujayraning ta'sirini zaiflashtiradi. Vodorod plastinkaning metalli bilan birgalikda qo'shimcha kuchlanish hosil qiladi, bu polarizatsiyaning elektromotor kuchi deb ataladi. Ushbu EMF ning zaryad yo'nalishi galvanik elementning EMF zaryad yo'nalishiga qarama-qarshidir. Pufakchalar o'zlari elementda qo'shimcha qarshilik hosil qiladi.
Biz ko'rib chiqqan element klassik misoldir. Aslida, bunday galvanik elementlar yuqori polarizatsiya tufayli oddiygina ishlatilmaydi. Buning oldini olish uchun elementlarni ishlab chiqarish jarayonida ularning tarkibiga vodorod atomlarini o'zlashtiradigan maxsus modda kiritiladi, bu depolarizator deb ataladi. Qoida tariqasida, bular kislorod yoki xlor o'z ichiga olgan preparatlardir.
Zamonaviy galvanik elementlarning afzalliklari va kamchiliklari
Zamonaviy galvanik hujayralar turli materiallardan tayyorlangan. Eng keng tarqalgan va tanish turi - ishlatiladigan uglerod-sink elementlari AA batareyalari. Ularning afzalliklari nisbatan arzonlikni o'z ichiga oladi, kamchiliklari esa yo'q uzoq muddatli saqlash va kam quvvat.
Ko'proq qulay variant- Bu ishqoriy galvanik hujayralar. Ular marganets-sink deb ham ataladi. Bu erda elektrolit ko'mir kabi quruq modda emas, balki gidroksidi eritmadir. Bo'shatilganda, bunday elementlar deyarli gaz chiqarmaydi, buning natijasida ularni germetik tarzda yopish mumkin. Bunday elementlarning saqlash muddati uglerod-sink elementlariga qaraganda yuqori.
Simob elementlari konstruktsiyasi bo'yicha ishqoriy elementlarga o'xshaydi. Bu erda simob oksidi ishlatiladi. Bunday oqim manbalari, masalan, tibbiy asbob-uskunalar uchun ishlatiladi. Ularning afzalliklari yuqori haroratga qarshilik (+50 gacha, ba'zi modellarda +70 ˚S gacha), barqaror kuchlanish, yuqori mexanik kuch. Kamchilik simobning toksik xususiyatlari bo'lib, shuning uchun sarflangan elementlarni juda ehtiyotkorlik bilan ishlatish va qayta ishlashga yuborish kerak.
Ba'zi hujayralarda kumush oksidi katodlarni tayyorlash uchun ishlatiladi, ammo metallning yuqori narxi tufayli ulardan foydalanish iqtisodiy jihatdan foydali emas. Lityum anodli hujayralar ko'proq uchraydi. Ularning narxi ham yuqori, lekin ko'rib chiqilgan barcha turdagi galvanik hujayralar orasida eng yuqori kuchlanishga ega.
Galvanik hujayralarning yana bir turi kontsentratsion galvanik hujayralardir. Ularda zarrachalar harakati jarayoni ion ko`chishi bilan ham, bo`lmasdan ham sodir bo`lishi mumkin. Birinchi tur - ikkita bir xil elektrodlar yarim o'tkazuvchan bo'linma bilan ajratilgan turli konsentratsiyalarga botiriladigan element. Bunday elementlarda EMF ionlarning konsentratsiyasi past bo'lgan eritmaga o'tkazilishi tufayli yuzaga keladi. Ikkinchi turdagi elementlarda elektrodlar ishlab chiqariladi turli metallar, va konsentratsiya elektrodlarning har birida sodir bo'ladigan kimyoviy jarayonlar tufayli tekislanadi. bu elementlar birinchi turdagilardan yuqori.
Galvanik hujayralar va batareyalar G element yoki galvanik juftlik ikkitadan iborat qurilma metall plitalar(ulardan biri koks bilan almashtirilishi mumkin), bir yoki ikki xil suyuqlikka botiriladi va galvanik oqim manbai bo'lib xizmat qiladi. Bir-biriga ma'lum bir tarzda ulangan ma'lum miqdordagi voltaik elementlar galvanik batareyani tashkil qiladi. Tuzilishi bo'yicha eng oddiy element ikki plastinkadan iborat bo'lib, gil yoki shisha stakanga botiriladi, unda plastinka turiga mos keladigan suyuqlik quyiladi; plitalar suyuqlikda metall bilan aloqa qilmasligi kerak. D. elementlari deyiladi asosiy agar ular oqimning mustaqil manbalari bo'lsa va ikkinchi darajali agar ular faqat ularni zaryadlovchi elektr energiyasi manbalariga ko'proq yoki kamroq uzoq vaqt ta'sir qilishdan keyin kuchga kirsa. Voltaik elementlarning kelib chiqishini ko'rib chiqayotganda, voltaik ustundan, keyingi barcha galvanik batareyalarning ajdodidan yoki Voltaik chashka batareyasidan boshlash kerak. Voltaj ustuni. Uni yaratish uchun Volta tagida katlanmış yoki hatto lehimlangan bir-biriga o'xshash bo'lmagan metall doiralarni va suv yoki kaustik kaliy eritmasi bilan namlangan karton yoki mato doiralarini oldi. Dastlab, kumush va mis krujkalar, keyin esa odatda sink va mis ishlatilgan. Diagrammada ko'rsatilganidek, ulardan ustun yasaldi. 1, ya'ni: birinchi navbatda, mis plastinka qo'yiladi va uning ustiga rux plitasi qo'yiladi (yoki aksincha), uning ustiga namlangan karton doira qo'yiladi; bu bitta juftni tashkil etdi, uning ustiga ikkinchisi o'rnatilgan, yana mis, rux va karton doiralardan iborat bo'lib, birinchi juftlikdagi kabi bir xil tartibda bir-biriga o'rnatilgan. Keyingi juftlarni bir xil tartibda qo'llashni davom ettirib, siz ustunni yaratishingiz mumkin; shaytonda ko'rsatilgan ustun. 1, chap tomonda, 11 voltli juftlikdan iborat. Agar izolyatsion, ya'ni elektr o'tkazmaydigan, masalan, shisha plitasiga ustun o'rnatilgan bo'lsa, uning o'rtasidan boshlab ustunning yarmi (bizning rasmimizdagi pastki qismi) zaryadlanadi. musbat elektr, ikkinchisi (chizmadagi yuqori) - salbiy. O'rtada sezilmaydigan elektr energiyasining intensivligi, u eng katta bo'lgan uchlarga yaqinlashganda kuchayadi. Simlar eng past va eng yuqori plitalarga lehimlanadi; simlarning erkin uchlarini kontaktga keltirish musbat elektr tokining qutbning pastki uchidan sim orqali yuqoriga va manfiy elektrning teskari yo'nalishda harakatlanishiga olib keladi; elektr yoki galvanik oqim hosil bo'ladi (bu so'zni ko'ring). Volta oʻxshash boʻlmagan metallardan iborat ikkita plastinani juft deb hisoblab, suyuqlikka faqat elektr tokini oʻtkazish qobiliyatini bogʻlagan (qarang Galvanizm); ammo keyinroq o'rnatilgan ko'rinishga ko'ra, bu juftlik ikkita o'xshash bo'lmagan plastinka va suyuqlik qatlamidan iborat ular orasida; shuning uchun ustunning eng yuqori va pastki plitalari (o'ngdagi 1-rasm) olib tashlanishi mumkin. Bunday ustun 10 juftdan iborat bo'ladi, keyin uning eng pastki plitasi mis, eng yuqori qismi esa rux bo'ladi va elektr tokining harakat yo'nalishi yoki galvanik oqim yo'nalishi bir xil bo'lib qoladi: pastki uchidan. ustundan (hozir sinkdan) yuqoriga (misga). Qutbning mis uchi musbat qutb, rux uchi manfiy qutb deb ataldi. Keyinchalik, Faraday terminologiyasida musbat qutb deyiladi anod, salbiy - katod. Voltaik ustunni gorizontal ravishda chuqurchaga yotqizish mumkin, ichkarida harpius bilan eritilgan mumning izolyatsion qatlami bilan qoplangan. Hozirgi vaqtda voltaik qutbni yig'ish va demontaj qilish uchun katta mehnat va vaqt talab qilinganligi sababli foydalanilmaydi; lekin o'tmishda ular yuzlab va minglab juftlardan tashkil topgan ustunlardan foydalanganlar; Professor V. Petrov 1801-2 yillarda Peterburgda foydalangan. Ba'zan 4200 juftdan iborat bo'lgan ustun bilan tajribalar paytida (qarang Galvanizm), Volta o'z apparatini boshqa shaklda, ya'ni keyingi batareyalar shaklida qurdi. Volta batareyasi (korona di tazze) aylana bo'ylab joylashgan stakanlardan iborat bo'lib, ichiga quyiladi. iliq suv yoki tuz eritmasi; har bir kosada bir-biriga qarama-qarshi bo'lgan ikkita o'xshash bo'lmagan metall plastinka bor edi. Har bir plastinka qo'shni stakanning o'xshash bo'lmagan plastinkasiga sim orqali ulanadi, shuning uchun bir stakandan ikkinchisiga butun aylana bo'ylab plitalar doimiy ravishda almashinadi: rux, mis, keyin yana rux va mis va hokazo. Doira yopilgan joyda. , bir stakanda sink plitasi, ikkinchisida - mis; bu tashqi plitalarni bog'laydigan sim bo'ylab oqim mis plastinkadan (musbat qutb) sink plastinkaga (salbiy qutb) oqib o'tadi. Volta bu batareyani qutbga qaraganda kamroq qulay deb hisobladi, lekin aslida u keng tarqalgan batareyaning shakli edi. Darhaqiqat, voltaik ustunning tuzilishi tez orada o'zgartirildi (Cruikshank): cho'zinchoq yog'och quti, suyuqlik quyilgan kichik bo'linmalarga lehimlangan mis va sink plitalari bilan ko'ndalang bo'linib, an'anaviy voltaik ustunga qaraganda qulayroq edi. Yog'och xoch devorlari bilan bo'linmalarga bo'lingan quti yanada yaxshi edi; Har bir qismning ikkala tomoniga mis va rux plitalari qo'yilib, tepada bir-biriga lehimlangan, bu erda qo'shimcha ravishda ko'z qopqog'i qoldirilgan. Barcha quloqlardan o'tadigan yog'och tayoq barcha plitalarni suyuqlikdan ko'tarish yoki ularni cho'ktirish uchun xizmat qildi. Bir suyuqlikka ega elementlar. Ko'p o'tmay, batareyalarga birlashtirilishi mumkin bo'lgan alohida juftliklar yoki hujayralar yaratila boshlandi turli yo'llar bilan. Elementlarning elektr qo'zg'atuvchi kuchi metallar va suyuqliklar va ularning tarkibiy qismlariga, ichki qarshilik esa suyuqliklarga va elementlarning o'lchamiga bog'liq. Qarshilikni kamaytirish va oqim intensivligini oshirish uchun o'xshash bo'lmagan plitalar orasidagi suyuqlik qatlamining qalinligini kamaytirish va metallarning suvga cho'mgan yuzasi hajmini oshirish kerak. Bu ichida amalga oshiriladi Vollaston elementi(Vollaston - Wulstenning to'g'ri talaffuziga ko'ra). Sink egilgan mis plastinka ichiga joylashtiriladi, unda plitalarga tegmaslik uchun yog'och yoki mantar bo'laklari kiritiladi; plitalarning har biriga sim, odatda mis lehimlanadi; bu simlarning uchlari tashqi o'tkazgichlar bo'ylab misdan ruxga va sinkdan misga yo'nalishda oqadigan oqimni o'tkazmoqchi bo'lgan ob'ekt bilan aloqa qiladi. ichki qismlar element. Umuman olganda, oqim suyuqlik ichida oqadi suyuqlik kimyoviy jihatdan kuchliroq ta'sir qiladigan metalldan kamroq kuchliroq ta'sir qiladigan boshqasiga. Bu hujayrada sink plitasining ikkala yuzasi elektr oqimi uchun xizmat qiladi; Plitalardan birining sirtini ikki barobarga oshirishning bu usuli keyinchalik barcha elementlarni bitta suyuqlik bilan joylashtirishda qo'llanila boshlandi. Vollaston elementida tok taʼsirida parchalanadigan suyultirilgan sulfat kislota ishlatiladi (qarang Galvanik oʻtkazuvchanlik); parchalanish natijasi sinkning oksidlanishi va sink sulfatining hosil bo'lishi, suvda eriydi va mis plastinkada vodorodning chiqishi bo'ladi, bu esa qutblangan holatga keladi (qarang Galvanik qutblanish va Galvanik o'tkazuvchanlik), oqimni kamaytiradi. kuch. Ushbu qutblangan holatning o'zgaruvchanligi oqim kuchining o'zgaruvchanligi bilan birga keladi. Biz bitta suyuqlik bilan ko'p elementlarni chaqiramiz media elementlari(Smee) va Yashil, birinchisida - ikkita sink plitalari orasida platina yoki platinalangan kumush, barchasi suyultirilgan sulfat kislotaga botiriladi. Kimyoviy ta'siri Wollaston elementidagi kabi va platinadagi vodorod bilan qutblangan; lekin oqim kamroq o'zgaruvchan. Elektr qo'zg'alish kuchi mis-sinkga qaraganda kattaroqdir. Grenet elementi koksdan kesilgan ikkita plitka orasiga joylashtirilgan sink plastinkasidan iborat; bu element uchun suyuqlik turli retseptlar bo'yicha tayyorlanadi, lekin har doim dikromopotasyum tuzi, sulfat kislota va suvdan. Bitta retseptga ko'ra, 2500 gramm suv uchun siz 340 gramm nomdagi tuz va 925 gramm sulfat kislota olishingiz kerak. Elektr qo'zg'alish kuchi Wollaston elementiga qaraganda kattaroqdir. Grenet elementining ta'sirida, avvalgi holatlardagi kabi, sink sulfat hosil bo'ladi; ammo vodorod xrom kislota kislorodi bilan qo'shilib, suv hosil qiladi; suyuqlikda xrom alum hosil bo'ladi; qutblanish kamayadi, lekin bartaraf etilmaydi. Grenet elementi uchun, rasmda ko'rsatilganidek, kengaytirilgan pastki qismi bo'lgan shisha idish ishlatiladi. 7-jadval "Galvanik elementlar va batareyalar". Juda ko'p suyuqlik quyiladi, shuning uchun sink plitasi Z, bu koksdan qisqaroq BILAN, unga biriktirilgan tayoqni tortib olish mumkin edi T, element harakatsiz qolishi kerak bo'lgan vaqt davomida suyuqlikdan olib tashlang. Qisqichlar V, V, ulangan - biri novda jant bilan T, va shuning uchun sink bilan, ikkinchisi esa ko'mirning jantiga ega, o'tkazgich simlarining uchlariga tayinlanadi. Yozuvlar ham, ularning ramkalari ham bir-biri bilan metall aloqaga ega emas; oqim tashqi ob'ektlar orqali birlashtiruvchi simlar bo'ylab koksdan sinkgacha bo'lgan yo'nalishda oqadi. Uglerod-sink elementi stol tuzining eritmasi bilan ishlatilishi mumkin (Shveytsariyada, telegraflar, qo'ng'iroqlar uchun) va keyin u 9-12 oy davomida amal qiladi. g'amxo'rliksiz. Laland va Chaperone elementi, Edison tomonidan takomillashtirilgan, sink plitasidan va mis oksididan siqilgan boshqa plitadan iborat. Suyuqlik gidroksidi kaliy eritmasi hisoblanadi. Kimyoviy ta'sir sinkning oksidlanishi bo'lib, keyinchalik kaliy bilan birikma hosil qiladi; Sink oksidi kislorodi bilan oksidlangan ajratilgan vodorod hosil bo'lgan suvning bir qismiga aylanadi va mis kamayadi. Ichki qarshilik past. Qo'zg'atuvchi kuch aniqlik bilan aniqlanmaydi, lekin Doniyor elementidan kamroq. Ikkita suyuqlikli elementlar. Vodorod elementlarining qattiq jismlaridan birida vodorodning chiqishi oqim kuchini pasaytiradigan (aslida elektr hayajonli) va uni beqaror qiladigan sabab bo'lganligi sababli, vodorod chiqariladigan plastinkani berish qobiliyatiga ega suyuqlikka joylashtirish. vodorod bilan birikish uchun kislorod oqimi doimiy bo'lishi kerak. Bekkerel birinchi bo'lib (1829) Grenet va Lalande elementlari hali ma'lum bo'lmaganda, ikkita suyuqlik bilan mis-rux elementini yaratdi. Keyinchalik Daniel(1836) shunga o'xshash elementni ishlab chiqdi, ammo ulardan foydalanish qulayroq. Suyuqliklarni ajratish uchun ikkita idish kerak bo'ladi: bir shisha yoki sirlangan loydan idish, silindrsimon, loydan, ozgina pishirilgan va shuning uchun g'ovak, suyuqliklardan biri quyilgan va metallardan biri joylashtirilgan idish; ikki idish orasidagi halqa shaklidagi bo'shliqda boshqa metallning plastinkasi botiriladigan boshqa suyuqlik quyiladi. Doniyor elementida sink zaif sulfat kislotaga, mis esa mis (ko'k) sulfatning suvli eritmasiga botiriladi. Anjir. Jadvalning 1-da batareyaga ulangan 3 ta Doniyor elementi tasvirlangan; ruxdan egilgan tsilindrlar tashqi shisha stakanlarga, mis plitalar, shuningdek, silindr shaklida yoki S harfi kabi egilib, ichki loy tsilindrlarga joylashtiriladi. Siz uni boshqa yo'l bilan joylashtirishingiz mumkin, ya'ni tashqi idishlarda mis. Oqim misdan ruxga tashqi o'tkazgichlar orqali va ruxdan misga hujayradagi suyuqlik yoki batareyaning o'zi orqali o'tadi va ikkala suyuqlik bir vaqtning o'zida parchalanadi: sulfat kislotasi bo'lgan idishda rux sulfat hosil bo'ladi va vodorod mis plastinkaga o'tadi, bir vaqtning o'zida mis sulfat (CuSO 4) mis (Cu) ga parchalanadi, mis plastinka ustiga yotqiziladi va alohida emas. mavjud aloqa(SO 4), u kimyoviy jarayon orqali vodorod bilan suv hosil qiladi, u mis ustida pufakchalar shaklida ajralib chiqishga ulgurmasdan oldin. Ikkala suyuqlik bilan osongina namlangan g'ovakli loy kimyoviy jarayonlarni zarrachadan zarrachaga ikkala suyuqlik orqali bir metalldan ikkinchisiga o'tkazish imkonini beradi. Davomiyligi uning kuchiga (va bu qisman tashqi qarshiliklarga), shuningdek idishlardagi suyuqlik miqdoriga bog'liq bo'lgan oqim ta'siridan so'ng barcha mis sulfat iste'mol qilinadi, bu rangning o'zgarishi bilan ko'rsatilgan. uning yechimi; keyin mis ustida vodorod pufakchalarining ajralishi boshlanadi va shu bilan birga bu metallning qutblanishi. Ushbu element doimiy deb ataladi, ammo buni nisbatan tushunish kerak: birinchidan, to'yingan vitriol bilan ham zaif polarizatsiya mavjud, ammo asosiysi elementning ichki qarshiligi avval kamayadi va keyin ortadi. Bunga ko'ra ikkinchi va asosiy sabab Element ta'sirining boshida oqimning asta-sekin o'sishi kuzatiladi, qanchalik muhim bo'lsa, oqim kuchi tashqi yoki ichki qarshiliklar tomonidan zaiflashadi. Yarim soat, bir soat yoki undan ko'proq vaqt o'tgach (davomiylik sink bilan suyuqlik miqdori bilan ortadi), oqim kuchayganidan ko'ra sekinroq zaiflasha boshlaydi va yana bir necha soatdan keyin u o'zining dastlabki kuchiga etib, asta-sekin yanada zaiflashadi. Agar erimagan shaklda bu tuzning zaxirasi mis sulfat eritmasi bo'lgan idishga joylashtirilsa, bu oqim mavjudligini davom ettiradi, shuningdek, olingan rux sulfat eritmasini yangi suyultirilgan sulfat kislota bilan almashtiradi. Biroq, yopiq element bilan, rux bilan suyuqlik darajasi asta-sekin pasayadi va mis bilan u ko'tariladi - bu o'z-o'zidan oqimni zaiflashtiradigan (shu sababli qarshilikning oshishi) va bundan tashqari, suyuqlikning bir elementdan o'tishini ko'rsatadi. idish boshqasiga (ionlarning o'tkazilishi, qarang: Galvanik o'tkazuvchanlik, galvanik osmos). Mis sulfat sink bilan idishga singib ketadi, undan rux sof kimyoviy yo'l bilan misni chiqaradi, bu uning qisman ruxda va qisman loy idishning devorlarida cho'kishiga olib keladi. Shu sabablarga ko'ra, oqim uchun foydasiz bo'lgan sink va mis sulfatning katta chiqindilari mavjud. Biroq, Doniyor elementi hali ham eng doimiy elementlardan biri hisoblanadi. Loy shisha, garchi suyuqlik bilan namlangan bo'lsa-da, oqimga katta qarshilik ko'rsatadi; loy o'rniga pergamentni ishlatib, qarshilikni kamaytirish orqali oqimni sezilarli darajada oshirish mumkin (Karre elementi); pergament hayvon qabariq bilan almashtirilishi mumkin. Suyultirilgan sulfat kislota o'rniga siz stol yoki eritmasidan foydalanishingiz mumkin dengiz tuzi; qo'zg'atuvchi kuch deyarli bir xil bo'lib qoladi. Kimyoviy ta'sirlar o'rganilmagan. Meidinger elementi. Tez-tez va uzluksiz va bundan tashqari, etarlicha doimiy, ammo zaif oqim uchun Doniyor elementining modifikatsiyasi bo'lgan Meidinger elementi (jadvalning 2-rasm) ishlatilishi mumkin. Tashqi oynaning yuqori qismida kengaytmasi bor, u erda sink tsilindri ichki labda joylashgan; Stakanning pastki qismida yana bir kichik joy qo'yiladi, unda mis varaqdan o'ralgan silindr qo'yiladi yoki ichki idishning pastki qismiga mis doira qo'yiladi, keyin u mis sulfat eritmasi bilan to'ldiriladi. Shundan so'ng, hamma narsani to'ldiradigan magniy sulfat eritmasini ehtiyotkorlik bilan to'kib tashlang bo'sh joy tashqi idish va vitriol eritmasini siqib chiqarmaydi, chunki u kattaroqdir solishtirma og'irlik. Shunga qaramay, suyuqliklarning tarqalishi orqali vitriol asta-sekin sinkga etib boradi va u erda misdan voz kechadi. Ushbu eritmaning to'yinganligini saqlab qolish uchun element ichiga mis sulfat va suv bo'laklari bo'lgan ag'darilgan shisha idish qo'yiladi. Supero'tkazuvchilar metallardan tashqariga chiqadi; ularning suyuqlikdagi qismlari guttapercha qobig'iga ega. Elementda loy idishning yo'qligi uni ishlatishga imkon beradi uzoq vaqt davomida; anchadan beri uning qismlarini o'zgartirmasdan; lekin uning ichki qarshiligi yuqori, uni bir joydan ikkinchi joyga juda ehtiyotkorlik bilan ko'chirish kerak va u juda ko'p mis sulfatni o'z ichiga oladi, bu oqim uchun foydasizdir; hatto kichik elementning kolbasiga taxminan 1/2 kilogramm vitriol qo'yiladi. Bu telegraflar, elektr qo'ng'iroqlari va boshqa shunga o'xshash holatlar uchun juda mos keladi va bir necha oy turishi mumkin. Callot va Trouvé-Callot elementlari Meidinger elementlariga o'xshash, ammo ikkinchisidan oddiyroq. Kresten Sankt-Peterburgda u Meidinger elementining foydali modifikatsiyasini ham uyushtirdi. Tomson elementi idish yoki tovoqlar shaklida o'zgartirilgan Doniyor mavjud; pergament qog'ozidan tayyorlangan gözenekli tekis membranalar bir suyuqlikni boshqasidan ajratib turadi, ammo siz membranalarsiz qilishingiz mumkin. Siemens elementi Va Halske ham Doniyor toifasiga kiradi. Minotto elementi. Pastki qismida mis doira shisha idish, uning ustiga mis sulfat kristallari quyiladi va tepada qalin kremniyli qum qatlami mavjud bo'lib, uning ustiga sink doirasi qo'yiladi. Hamma narsa suv bilan to'ldirilgan. Telegraf liniyalarida 1 1/2 dan 2 yilgacha davom etadi. Qum o'rniga siz hayvonlarning ko'mir kukunini (Darsonval) olishingiz mumkin. Trouvé elementi. Pastki qismida mis sulfat va yuqori qismida rux sulfat bilan singdirilgan, o'tkazuvchi qog'ozdan yasalgan doiralar ustuni bo'lgan mis doira. Qog'ozni namlaydigan oz miqdorda suv elementni faollashtiradi. Qarshilik ancha yuqori, harakat uzoq va doimiy. Grove elementi, platina-sink; platina kuchli nitrat kislotaga, rux zaif sulfat kislotaga botiriladi. Oqim ta'sirida chiqarilgan vodorod nitrat kislota kislorodi (NHO 2) bilan oksidlanadi, u nitrat angidridga (N 2 O 4) aylanadi, uning ajralib chiqqan qizil-to'q sariq bug'lari nafas olish uchun zararli va barcha misni buzadi. apparatning qismlari, shuning uchun ular qo'rg'oshindan yaxshiroqdir. Ushbu elementlar faqat mavjud bo'lgan laboratoriyalarda ishlatilishi mumkin dudbo'ronlar, va ichida oddiy xona pechka yoki kaminga joylashtirilishi kerak; ular yuqori qo'zg'atuvchi kuchga va past ichki qarshilikka ega - yuqori oqim kuchi uchun barcha sharoitlar mavjud, bu element tarkibidagi suyuqliklar hajmi qanchalik doimiy bo'lsa. Anjir. Jadvalning 6-bandida bunday element tasvirlangan tekis shakl; uning tashqarisida o'ng tomonda elementning platina varag'iga ulangan egilgan sink plitasi mavjud Z ikkinchi element, uning burmasida tekis loydan idish joylashgan V platina uchun. Chap tomonda sink elementiga mahkamlangan va uchinchi elementga tegishli bo'lgan platina varag'i joylashgan. Ushbu shakldagi elementlar bilan ichki qarshilik juda kichik, ammo suyuqlikning oz miqdori tufayli oqimning kuchli ta'siri uzoq davom etmaydi. Yuqorida aytib o'tilgan umumiy qoidaga ko'ra, oqim platinadan tashqi o'tkazgichlar orqali sinkga o'tadi. Bunsen elementi(1843), ko'mir-sink avvalgisini to'liq almashtiradi va undan arzonroqdir, chunki qimmatbaho platina koks plitkalari bilan almashtiriladi. Suyuqliklar Grove elementi bilan bir xil, elektr qo'zg'alish kuchi va qarshilik taxminan bir xil; oqimning yo'nalishi bir xil. Shunga o'xshash element rasmda ko'rsatilgan. 3 ta stol; harf bilan belgilangan ko'mir kafel BILAN,+ belgisi bo'lgan metall qisqich bilan; bu elementning musbat qutbi yoki anodidir. Rux tsilindridan Z qisqich bilan (salbiy qutb yoki katod) batareya holatida ikkinchi elementning uglerod plitasiga qo'llaniladigan boshqa qisqichli plastinka mavjud. Grove birinchi bo'lib o'z elementidagi platinani ko'mir bilan almashtirdi, ammo uning tajribalari unutildi. Darsonval elementi, uglerod-sink; ko'mir bilan azot aralashmasi va xlorid kislotasi Har biri 1/20 sulfat kislota o'z ichiga olgan 2 hajmli suv bilan 1 hajm. Fora elementi.- koks bar o'rniga grafit va loydan tayyorlangan shisha ishlatiladi; U erda nitrat kislota quyiladi. Bunsen elementidagi bu tashqi ko'rinishdagi o'zgarish nitrat kislotadan foydalanishni to'liqroq qiladi. Sosnovskiy elementi.- natriy gidroksidi yoki kaliy gidroksidi eritmasida sink; 1 hajm nitrat kislota, 1 hajm sulfat kislota, 1 hajm xlorid kislota, 1 hajm suvdan iborat suyuqlikdagi ko'mir. O'zining juda yuqori elektr qo'zg'atuvchi kuchi bilan ajralib turadi. Kallan elementi.- Bunsen elementlarining uglerodlari temir bilan almashtiriladi; qo'zg'atuvchi kuch ko'mirdan foydalanganda bir xil bo'lib qoladi. Temir passiv holatda bo'lgan nitrat kislotaga ta'sir qilmaydi. Temir o'rniga kremniy tarkibidagi quyma temirdan foydali foydalanish mumkin. Poggendorff elementi Bunsen elementidan nitrat kislotani Grenet elementida ishlatiladiganga o'xshash suyuqlik bilan almashtirish bilan farq qiladi. 100 qism suvda eritilgan kaliy dixromatning og'irligi bo'yicha 12 qismga 25 qism kuchli sulfat kislota qo'shing. Qo'zg'atuvchi kuch Bunsen elementi bilan bir xil; lekin ichki qarshilik kattaroqdir. Vodorodning oksidlanishi uchun berilgan suyuqlikdagi kislorod bir xil hajmdagi nitrat kislotaga qaraganda kamroq. Ushbu elementlardan foydalanganda hidning yo'qligi, boshqa afzalliklar bilan birgalikda foydalanish uchun eng qulay bo'ldi. Biroq, polarizatsiya to'liq bartaraf etilmagan. Imshenetskiy elementi, uglerod-sink. Xrom kislota eritmasida grafit (uglerod) plastinka, natriy sulfid tuzi eritmasida rux. Yuqori qo'zg'atuvchi kuch, past ichki qarshilik, sinkdan deyarli to'liq foydalanish va xrom kislotasidan juda yaxshi foydalanish. Leclanche elementi, uglerod-sink; oksidlovchi suyuqlik o'rniga, u ko'mir plitasida marganets peroksidning kukunini (katta) o'z ichiga oladi, koks kukuni bilan aralashtiriladi (5-rasm) ichki, suyuqlik o'tkazuvchan gil idishda; Rux tayoqchasi tashqarida maxsus shakldagi kolbaning burchaklaridan biriga joylashtiriladi. Suyuqlik - ammiakning suvli eritmasi - tashqaridan quyiladi va loy idishga ko'mirga (koks) kirib, marganets peroksidni namlaydi; kavanozning yuqori qismi odatda qatron bilan to'ldiriladi; gazlar chiqishi uchun teshiklar qoldiriladi. Qo'zg'atuvchi kuch Daniel va Bunsen elementlari orasida o'rtacha, qarshilik yuqori. Yopiq qolgan bu element tez pasayib borayotgan quvvat oqimini beradi, lekin telegraflar va uy foydalanish uchun suyuqlik qo'shganda bir yildan ikki yilgacha davom etadi. Ammiak (NH 4 Cl) parchalanganda xlor sinkga ajralib, rux xlorid va ko'mir bilan ammiak hosil qiladi. Kislorodga boy marganets peroksidi asta-sekin pastroq oksidlanish darajasidagi birikmaga o'tadi, lekin massaning barcha qismlarida loy idishni to'ldirmaydi. Marganets peroksidini to'liqroq ishlatish va kamaytirish uchun ichki qarshilik bu elementlar loydan idishsiz joylashtirilgan va plitkalar marganets peroksid va ko'mirdan presslangan bo'lib, ular o'rtasida rasmda ko'rsatilganidek, koks qo'yiladi. 4 ta stol. Ushbu turdagi elementlar yopiq va tashish uchun qulay bo'lishi mumkin; shisha shoxli kauchuk bilan almashtiriladi. Geff bu elementni ham o'zgartirib, ammiak eritmasini rux xlorid eritmasi bilan almashtirdi. Mari-Devi elementi, ko'mir-sink, ko'mir bilan, suv bilan namlangan, g'ovakli loy idishga joylashtirilgan simob sulfatning xamirga o'xshash massasini (Hg 2 SO 4) o'z ichiga oladi. Rux ustiga zaif sulfat kislota yoki hatto suv quyiladi, chunki birinchisi simob tuzidan oqim ta'sirida ajralib chiqadi, unda vodorod oksidlanadi va ko'mir bilan metall simob ajralib chiqadi, shuning uchun bir muncha vaqt o'tgach element rux-simobga aylanadi. Elektr qo'zg'atuvchi kuch ko'mir o'rniga sof simobdan foydalanishdan o'zgarmaydi; u Leclanche elementiga qaraganda bir oz kattaroq, ichki qarshilik katta. Telegraflar uchun va umuman, intervalgacha oqim harakati uchun javob beradi. Ushbu elementlar tibbiy maqsadlarda ham qo'llaniladi va ular simob sulfat oksidi (HgSO 4) bilan zaryadlashni afzal ko'radilar. Tibbiy va boshqa maqsadlar uchun qulay bo'lgan ushbu elementning shakli shoxli kauchukdan yasalgan baland silindr bo'lib, uning yuqori yarmida sink va ko'mir, pastki yarmida esa suv va simob sulfat mavjud. Agar element teskari burilsa, u harakat qiladi, lekin birinchi holatda u oqim hosil qilmaydi. Uorren Delaru elementi- sink-kumush. Pergament qog'oz naychasiga joylashtirilgan eritilgan kumush xlorid (AgCl) silindridan tor kumush chiziq chiqib turadi; sink yupqa tayoqcha shakliga ega. Ikkala metal ham kerosin tiqin bilan yopilgan shisha naychaga joylashtiriladi. Suyuq ammiak eritmasi (1 litr suv uchun 23 qism tuz). Elektr qo'zg'alish kuchi Doniyor elementidagi kabi deyarli bir xil (bir oz ko'proq). Kumush metall kumush xloriddan elementning kumush chizig'iga to'planadi va qutblanish sodir bo'lmaydi. Ulardan tayyorlangan akkumulyatorlar yorug'likning kam uchraydigan gazlarda o'tishi bo'yicha tajribalar uchun ishlatilgan (V, Uorren Delarue). Geff bu elementlarga ularni tashish uchun qulay bo'lgan qurilma berdi; tibbiy indüksiyon bobinlari va to'g'ridan-to'g'ri oqimlar uchun ishlatiladi. Duchaumin, Partz, Figier elementlari. Birinchisi - sink-uglerod; stol tuzining zaif eritmasida sink, ko'mir - temir xlorid eritmasida. Beqaror va ozgina o'rganilgan. Partz sinkni temir bilan almashtirdi; osh tuzi eritmasi zichligi 1,15, temir xlorid eritmasi 1,26 zichlikka ega. Elektr qo'zg'atuvchi kuch kamroq bo'lsa-da, avvalgisidan yaxshiroq. Figier temir sulfatning to'yingan eritmasi orqali xlor oqimini o'tkazish orqali olingan temir-ko'mir elementida bitta suyuqlikdan foydalanadi. Nyode elementi, uglerod-sink. Rux oqartirgich bilan qoplangan koks plitasini o'z ichiga olgan gözenekli loy tsilindrni o'rab turgan silindrga o'xshaydi. Element mum bilan to'ldirilgan tiqin bilan yopiladi; undagi teshikdan osh tuzining eritmasi (100 qism suv uchun 24 qism) quyiladi. Elektr qo'zg'atuvchi kuch katta; tashqi kichik qarshilikka doimiy, biroz uzoq davom etadigan ta'sir bilan u tez orada zaiflashadi, lekin elementning bir yoki ikki soat harakatsizligidan keyin u avvalgi qiymatiga etadi. Quruq elementlar. Bu nom elementning g'ovakli jismlariga so'rilganda suyuqlik mavjudligi ko'rinmaydigan elementlarga berilishi mumkin; ularni chaqirish yaxshiroqdir nam. Ular orasida yuqorida tavsiflangan mis-sink Trouvé elementi va Germain tomonidan o'zgartirilgan Leclanche elementi mavjud. Bu ikkinchisi hindiston yong'og'idan olingan toladan foydalanadi; undan suyuqlik va gazlarni kuchli singdiradigan, quruq ko'rinadigan va bosim ostida faqat nam ko'rinishga ega bo'lgan massa tayyorlanadi. Oson portativ va sayohat telegraf va telefon stantsiyalari uchun mos. Gipsni o'z ichiga olgan Gasner elementlari (uglerod-sink), ehtimol sink xlorid yoki ammiak bilan singdirilgan (sir saqlanadi). Qo'zg'atuvchi kuch Leclanche elementida bo'lgani kabi, ikkinchisining harakati boshlanganidan biroz vaqt o'tgach; ichki qarshilik Leclanchenikidan kamroq. Quruq Leclanche-Barbier kamerasida marganets peroksidini o'z ichiga olgan tashqi rux tsilindri va aglomeratning ichki ichi bo'sh tsilindri orasidagi bo'shliq noma'lum tarkibdagi to'yingan eritma gips bilan to'ldiriladi. Ushbu elementlarning birinchi, ancha uzoq sinovlari ular uchun qulay edi. Jelatin-glitserin elementi Kuznetsova mis-sink bor; tubi ichi va tashqarisi qalay bilan qoplangan, kerosinga namlangan karton qutidan iborat. Qalayga maydalangan mis sulfat qatlami quyiladi, uning ustiga sulfat kislotasi bo'lgan jelatin-gliserin massasi quyiladi. Bu massa qattiqlashganda, ezilgan amalgamlangan sink qatlami quyiladi, yana bir xil massa bilan to'ldiriladi. Ushbu elementlar voltaik ustun kabi batareyani tashkil qiladi. Qo'ng'iroqlar, telegraflar va telefonlar uchun mo'ljallangan. Umuman olganda, turli xil quruq elementlarning soni juda muhim; lekin ko'pchilikda suyuqliklar va aglomeratlarning yashirin tarkibi tufayli ular haqida mulohaza yuritish faqat amaliy, ammo ilmiy emas. Katta sirt va past qarshilik elementlari. Qisqa, ancha qalin simlar yoki plitalarning porlashi kerak bo'lgan hollarda, masalan, ba'zi jarrohlik operatsiyalari paytida (qarang Galvanokaustika) suyuqlikka botirilgan katta metall yuzalarga ega bo'lgan elementlar ishlatiladi, bu ichki qarshilikni kamaytiradi va shu bilan birga oshiradi. joriy. Vollastonning sirtni ikki barobarga oshirish usuli shaklda ko'rsatilganidek, ko'p sonli plitalardan yuzalar tarkibiga qo'llaniladi. 2, qayerda y, y, y- bir xil metallning plitalari plitalar orasidagi bo'shliqlarga joylashtiriladi ts, ts, ts, ts boshqa metall. Barcha plitalar bir-biriga parallel va tegmaydi, lekin bir xil nomdagi barcha tashqi simlar bilan bir butunga ulanadi. Bu butun tizim ikkita plastinkaning bir xil elementi bo'lib, ularning har biri olti marta ko'rsatilgan sirt maydoniga ega, plitalar orasidagi suyuqlik qatlamining qalinligi chizmada ko'rsatilgan har ikki plastinka orasidagi masofaga teng. Ushbu asrning boshida (1822) katta metall yuzasiga ega qurilmalar qurilgan. Bularga deflagrator deb ataladigan katta Gare elementi kiradi. Sink va mis plitalar uzun uzunlik, flanel yoki yog'och tayoq bilan ajratilgan, rulonga o'raladi, unda choyshablar bir-biri bilan metall aloqada bo'lmaydi. Ushbu rolik suyuqlikli vannaga botiriladi va juda kichik tashqi qarshilikka ta'sir qilganda juda yuqori oqim hosil qiladi. Har bir varaqning yuzasi taxminan 50 kvadrat metrni tashkil qiladi. fut (4 kvadrat metr). Hozirgi vaqtda, umuman olganda, ular elementlarning ichki qarshiligini kamaytirishga harakat qilishadi, lekin ba'zi bir ilovalar uchun, masalan, og'riqli o'simtalarni issiq sim yoki plastinka bilan kesish uchun jarrohlikda, kuydirish uchun ularga ayniqsa katta sirt beradilar (qarang. Galvanokustika. ). Past qarshilikka ega o'tkazgichlar qizdirilganligi sababli, ichki qarshilikni kamaytirish orqali tokni aniq olish mumkin. Shuning uchun galvanokatik elementlarda ular joylashadilar katta raqam plitalar rasmda ko'rsatilgandek joylashtirilgan. 2 ta matn. Qurilma hech qanday maxsus xususiyatlarni taqdim etmaydi, lekin qulay foydalanish uchun moslashtirilgan; masalan, uglerod-sink xujayralari yoki Parij, Lion, Monpelye va Bryusselda ishlatiladigan xrom suyuqlikli Chardin batareyalari. Operatorlar ishlamasdan oldin batareyaning yaxshi holatda bo'lishini ta'minlash uchun juda past qarshilikli oqim o'lchagichni (ampermetr yoki ampermetr) ishlatish zarurligi haqida ogohlantirishi kerak. Oddiy elementlar elektr qo'zg'atuvchi kuchlarni bir-biri bilan solishtirganda normal o'lchov birligi bo'lib xizmat qilish uchun ular ochiq turganda iloji boricha uzoq vaqt davomida o'zlarining elektr qo'zg'atuvchi kuchlarini saqlab qolishlari yoki doimiy potentsial farqiga ega bo'lishlari kerak. Shu maqsadda Rainier mis-sink juftligini taklif qildi, unda misning yuzasi sinkga nisbatan juda katta. Suyuqlik 1000 qism suvda 200 qism quruq osh tuzining eritmasi. Bunday holatda, misning polarizatsiyasi, agar bu element yuqori qarshilikka ega bo'lgan kontaktlarning zanglashiga olib kirilishi va qisqa vaqt ichida bo'lsa, juda zaifdir. Oddiy element Latimer Klark rux sulfat, simob va simob sulfid tuzi (Hg 2 SO 4) eritmasidagi ruxdan iborat. Oddiy element Fleming, mis-sink, mis sulfat va sink sulfat eritmalari bilan ma'lum, har doim doimiy zichlik. Oddiy element London pochta va telegraf idorasi, mis-sink, sink sulfat eritmasi va mis bilan mis sulfat kristallari bilan juda mos keladi. Fleming elementining elektr qo'zg'atuvchi kuchi uchun maqolaning oxiridagi plastinkaga qarang. Ikkilamchi elementlar, yoki batareyalar, 50 yil davomida alohida e'tibor berilmagan Ritterning ikkilamchi ustunlaridan kelib chiqqan (qarang Galvanizm). Ba'zi suyuqlikka botirilgan mis plitalardan tashkil topgan Ritter ustuni voltaik ustunning ta'siridan keyin qutblangan bo'lib, shundan so'ng uning o'zi birlamchi oqimga qarama-qarshi bo'lgan oqim hosil qilishi mumkin edi. 1859 yilda Plante ikkita qo'rg'oshin varaqdan iborat bo'lgan, Gare deflagratori kabi spiral shaklida o'ralgan, o'zaro metall aloqasiz va zaif sulfat kislotaga botirilgan elementni qurdi. Bir qo'rg'oshin varag'ini anodga (musbat qutb), ikkinchisini esa ketma-ket ulangan kamida 2 ta Bunsen yoki Poggendorff xujayrasi batareyasining katodiga ulash va shu bilan suyuqlikda oqayotgan oqimni qo'rg'oshindan qo'rg'oshinga o'tkazish orqali qo'rg'oshin plastinkasida kislorodning ajralishi , anodga ulangan va vodorod katodga ulangan varaqda. Anod plastinkasida qo'rg'oshin peroksid qatlami hosil bo'ladi, katod plitasi esa oksidlardan butunlay tozalanadi. Plitalarning heterojenligi tufayli ular oldingisiga qarama-qarshi yo'nalishda oqim berib, katta elektr qo'zg'atuvchi kuchga ega bo'lgan juftliklar hosil qiladi. Ikkilamchi elementda rivojlanayotgan va birlamchi batareyaning qo'zg'atuvchi kuchiga qarama-qarshi yo'naltirilgan katta qo'zg'atuvchi kuch, ikkinchisining birinchisidan oshib ketishi talabining sababidir. Ketma-ket ulangan ikkita Poggendorff elementi taxminan 4 voltlik hayajonli kuchga ega, ammo Plante elementi atigi 2 1/2 ni tashkil qiladi. Zaryadlash uchun 3 yoki 4 ta Plante hujayralari parallel ulangan (qarang. Galvanik batareyalar), aslida, oldingi 2 ta Poggendorff elementi etarli bo'lar edi, lekin ularning harakati qo'rg'oshinning bunday katta sirtini oksidlash uchun juda sekin bo'ladi; shuning uchun, masalan, parallel ravishda ulangan 12 Plante elementini bir vaqtning o'zida zaryad qilish uchun sizga bir necha soat davomida 6-8 voltlik hayajonli kuchga ega 3-4 Bunsen elementining ta'siri kerak bo'ladi. Zaryadlangan Plante xujayralari ketma-ket ulangan 24 voltlik elektr qo'zg'alish kuchini rivojlantiradi va masalan, zaryadlovchi batareyaga qaraganda ko'proq akkor hosil qiladi, ammo ikkilamchi batareyaning ta'siri qisqaroq bo'ladi. Ikkilamchi akkumulyator tomonidan harakatga keltiriladigan elektr quvvati miqdori birlamchi akkumulyatordan u orqali o'tadigan elektr energiyasi miqdoridan ko'p emas, lekin tashqi o'tkazgichlar orqali kattaroq kuchlanish yoki potentsial farq bilan o'tib, qisqa vaqt ichida sarflanadi. O'simlik hujayralari, turli amaliy takomillashtirishdan so'ng, batareyalar deb ataldi. 1880 yilda For qo'rg'oshin plitalarini qizil qo'rg'oshin qatlami, ya'ni tayyor qo'rg'oshin oksidi bilan qoplash g'oyasini ilgari surdi, u birlamchi oqim ta'sirida yana bir plastinkada oksidlanadi va oksidisizlanadi. boshqa. Ammo qizil qo'rg'oshinni ulash usuli texnik yaxshilanishlarni talab qildi, bu asosan qo'rg'oshin panjarasidan foydalanishdan iborat bo'lib, unda bo'sh hujayralar qizil qo'rg'oshin va zaif sulfat kislotada litharj sinovi bilan to'ldiriladi. Fitz-Jerald batareyasi hech qanday metall asossiz qo'rg'oshin oksidli plitkalardan foydalanadi; Umuman olganda, batareya tizimlari juda ko'p va bu erda faqat eng yaxshilaridan birining tasviri (jadvalning 8-rasm). Hagen qo'rg'oshin panjarasi bir-biriga qaragan ikkita o'simtadan iborat bo'lib, qo'rg'oshin oksidi bo'laklarining ramkadan tushishiga yo'l qo'ymaydi; chiziqlar bo'ylab maxsus tasvirlangan kesmalar ab Va CD Asosiy chizma ushbu ramkaning tuzilishini tushuntiradi. Bir ramka qizil qo'rg'oshin bilan, ikkinchisi litarj bilan to'ldirilgan (qo'rg'oshinning eng past oksidlanish darajasi). Toq raqam, odatda besh yoki etti, plitalar shaytonda tushuntirilganidek bir xil tarzda bog'langan. 2; birinchi holatda 3 ta, ikkinchisida 4 ta litarj bilan qoplangan. Rus texniklaridan Yablochkov va Xotinskiy batareyalar dizaynidan foyda ko'rdilar. Bir texnik noqulaylikni ifodalovchi bu ikkilamchi elementlar juda og'ir vazn, xilma-xillikni oldi texnik ilovalar, Aytgancha, bu maqsadda dinamolardan to'g'ridan-to'g'ri oqimdan foydalanish mumkin bo'lmagan hollarda uyning elektr yoritilishiga. Bir joyda zaryadlangan batareyalar boshqa joyga ko'chirilishi mumkin. Endi ular asosiy elementlar bilan emas, balki ba'zi maxsus qoidalarga muvofiq dinamolar bilan zaryadlangan (qarang: Dinamolar, Elektr yoritish). Galvanik batareyalarning tarkibi. Batareya uchta usulda elementlardan iborat: 1) ketma-ket ulanish, 2) parallel ulanish, 3) oldingi ikkalasidan birlashtirilgan. Shaklda. 1-jadvalda 3 ta Daniel elementining ketma-ket ulanishi ko'rsatilgan: o'ngdan hisoblangan birinchi juftning sinki ulangan. mis lenta ikkinchi juft mis bilan, ikkinchi juft sink bilan - uchinchi mis bilan. Birinchi juftlik misining bo'sh uchi anod yoki batareyaning musbat terminali; uchinchi juftlikning erkin uchi katod yoki batareyaning salbiy terminalidir. Xuddi shu elementlarni parallel ravishda ulash uchun barcha sinklarni bir-biriga metall lentalar bilan ulash va barcha mis plitalarni lenta yoki simlar bilan sinkdan alohida bir butunga ulash kerak; murakkab rux yuzasi katod, murakkab mis yuzasi anod bo'ladi. Bunday batareyaning harakati bitta hujayraning harakati bilan bir xil bo'lib, uning sirt maydoni batareyaning bitta hujayrasidan uch baravar kattaroq bo'ladi. Nihoyat, uchinchi ulanish usuli kamida 4 ta elementga qo'llanilishi mumkin. Ularning ikkitasini parallel ravishda ulash orqali biz ikkita murakkab anodni va bir xil ikkita katodni olamiz; Birinchi kompleks anodni ikkinchi kompleks katod bilan bog'lab, biz ikki elementli ikkita sirtli batareyani olamiz. Jin bo'lsin. Ikki xil tasvirlangan 3 ta matn murakkab birikmalar 8 ta elementdan iborat bo'lib, ularning har biri qora bo'shliqlar bilan ajratilgan ikkita konsentrik halqa bilan ifodalanadi. Tafsilotlarga kirmasdan, shuni ta'kidlaymizki, shunga ko'ra ko'rinish ushbu batareyalarni yaratish usuli yuqorida tavsiflanganlardan farq qiladi. (I) da 4 ta element ketma-ket ulangan, lekin bir uchida ikkita tashqi rux metall chiziq bilan bog'langan. KK, qarama-qarshi tomonda esa ikkita tashqi mis plitalar plastinka bilan bog'langan AA, bu anod, holbuki QC -
ketma-ket ulangan ikki qavatli sirtning 4 ta elementiga teng bo'lgan murakkab batareyaning katodi. 3-chizma (II) ketma-ket ulangan to'rtta sirtning ikkita elementiga ekvivalent batareyani ko'rsatadi. Muayyan tarzda tuzilgan batareyalar zarur bo'lgan holatlar Ohm formulasi (galvanik tok) bilan to'liq aniqlangan, undan kelib chiqadigan qoidaga ko'ra, olish uchun eng yaxshi harakat Ma'lum miqdordagi galvanik elementlarga ega bo'lgan har qanday o'tkazgich uchun ulardan batareyani shunday qurish kerakki, uning ichki qarshiligi tashqi o'tkazgichning qarshiligiga teng yoki hech bo'lmaganda unga iloji boricha yaqinroq bo'ladi. Bunga qo'shimcha qilishimiz kerakki, ketma-ket ulanish bilan ichki qarshilik ulangan juftliklar soniga mutanosib ravishda ortadi va parallel ulanish bilan, aksincha, qarshilik bu raqamga mutanosib ravishda kamayadi. Shuning uchun, galvanik oqimga katta qarshilik ko'rsatadigan telegraf liniyalarida batareyalar ketma-ket ulangan elementlardan iborat; jarrohlik operatsiyalarida (galvanokustika) parallel ulangan elementlarning batareyasi kerak. Do'zaxda tasvirlangan. 3 (I) batareya ifodalaydi eng yaxshi ulanish 8 ta element tashqi qarshilikka ta'sir qiladi, bu bitta elementning ichki qarshiligidan ikki baravar ko'p. Agar tashqi qarshilik birinchi holatdan to'rt baravar kam bo'lsa, unda batareyaga do'zaxning ko'rinishi berilishi kerak. 3 (II). Bu Ohm formulasi yordamida hisob-kitoblardan kelib chiqadi. [Elementlar va batareyalar haqida Niodet ishiga qarang (D. Golovning rus tilidagi tarjimasida - " Elektr elementlari" 1891); batafsilroq: "Die galvanischen Batterien", Hauck, 1883. "Elektr energiyasi" jurnalidagi maqolalar, 1891 va 1892] Galvanik hujayralarni solishtirish o'zaro. Bu bilan bog'liq eslatmalar qisman elementlarning tavsifida berilgan. Galvanik elementning qadr-qimmati u ishlab chiqaradigan oqimning kuchi va uning ta'sir qilish muddati, ya'ni birinchi miqdorning ikkinchisining mahsuloti bilan o'lchanadi. Agar oqim birligi sifatida amperni (qarang Galvanik tok ), vaqt birligi sifatida soatni olsak, u holda galvanik elementning ishlashini amper-soatlarda o'lchashimiz mumkin. Masalan, batareyalar hajmiga qarab, 40 dan 90 amper-soatgacha bo'lgan quvvatni ta'minlashi mumkin. Bug 'otining bir soatlik ishiga teng keladigan elektr toki bilan etkazilgan ishni o'lchash usullari uchun qarang: Ish, elektr tokining energiyasi.


Galvanik hujayra
Daniel-Yakobi galvanik elementining diagrammasi
Galvanik element- ikkita metalning va (yoki) ularning oksidlarining elektrolitdagi o'zaro ta'siriga asoslanib, yopiq zanjirda elektr tokining paydo bo'lishiga olib keladi. Luidji Galvani sharafiga nomlangan.
Turli metallar bilan aloqa qilganda elektr tokining paydo bo'lishi fenomeni italiyalik fiziolog, Boloniya universiteti tibbiyot professori Luidji Galvani tomonidan 1786 yilda kashf etilgan. Galvani po'lat skalpel bilan teginganda, mis ilgaklarga biriktirilgan yangi ajratilgan qurbaqaning orqa oyoqlari mushaklarining qisqarishini tasvirlab berdi. Kuzatishlar kashfiyotchi tomonidan "hayvon elektr energiyasi" ning namoyon bo'lishi sifatida talqin qilingan.
Elektrokimyoviy generatorlar (yoqilg'i xujayralari)- bular kimyoviy energiyaning elektr energiyasiga aylanishi sodir bo'lgan elementlardir. Oksidlovchi va qaytaruvchi vosita hujayradan tashqarida saqlanadi va ish paytida elektrodlarga doimiy va alohida etkazib beriladi. Yoqilg'i xujayrasining ishlashi paytida elektrodlar iste'mol qilinmaydi. Qaytaruvchi vosita vodorod (H 2), metanol (CH 3 OH), metan (CH 4) suyuq yoki gazsimon holatda. Oksidlovchi vosita odatda havo kislorodi yoki sof kisloroddir. Kislorod-vodorodda yonilg'i xujayrasi Ishqoriy elektrolit bilan kimyoviy energiya elektr energiyasiga aylanadi. Elektr stantsiyalari kosmik kemalarda ishlatiladi, ular kosmik kemalar va kosmonavtlarni energiya bilan ta'minlaydi;
Ilova
- Batareyalar signalizatsiya tizimlari, chiroqlar, soatlar, kalkulyatorlar, audio tizimlar, o'yinchoqlar, radiolar, avtotexnika, masofadan boshqarish pultlarida qo'llaniladi.
- Batareyalar avtomobil dvigatellarini ishga tushirish uchun foydalaniladi, shuningdek, ularni aholi punktlaridan uzoqda joylashgan joylarda elektr energiyasining vaqtinchalik manbalari sifatida ishlatish mumkin;
- Yoqilg'i xujayralari elektr energiyasini ishlab chiqarishda ishlatiladi (uchun elektr stantsiyalari), favqulodda energiya manbalari, avtonom elektr ta'minoti, transport, bort elektr ta'minoti, mobil qurilmalar.
Shuningdek qarang
Adabiyot
- Axmetov N.S. Umumiy va noorganik kimyo
- Aksenovich L.A. Fizika o'rta maktab: Nazariya. Topshiriqlar.
Havolalar
| Galvanik hujayra | Galvanik hujayra Daniel | Ishqoriy element | | Quruq element | Konsentratsiya elementi | Rux havo elementi | Weston oddiy elementi |
|---|---|
| Elektr batareyalari | Qo'rg'oshin kislotasi | Kumush-rux | Nikel-kadmiy | Nikel metall gidrid | Nikel-sink batareya | Litiy-ion | Litiy polimer | Litiy temir sulfid | Litiy temir fosfat | Lityum titanat | Vanadiy | Temir-nikel |
| Yoqilg'i xujayralari | Bevosita metanol | Qattiq oksid | Ishqoriy |
| Modellar | Batareya | Elektr batareya | Yoqilg'i xujayrasi |
| Qurilma | Anod | Katod | Elektrolit |
1. Galvanik element
Galvanik element Luidji Galvani nomi bilan atalgan elektr tokining kimyoviy manbai. Galvanik elementning ishlash printsipi ikkita metallning elektrolitlar orqali o'zaro ta'siriga asoslangan bo'lib, yopiq zanjirda elektr tokining paydo bo'lishiga olib keladi. Galvanik hujayraning emfsi elektrodlarning materialiga va elektrolitlar tarkibiga bog'liq. Bular birlamchi CITlar bo'lib, ularda yuzaga keladigan reaktsiyalarning qaytarilmasligi tufayli ularni qayta zaryadlab bo'lmaydi.
Galvanik hujayralar elektr energiyasining bir martalik manbalaridir. Reagentlar (oksidlovchi va qaytaruvchi) to'g'ridan-to'g'ri galvanik elementning tarkibiga kiradi va uning ishlashi davomida iste'mol qilinadi. Galvanik hujayra tashqi kontaktlarning zanglashiga olib keladigan emf, kuchlanish, quvvat, quvvat va energiya, shuningdek, saqlanishi va ekologik xavfsizligi bilan tavsiflanadi.
EMF galvanik elementda sodir bo'ladigan jarayonlarning tabiati bilan belgilanadi. Galvanik hujayraning kuchlanishi U elektrodlarning qutblanishi va qarshilik yo'qotishlari tufayli har doim uning EMF dan past bo'ladi:
U = EE – I(r1–r2) – DE,
bu erda Ee - elementning EMF; I - elementning ish rejimidagi oqim kuchi; r1 va r2 - galvanik element ichidagi birinchi va ikkinchi turdagi o'tkazgichlarning qarshiligi; DE - galvanik elementning polarizatsiyasi, uning elektrodlari (anod va katod) qutblanishlaridan iborat. Polarizatsiya i = I / S formulasi bo'yicha aniqlangan oqim zichligi (i) ortishi bilan ortadi, bu erda S - elektrodning tasavvurlar maydoni va tizim qarshiligini oshiradi.
Galvanik elementning ishlashi davomida uning EMF va shunga mos ravishda kuchlanish reagentlar kontsentratsiyasining pasayishi va elektrodlardagi oksidlanish-qaytarilish jarayonlari mahsulotlari kontsentratsiyasining oshishi tufayli asta-sekin pasayadi (Nernst tenglamasini eslang). Shu bilan birga, galvanik elementning zaryadsizlanishi vaqtida kuchlanish qanchalik sekin pasaysa, uni amalda qo'llash imkoniyatlari shunchalik katta bo'ladi. Elementning sig'imi - galvanik element ish paytida (bo'shatish paytida) etkazib berishga qodir bo'lgan Q elektr energiyasining umumiy miqdori. Imkoniyat galvanik kamerada saqlanadigan reagentlar massasi va ularning konversiya darajasi bilan aniqlanadi. Chiqarish oqimining oshishi va elementning ish haroratining pasayishi bilan, ayniqsa 00C dan past bo'lsa, reagentlarning konversiya darajasi va elementning sig'imi pasayadi.
Galvanik elementning energiyasi uning sig'imi va kuchlanishining ko'paytmasiga teng: DN = Q.U. EMF qiymati yuqori bo'lgan elementlar, past massa va yuqori daraja reagentlarning transformatsiyasi.
Saqlash qobiliyati - bu elementni saqlash muddatining uzunligi, uning xususiyatlari belgilangan parametrlar doirasida qoladi. Elementni saqlash va ishlatish harorati oshishi bilan uning saqlash muddati kamayadi.
Galvanik elementning tarkibi: ko'chma galvanik hujayralardagi qaytaruvchi moddalar (anodlar), qoida tariqasida, sink Zn, litiy Li, magniy Mg; oksidlovchi moddalar (katodlar) - marganets MnO2, mis CuO, kumush Ag2O, oltingugurt SO2 oksidlari, shuningdek CuCl2, PbCl2, FeS va kislorod O2 tuzlari.
Dunyoda eng keng tarqalgan ishlab chiqarish Mn-Zn marganets-rux elementlarini ishlab chiqarish bo'lib qolmoqda, ular radio jihozlari, aloqa asboblari, magnitafonlar, chiroqlar va boshqalarni quvvatlantirish uchun keng qo'llaniladi. Bunday galvanik hujayraning dizayni rasmda ko'rsatilgan.
Ushbu elementda tok hosil qiluvchi reaktsiyalar:
Anodda (–): Zn – 2ē → Zn2+ (amalda element tanasining rux qobig'i asta-sekin eriydi);
Katodda (+): 2MnO2 + 2NH4+ + 2ē → Mn2O3 + 2NH3 + H2O.
Elektrolitik fazoda quyidagi jarayonlar ham sodir bo'ladi:
Anodda Zn2+ + 2NH3 →2+;
Mn2O3 + H2O katodida → yoki 2.
Molekulyar shaklda galvanik hujayraning kimyoviy tomoni umumiy reaktsiya bilan ifodalanishi mumkin:
Zn + 2MnO2 + 2NH4Cl → Cl2 + 2.
Galvanik hujayra diagrammasi:
(–) Zn|Zn(NH3)2]2+|||MnO2 (C) (+).
Bunday tizimning EMF E = 1,25 ÷ 1,50V ga teng.
Ishqoriy elektrolitdagi (KOH) reagentlarning o'xshash tarkibiga ega bo'lgan galvanik hujayralar yaxshiroq chiqish ko'rsatkichlariga ega, ammo ular qo'llanilmaydi. portativ qurilmalar ekologik xavflar tufayli. Ag-Zn kumush-sink xujayralari yanada foydali xususiyatlarga ega, ammo ular juda qimmat va shuning uchun iqtisodiy jihatdan samarali emas. Hozirgi vaqtda odatda "quruq batareyalar" deb ataladigan 40 dan ortiq turli xil portativ galvanik hujayralar ma'lum.
2. Elektr batareyalari
Elektr batareyalari (ikkilamchi HIT) qayta zaryadlanuvchi galvanik hujayralar bo'lib, ular tashqi oqim manbai ( zaryadlovchi) qayta zaryadlash mumkin.
Batareyalar - bu tashqi oqim manbai ta'sirida tizim to'planadigan (to'planadigan) qurilmalar. kimyoviy energiya(batareyani zaryad qilish jarayoni), so'ngra qurilma ishlaganda (zaryad qilish) kimyoviy energiya yana elektr energiyasiga aylanadi. Shunday qilib, zaryad olayotganda akkumulyator elektrolizator vazifasini bajaradi, zaryadsizlanayotganda esa galvanik hujayra vazifasini bajaradi.
Soddalashtirilgan shaklda akkumulyator ikkita elektroddan (anod va katod) va ular orasidagi ionli o'tkazgichdan - elektrolitdan iborat. Oksidlanish reaksiyalari anodda zaryadsizlanish vaqtida ham, zaryadlash vaqtida ham, katodda esa qaytarilish reaktsiyalari sodir bo'ladi.
Yaqin vaqtgacha kislotali qo'rg'oshin va gidroksidi nikel-kadmiy va nikel-temir batareyalari Rossiyada va hatto Dnestryanıda eng keng tarqalgan bo'lib qoldi.

Undagi elektrodlar qo'rg'oshin panjaralari bo'lib, ulardan biri qo'rg'oshin oksidi IV kukuni - PbO2 bilan teshiklarga to'ldirilgan. Elektrodlar elektrolitga g'ovakli ajratgich orqali ulanadi. Butun batareya ebonit yoki polipropilendan tayyorlangan tankga joylashtiriladi.
Bunday qurilma ishlaganda, unda quyidagi elektrod jarayonlari sodir bo'ladi:
A). Elektr energiyasi manbai sifatida batareyaning zaryadsizlanishi yoki ishlashi.
Anodda: (–) Pb – 2ē → Pb2+;
katodda: (+) PbO2 + 4H+ + 2ē → Pb2+ + 2H2O.
Elektrodlarda hosil bo'lgan qo'rg'oshin kationlari elektrolit anionlari bilan o'zaro ta'sirlanib, oq qo'rg'oshin sulfat cho'kmasini chiqaradi.
Pb2+ + SO42– = ↓PbSO4.
Batareyani tushirish jarayonining umumiy oqim hosil qiluvchi reaktsiyasi:
Pb + PbO2 + 2H2SO4 = 2PbSO4↓ + 2H2O,
va galvanik element sifatida ishlaydigan batareyaning sxemasi (-) Pb|PbSO4||PbO2 (+) ko'rinishga ega.
Ishlayotgan akkumulyator terminallaridagi kuchlanish 2,0÷2,5V ga etadi. Qurilmaning ishlashi paytida elektrolitlar iste'mol qilinadi va tizimda cho'kma to'planadi. Faol vodorod ionlarining kontsentratsiyasi [H+] katoddagi reaktsiya uchun muhim bo'lganida, batareya ishlashni to'xtatadi.
B). Batareyaning kimyoviy potentsialini keyinchalik aylantirish uchun zaryadlash yoki tiklash elektr energiyasi. Buning uchun batareya tashqi oqim manbaiga shunday ulanadiki, salbiy qutb "anod" terminaliga, musbat qutb esa "katod" terminaliga beriladi. Bunday holda, tashqi kuchlanish ta'sirida elektrodlarda teskari jarayonlar sodir bo'lib, ularni asl holatiga qaytaradi.
Metall qo'rg'oshin elektrod sirtini tiklaydi (–): PbSO4 + 2ē → Pb + SO42;
Olingan qo'rg'oshin oksidi IV qo'rg'oshin panjarasining teshiklarini to'ldiradi (+): PbSO4 + 2H2O – 2ē → ↓PbO2 + 4H+ + SO42.
Umumiy qaytarilish reaksiyasi: 2PbSO4 + 2H2O = Pb + PbO2 + 2H2SO4.
Batareyani zaryadlash jarayoni tugashini uning terminallari ustidagi gaz pufakchalari ("qaynatish") bilan aniqlashingiz mumkin. Bu elektrolitlar kamayishi paytida vodorod kationlarini pasaytirishning yon jarayonlari va kuchlanish kuchayishi bilan suvning oksidlanishi bilan bog'liq:
2N+ + 2ē → N2; 2H2O – 4ē → O2 + 2H2.
Batareya samaradorligi 80% va ish kuchlanishiga etadi uzoq vaqt ma’nosini saqlab qoladi.
Batareyaning EMFni tenglama yordamida hisoblash mumkin:
RT a4(H+) a2(SO42–)
EE = EE0 + –––– ℓn ––––––––––––––– (Komp.
2F a2(H2O) hisobga olinadi).
Shuni ta'kidlash kerakki, konsentrlangan sulfat kislota (ō(H2SO4) > 30%) batareyada ishlatilmaydi, chunki shu bilan birga, uning elektr o'tkazuvchanligi pasayadi va metall qo'rg'oshinning eruvchanligi ortadi. Qo'rg'oshin kislotali akkumulyatorlar keng qo'llaniladi avtomobil transporti barcha turdagi, telefon va elektr stantsiyalarida. Biroq, qo'rg'oshin va uning mahsulotlarining yuqori toksikligi tufayli, qo'rg'oshin kislotali batareyalar germetik muhrlangan qadoqlash va ularning ishlash jarayonlarini to'liq avtomatlashtirishni talab qiladi.
A) Ishqoriy akkumulyatorlarda musbat elektrod gelsimon nikel gidroksidi II Ni(OH)2 bilan singdirilgan nikel panjarasidan yasaladi; va salbiy - kadmiy yoki temirdan. Ion o'tkazgich kaliy gidroksid KOH ning 20% li eritmasidir. Bunday akkumulyatorlarda tok hosil qiluvchi va hosil qiluvchi umumiy reaksiyalar quyidagi shaklga ega:
2NiOOH + Cd + 2H2O ◄====== 2Ni(OH)2 + Cd(OH)2; EE0 = 1,45V.
2NiOOH + Fe + 2H2O ◄====== 2Ni(OH)2 + Fe(OH)2; EE0 = 1,48V.
Ushbu akkumulyatorlarning afzalliklari orasida ularning uzoq xizmat qilish muddati (10 yilgacha) va yuqori mexanik kuch, kamchiliklar esa past samaradorlik va ish kuchlanishidir. Ishqoriy batareyalar elektromobillarni, yuk ko'taruvchilarni, tog'-kon elektrovozlarini, aloqa va elektron uskunalarni, radiostantsiyalarni quvvatlantirish uchun ishlatiladi. Shuni ham eslaylikki, kadmiy juda zaharli metall bo'lib, ishlatilgan qurilmalarni utilizatsiya qilishda xavfsizlik qoidalariga rioya qilishni talab qiladi.
EMF va oqim. Shuni esda tutish kerakki, batareyada bir xil xususiyatlarga ega elementlar bo'lishi kerak. Ish rejasi Ekvivalent sxemalarni chizing: Reostatni ulash sxemalari Potensiometrni ulash sxemalari Galvanik elementlarni ulash sxemalari. Xulosa Tuzilgan sxemalar va shartlardan har bir zanjirning o'ziga xos EMF qiymati bor, u boshqacha tarzda aniqlanadi. Javoblar...
19-20-asrlarda elektrokaplama texnologiyasining rivojlanishi. asosan ochiqligicha qolmoqda. Aftidan, uni galvanik ishlab chiqarishni yaratish jarayonini qayta qurish asosida hal qilish mumkin; fan va texnikaning qaysi sohalari, ularning o'ziga xos yutuqlari, uning shakllanishiga qarzdorligini kuzatish; elektrokaplama texnologiyasining paydo bo'lishi va rivojlanishi uchun ijtimoiy-iqtisodiy shart-sharoitlarni hisobga olish. ...
Oqim galvanostegiyaga qaraganda past; temir galvanoplastik vannalarda u 10-30 a / m2 dan oshmaydi, temir qoplama (galvanik) paytida oqim zichligi 2000-4000 a / m2 ga etadi. Galvanik qoplamalar nozik kristalli tuzilishga ega bo'lishi kerak va qoplangan mahsulotlarning turli joylarida - o'simtalar va chuqurchalar bir xil qalinlikda bo'lishi kerak. Bu talab, ayniqsa, elektrokaplamada muhim ahamiyatga ega ...