Atomning massa soni qancha. Atom massasi
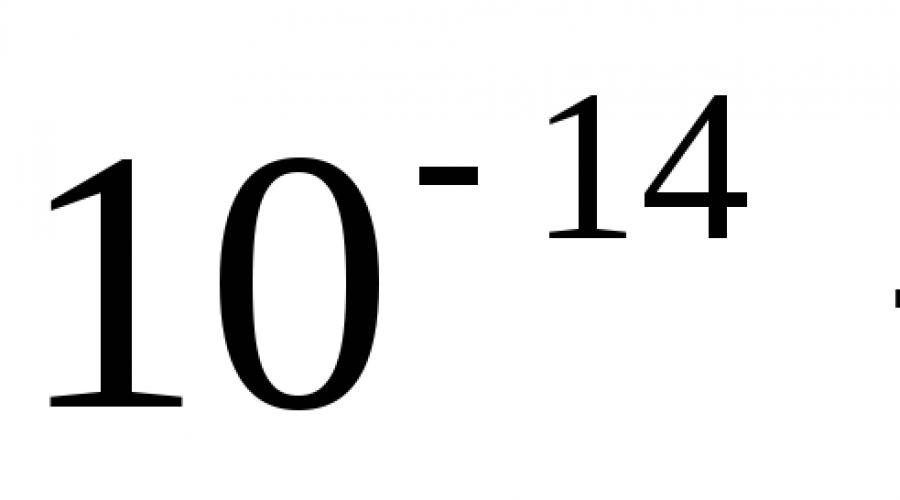
Shuningdek o'qing
") yadroda. Odatda harf bilan belgilanadi A. Massa soni atom massa birliklarida ifodalangan izotopning atom massasiga yaqin, lekin u faqat uglerod-12 uchun mos keladi, chunki atom massasi birligi (a.m.u.) endi 1 ⁄ 12 atom massasi sifatida aniqlanadi. 12 C. Boshqa barcha holatlarda atom massasi massa sonidan farqli o'laroq, butun son emas. Shunday qilib, 35 Cl xlor izotopining massa soni 35 ga, atom massasi esa 34,96885 amuga teng.
Muayyan nuklidni (atom yadrolarining turi) belgilashdagi massa soni yuqori chap indeks bilan yoziladi, masalan, 232 Th. Massa soni bir xil bo'lgan nuklidlar izobarlar deyiladi (masalan, 14 C va 14 N nuklidlari izobarlar).
Massa sonini bilish yadro va atomning massasini taxmin qilish imkonini beradi. Agar massa soni ma'lum bo'lsa, u holda massa M atom va uning yadrosi quyidagi munosabat asosida baholanadi M ≈ A m N, Qayerda m N ≈ 1,67·10 −27 kg - nuklon, ya'ni proton yoki neytronning massasi. Masalan, alyuminiy-27 atomi va uning yadrosida 27 ta nuklon (13 proton va 14 neytron) mavjud. Uning massasi taxminan 27·1,67·10−27 kg ≈ 4,5·10−26 kg. Agar yadroning massasini kattaroq aniqlik bilan olish zarur bo'lsa, yadrodagi nuklonlar yadro tortishish kuchlari bilan bog'langanligini hisobga olish kerak va shuning uchun munosabatlarga muvofiq. E=mc 2 yadroning massasi kamayadi. Yadro atrofidagi orbitalardagi elektronlarning umumiy massasi ham atom massasiga qo'shilishi kerak. Biroq, bu tuzatishlarning barchasi 1% dan oshmaydi.
| 238 92 U | → | 234 90 Th | + | 4 2 U |
chap tomonda boshlang'ich yadroning massa soni 238, reaksiyaning o'ng tomonida massa raqamlari 234 va 4 bo'lgan ikkita yadro joylashgan bo'lib, ular jami 238 tani beradi. Alfa massa raqamini hisobga olgan holda. zarracha (geliy-4 yadrosi) 4, alfa-parchalanish parchalanuvchi yadroning massa sonini 4 birlikka kamaytiradi. Beta-yemirilishning har qanday turlari (beta-minus yemirilish, pozitron yemirilishi, elektronni tutib olish, qoʻshaloq beta-yemirilishning barcha turlari) massa sonini oʻzgartirmaydi, chunki bu jarayonda yadroning faqat baʼzi nuklonlari bir turdan ikkinchi turga (protonlar) aylanadi. neytronlar yoki orqaga). Izomerik o'tish ham yadroning massa sonini o'zgartirmaydi.
Eslatmalar
Shuningdek qarang
Wikimedia fondi. 2010 yil.
Boshqa lug'atlarda "Ommaviy raqam" nima ekanligini ko'ring:
- (nuklonlar soni, A belgisi), umumiy soni ATOM YADROSIDAGI NUKLEONLAR (NEYTRON va PROTONLAR). Odatda elementning kimyoviy belgisidan oldin ustun belgisi sifatida yoziladi. Shunday qilib, eng yengil element vodorodning yadrosida faqat bitta proton bor va... ... Ilmiy va texnik ensiklopedik lug'at
Nuklonlarning umumiy soni (neytronlar va protonlar). yadro. Bir xil kimyoviy izotoplar uchun har xil. element. Jismoniy ensiklopedik lug'at. M .: Sovet Entsiklopediyasi. Bosh muharrir A. M. Proxorov. 1983. MASS RANGAR ... Jismoniy ensiklopediya
Atom yadrosidagi nuklonlar soni. Odatda belgining yuqori chap qismida ko'rsatiladi kimyoviy element(masalan, 10V)… Katta ensiklopedik lug'at
MASS NUMBER- atom yadrosidagi nuklonlarning (proton va neytronlarning) umumiy soni, masalan, A bilan belgilangan va tegishli element belgisining yuqori chap qismidagi indeks bilan ko'rsatilgan. 32S massa soni 32 (A = 32) bo'lgan oltingugurt izotopi degan ma'noni anglatadi. Izotopning qism raqami butunga teng...... ... Katta politexnika entsiklopediyasi
massa raqami- - [Ya.N.Luginskiy, M.S.Fezi Jilinskaya, Yu.S.Kabirov. Elektrotexnika va energetikaning inglizcha-ruscha lug'ati, Moskva] Elektrotexnika mavzulari, asosiy tushunchalar EN massa raqami ... Texnik tarjimon uchun qo'llanma
Atom yadrosidagi nuklonlar soni. Odatda kimyoviy element belgisining yuqori chap qismida ko'rsatiladi (masalan, 10B). * * * MASSA SONI MASS SONI, atom yadrosidagi nuklonlar soni. Odatda kimyoviy element belgisining yuqori chap qismida ko'rsatilgan... ... ensiklopedik lug'at
massa raqami- masės skaičius statusas T sritis Standartizacija ir metrologija apibrėžtis Atomo branduolio nukleonų skaičius. attikmenys: ingliz. massa soni; yadro raqami; nuklon soni vok. Massenzahl, f; Nukleonenzahl, f rus. massa soni, n; raqam…… Penkiakalbis aiškinamasis metrologijos terminų žodynas
massa raqami- masės skaičius statusas T sritis chemija apibrėžtis Atomo branduolio nukleonų skaičius. attikmenys: ingliz. massa raqami; yadro raqami; nuklon raqami rus. ommaviy raqam ... Chemijos terminų aiškinamasis žodynas
massa raqami- masės skaičius statusas T sritis fizika atitikmenys: ingliz. massa soni; yadro raqami; nuklon soni vok. Massenzahl, f; Massezahl, f; Nukleonenzahl, f rus. massa soni, n pranc. nombre de masse, m; nombre de nucléons, m … Fizikos terminų žodynas
Atom yadrosidagi nuklonlar (proton va neytronlar) soni; A harfi bilan belgilanadi va odatda element belgisining yuqori chap qismida ko'rsatiladi, masalan, 32S oltingugurtning A = 32 izotopi bilan ifodalanadi. M.p va yadroviy zaryad Z, elementar birliklarda ifodalanadi. Buyuk Sovet Entsiklopediyasi
Kitoblar
- Qobiliyatsiz menejer. Ommaviy jinnilik kabi qobiliyatsizlik, Adrian Farnham. Ajablanarlisi shundaki, qobiliyatsiz bo'lgan menejerlar qo'l ostida ishlaydi. Ayrim ekspertlarning fikricha, iqtisodiyotning ayrim tarmoqlarida layoqatsizlar soni...
Atom markazi uning massasining asosiy qismini va barcha musbat zaryadini o'z ichiga oladi. Atomning bu hududi yadro deb ataladi.
Atomning o'lchamlari m, yadroning o'lchamlari  m yadro massasi atom massasining 99,95% ni tashkil qiladi. Neytral atomda Z elektronlar. Yadro zaryadi musbat va elementar zaryadga karrali
m yadro massasi atom massasining 99,95% ni tashkil qiladi. Neytral atomda Z elektronlar. Yadro zaryadi musbat va elementar zaryadga karrali  Cl. Yadro zaryadini quyidagicha ifodalash mumkin
Cl. Yadro zaryadini quyidagicha ifodalash mumkin  , Qayerda Z- zaryad raqami, u davriy jadvalning kimyoviy soniga to'g'ri keladi va yadroga kiritilgan protonlar soniga teng.
, Qayerda Z- zaryad raqami, u davriy jadvalning kimyoviy soniga to'g'ri keladi va yadroga kiritilgan protonlar soniga teng.
Yadroning ikkinchi muhim xususiyati uning massasidir. Yadroning massasi yadro tarkibiga kirgan protonlarning massalari yig'indisidan kattaroq bo'lib chiqdi.
Yadro tarkibida neytral zarrachalar bor deb taxmin qilingan. 1932 yilda Chadvig neytronlarni kashf etdi. Ivanenko va Geyzenberg yadroning proton-neytron nazariyasini taklif qildilar. Yadro proton va neytronlarga bo'linadi. Ular nuklonlar deb ataladi. Yadrodagi nuklonlarning umumiy soni massa raqami deb ataladiA
.
Neytronlarning umumiy soni N=A-Z ga teng. Protonning qolgan massasi  kg, neytron massasi
kg, neytron massasi  kg.
kg.
Kimyoviy elementning yadrosi neytral atom bilan bir xil belgi bilan belgilanadi  , Qayerda Z- atom raqami (yadro zaryadi), A- massa soni (yadrodagi nuklonlar soni). Zaryad soni bir xil, ammo massalari har xil bo'lgan yadrolar izotoplar deb ataladi (izotoplar neytronlar soni bilan farqlanadi). Massa soni bir xil, lekin zaryad raqamlari har xil bo'lgan yadrolar izobarlar deyiladi.
, Qayerda Z- atom raqami (yadro zaryadi), A- massa soni (yadrodagi nuklonlar soni). Zaryad soni bir xil, ammo massalari har xil bo'lgan yadrolar izotoplar deb ataladi (izotoplar neytronlar soni bilan farqlanadi). Massa soni bir xil, lekin zaryad raqamlari har xil bo'lgan yadrolar izobarlar deyiladi.
28. Yadro kuchlarining xossalari.
Yadro kuchlarining xususiyatlari:

29. Radioaktivlik. Alfa va beta parchalanishi. Ofset qoidalari.
Radioaktivlik deyiladi bir kimyoviy elementning beqaror izotoplarining boshqa elementning izotoplariga aylanishi, ba'zi zarrachalarning emissiyasi. Tabiiy radioaktivlik - bu tabiatda mavjud bo'lgan beqaror izotoplarda kuzatiladigan radioaktivlik. Sun'iy radioaktivlik - yadro reaksiyalari natijasida olingan izotoplarning radioaktivligi.
Radioaktiv nurlanish murakkab tarkibga ega. Magnit maydonda radioaktiv nurlanishning tor nurlari uch qismga bo'linadi:

 -zarralar -
geliy yadrolarining zaryad bilan oqimi Z=2
e va massa soni A=4
(
-zarralar -
geliy yadrolarining zaryad bilan oqimi Z=2
e va massa soni A=4
( ). Tezlik
). Tezlik  -zarralar ga teng
-zarralar ga teng  Xonim. Moddaga kirish
Xonim. Moddaga kirish  -zarralar atomlar va molekulalar bilan faol ta'sir qiladi, uni ionlashtiradi va qo'zg'atadi. Qachon energiya
-zarralar atomlar va molekulalar bilan faol ta'sir qiladi, uni ionlashtiradi va qo'zg'atadi. Qachon energiya  -zarrachalar qisqaradi termal harakat, u ikkita elektronni ushlaydi va geliy atomiga aylanadi ( U). Bundan oldin u yugurish deb ataladigan yo'ldan o'tadi. Materiya bilan kuchli o'zaro ta'sir tufayli diapazon qisqa. Bir parcha qog'oz yoki kiyim ko'tarilib turibdi
-zarrachalar qisqaradi termal harakat, u ikkita elektronni ushlaydi va geliy atomiga aylanadi ( U). Bundan oldin u yugurish deb ataladigan yo'ldan o'tadi. Materiya bilan kuchli o'zaro ta'sir tufayli diapazon qisqa. Bir parcha qog'oz yoki kiyim ko'tarilib turibdi  -zarralar. 0,05 mm qalinlikdagi alyuminiy qatlam ham kechiktiradi
-zarralar. 0,05 mm qalinlikdagi alyuminiy qatlam ham kechiktiradi  -zarralar. Ionlashtiruvchi kuch
-zarralar. Ionlashtiruvchi kuch  -zarralar katta va teng
-zarralar katta va teng  yugurish uzunligi bo'ylab bug '.
yugurish uzunligi bo'ylab bug '.
 -zarralar
tezlikda yadrolardan chiqadigan elektronlar oqimidir
-zarralar
tezlikda yadrolardan chiqadigan elektronlar oqimidir  Xonim. Neytron protonga aylanganda yadro elektron chiqaradi:
Xonim. Neytron protonga aylanganda yadro elektron chiqaradi:
![]()
Qayerda  - elektron belgilanishi,
- elektron belgilanishi,  - elektron antineytrino.
- elektron antineytrino.
Ionlashtiruvchi kuch  - zarralar nikidan yuzlab marta kichik
- zarralar nikidan yuzlab marta kichik  -zarralar va penetratsion quvvat kattaroqdir.
-zarralar va penetratsion quvvat kattaroqdir.  -radiatsiya 2 mm qalinlikdagi alyuminiy qatlami bilan kechiktiriladi.
-radiatsiya 2 mm qalinlikdagi alyuminiy qatlami bilan kechiktiriladi.
Massa soni nima atom yadrosi? Massa soni son jihatdan yadroning neytronlari va protonlari yig'indisiga teng. U A harfi bilan belgilanadi. "Masa soni" tushunchasi yadro massasi yadro zarralari soni bilan aniqlanishi tufayli paydo bo'ldi. Yadro massasi va zarrachalar soni qanday bog'liq? Keling, bilib olaylik.
Atom tuzilishi
Har qanday atom yadro va elektronlardan iborat. Vodorod atomidan tashqari, chunki u faqat bitta elektronga ega. Yadro musbat zaryadlangan. Elektronlar manfiy zaryadga ega. Har bir elektronning zaryadi -1 deb qabul qilinadi. Atom umuman elektr neytral, ya'ni zaryadga ega emas. Demak, manfiy zaryadli zarrachalar, ya'ni elektronlar soni yadroning musbat zaryadiga teng. Masalan, kislorod atomida yadro zaryadi +8, kaltsiy atomida esa yadro zaryadi +20 va 20 ta elektron bor;
Yadro tuzilishi
Yadro ikki xil zarrachalardan - proton va neytronlardan iborat. Protonlar musbat zaryadlangan, neytronlar esa zaryadga ega emas. Shunday qilib, protonlar yadroga zaryad beradi. Har bir protonning zaryadi +1 deb qabul qilinadi. Ya'ni, yadroda qancha proton bo'lsa, bu butun yadroning zaryadi bo'ladi. Masalan, uglerod yadrosida 6 ta proton bor, yadro zaryadi +6 ga teng.
Mendeleyevning elementlar davriy sistemasida barcha elementlar yadro zaryadining ortib borishi tartibida joylashtirilgan. Vodorod +1 yadro zaryadiga ega va birinchi bo'lib joylashgan; geliy +2 ga ega, u jadvalda ikkinchi o'rinda turadi; lityum +3 ga ega, u uchinchi va hokazo. Ya'ni, yadro zaryadi jadvaldagi elementning seriya (atom) raqamiga mos keladi.
Umuman olganda, har qanday atom elektr neytral hisoblanadi. Bu shuni anglatadiki, elektronlar soni yadro zaryadiga, ya'ni protonlar soniga teng. Protonlar soni elementning atom raqamini aniqlaganligi sababli, bu atom raqamini bilib, biz elektronlar sonini, protonlar sonini va yadro zaryadini bilamiz.
Atom massasi
Atomning massasi (M) uning tarkibiy qismlari, ya'ni elektronlar va yadrolarning massasi bilan aniqlanadi. Elektronlar yadroga nisbatan juda engil va butun atom massasiga deyarli hech qanday hissa qo'shmaydi. Ya'ni, atomning massasi yadro massasi bilan belgilanadi. Massa soni nima? Yadroning massasi uning tarkibiga kiradigan zarrachalar soni - protonlar va neytronlar bilan belgilanadi. Shunday qilib, massa soni yadro massasi bo'lib, massa birliklarida (gramm) emas, balki zarrachalar sonida ifodalanadi. Albatta, yadrolarning grammda ifodalangan absolyut massasi (m) ma'lum. Ammo bu salbiy kuchlarda ifodalangan juda kichik raqamlar. Masalan, uglerod atomining massasi m (C) = 1,99 ∙ 10 -23 g Bunday raqamlarni ishlatish noqulay. Va agar kerak bo'lmasa mutlaq qiymatlar massalar, lekin siz faqat elementlar yoki zarralar massalarini solishtirishingiz kerak, keyin amuda ifodalangan atomlarning nisbiy massalaridan (A r) foydalaning. Atomning nisbiy massasi davriy jadvalda ko'rsatilgan, masalan, azot 14,007 ga ega. Atomning nisbiy massasi, butun songa yaxlitlangan, element yadrosining massa soni (A). Massa raqamlari shundayki, ulardan foydalanish qulay - ular har doim butun sonlar: 1, 2, 3 va hokazo. Misol uchun, azotda 14, uglerodda 12. Ular yuqori chap indeks bilan yoziladi, masalan, 14 N yoki 12 C.

Massa raqamini qachon bilishingiz kerak?
Davriy jadvaldagi (Z) elementning massa raqamini (A) va atom raqamini bilib, siz neytronlar sonini aniqlashingiz mumkin. Buning uchun massa sonidan protonlarni ayirish kerak.
Massa sonini bilib, siz yadro yoki butun atomning massasini hisoblashingiz mumkin. Yadroning massasi uning tarkibini tashkil etuvchi zarrachalar massasi bilan aniqlanganligi sababli, u bu zarralar soni va bu zarralar massasining ko'paytmasiga, ya'ni neytron massasining ko'paytmasiga teng. va massa soni. Neytronning massasi umuman protonning massasiga teng, ular nuklonning (yadro zarrasi) massasi sifatida belgilanadi;
Masalan, alyuminiy atomining massasini hisoblaylik. Mendeleyevning elementlar davriy sistemasidan ko‘rinib turibdiki, alyuminiyning nisbiy atom massasi 26,992 ga teng. Yaxlitlash, alyuminiy yadrosining massa raqamini olamiz 27. Ya'ni uning yadrosi 27 zarradan iborat. Bir zarrachaning massasi 1,67 ∙ 10 -24 g ga teng bo'lgan doimiy qiymat bo'lsa, alyuminiy yadrosining massasi quyidagicha bo'ladi: 27 ∙ 1,67 ∙ 10 -24 g = 4,5 ∙ 10 -23 g.

Radioaktiv parchalanish yoki yadro reaksiyalarini tuzishda element yadrolarining massa sonini bilishingiz kerak. Masalan, uran 235 U bir neytronni 1 n tutganda, bariy 141 Ba va kripton 92 Kr yadrolari, shuningdek, uchta erkin neytron 1 n hosil bo'ladi. Bunday reaksiyalarni tuzishda qoida qo'llaniladi: tenglamaning o'ng va chap tomonidagi massa sonlarining yig'indisi o'zgarmaydi. 235+1 = 92+141+3.
Massa soni - atom yadrosidagi proton va neytronlarning umumiy soni. U A belgisi bilan belgilanadi.
Muayyan atom yadrosi haqida gap ketganda, odatda nuklid atamasi ishlatiladi va yadro zarralari protonlar va neytronlar birgalikda nuklonlar deb ataladi.
Atom raqami.
Elementning atom raqami - bu uning atom yadrosidagi protonlar soni. U Z belgisi bilan belgilanadi. Atom raqami massa soniga quyidagi munosabat bilan bog'lanadi:
bu erda N - atom yadrosidagi neytronlar soni.
Har bir kimyoviy element ma'lum bir atom raqami bilan tavsiflanadi. Boshqacha qilib aytganda, ikkita element bir xil atom raqamiga ega bo'lolmaydi. Atom raqami faqat atom yadrosidagi protonlar soniga teng emas ushbu elementdan, lekin atom yadrosini oʻrab turgan elektronlar soniga ham teng. Bu butun atomning elektr neytral zarra ekanligi bilan izohlanadi. Shunday qilib, atom yadrosidagi protonlar soni yadroni o'rab turgan elektronlar soniga teng. Bu bayonot, albatta, zaryadlangan zarralar bo'lgan ionlarga taalluqli emas.
Elementlarning atom raqamlarining birinchi eksperimental isboti 1913 yilda Oksfordda ishlagan Genri Mozili tomonidan olingan. U qattiq metall nishonlarni katod nurlari bilan bombardimon qildi. (Barkla va Kayi 1909 yilda har qanday qattiq element katod nurlarining tez nurlari bilan bombardimon qilinganda, ushbu elementga xos bo'lgan rentgen nurlarini chiqarishini allaqachon ko'rsatgan edi.) Mozeli fotosuratga olish texnikasi yordamida xarakterli rentgen nurlarini tahlil qildi. U xarakterli rentgen nurlanishining to'lqin uzunligi metallning atom og'irligi (massasi) ortishi bilan ortib borishini aniqladi va shuni ko'rsatdiki Kvadrat ildiz Ushbu rentgen nurlanishining chastotasi u belgi bilan belgilagan ba'zi bir butun songa to'g'ridan-to'g'ri proportsionaldir.
![]()
Mozeli bu raqam atom massasining taxminan yarmi ekanligini aniqladi. U bu raqam - elementning atom raqami - degan xulosaga keldi asosiy mulk uning atomlari. Bu berilgan element atomidagi protonlar soniga teng bo'lib chiqdi. Shunday qilib, Mozeley xarakterli rentgen nurlanishining chastotasini chiqaradigan elementning seriya raqami bilan bog'ladi (Moselining qonuni). Bu qonun bor edi katta ahamiyatga ega kimyoviy elementlarning davriy qonunini o'rnatish va elementlarning atom sonining fizik ma'nosini o'rnatish.
Moselining tadqiqotlari unga o'sha vaqtga kelib uchta bedarak yo'qolganlar borligini bashorat qilishga imkon berdi davriy jadval atom raqamlari 43, 61 va 75 bo'lgan elementlar. Bu elementlar keyinroq kashf etilgan va mos ravishda texnetiy, prometiy va reniy deb nomlangan.
Moseley Birinchi jahon urushidagi janglarda halok bo'ldi.
Nuklid belgilari.
Nuklidning massa raqami odatda ustun belgisi sifatida, atom raqami esa element belgisining chap tomonida pastki chiziq sifatida ko'rsatiladi. Masalan, yozuv bu uglerod nuklidining (barcha boshqa uglerod nuklidlari kabi) atom raqami 6 ekanligini bildiradi. Bu nuklidning massa soni 12 ga teng. Boshqa uglerod nuklidiga belgi berilgan. nuklid ko'pincha oddiy yoki uglerod-14 sifatida yoziladi.
Izotoplar.
Izotoplar - har xil xususiyatlarga ega bo'lgan bir elementning atom navlari. Ular yadrosidagi neytronlar soni bilan farqlanadi. Shunday qilib, bir elementning izotoplari bir xil atom raqamiga ega, ammo massa raqamlari har xil. Jadvalda 1.1-jadvalda A massa soni, Z atom raqami va uglerodning uchta izotopining har bir atomi yadrosidagi neytronlar soni N qiymatlari ko'rsatilgan.
1.1-jadval. Uglerod izotoplari

Elementlarning izotopik tarkibi.
Ko'pgina hollarda har bir element turli xil izotoplarning aralashmasidir. Bunday aralashmadagi har bir izotopning tarkibiga izotopik ko'plik deyiladi. Masalan, kremniy tabiatda uchraydigan birikmalarda quyidagi tabiiy izotopik ko'pliklarga ega: . E'tibor bering, elementning umumiy izotopik ko'pligi aniq 100% bo'lishi kerak. Ushbu izotoplarning har birining nisbiy izotopik miqdori mos ravishda 0,9228, 0,0467 va 0,0305 ni tashkil qiladi. Bu raqamlarning yig'indisi aniq 1.0000 ni tashkil qiladi.
Atom massa birligi (a.m.u.).
Hozirgi vaqtda atom massasi birligini aniqlash uchun standart nuklidning massasi hisoblanadi. Shunday qilib, atom massa birligi ushbu nuklid massasining o'n ikkidan biriga teng. Atom massa birligining haqiqiy qiymati kg ga teng. Uch asosiy zarralar, qaysiki komponentlar atom quyidagi massalarga ega:
proton massasi = 1,007277 amu
neytron massasi = 1,008 665 amu
elektron massasi = 0,000 548 6 a. yemoq.
Ushbu qiymatlardan foydalanib, har bir o'ziga xos nuklidning izotopik massasini hisoblashingiz mumkin. Masalan, nuklidning izotopik massasi 17 proton, 18 neytron va 17 elektron massalarining yig'indisidir:
Biroq, aniq eksperimental ma'lumotlar izotop massasi 34,968 85 a qiymatiga ega ekanligini ko'rsatadi. e.m. Hisoblangan va eksperimental ravishda topilgan qiymatlar o'rtasidagi tafovut ommaviy nuqson deb ataladi, ommaviy nuqsonning paydo bo'lishining sababi bo'limda tushuntiriladi. 1.3.
Nisbiy atom massasi shkalasida izotop massalari ularni nuklid massasining o'n ikkidan biriga bo'lish natijasida ifodalanadi. Shunday qilib, izotopning nisbiy izotopik massasi

E'tibor bering, nisbiy izotopik massalar o'lchovsiz birliklarda ifodalanadi.
Kimyoviy elementning nisbiy atom massasi AT izotop tarkibini hisobga olgan holda nisbiy izotopik massalarning o'rtacha arifmetik ko'rsatkichidir. U har bir izotopning nisbiy izotopik massasi va uning nisbiy ko'pligi mahsulotini yig'ish yo'li bilan hisoblanadi.
Quyidagi ma'lumotlardan foydalanib, xlorning nisbiy atom massasini hisoblaymiz:

(chaqirdi umumiy atama yadrodagi "nuklonlar"). Odatda harf bilan belgilanadi A. Massa soni atom massa birliklarida ifodalangan izotopning atom massasiga yaqin, lekin faqat uglerod-12 uchun bir xil, chunki atom massasi birligi (a.m.u.) endi quyidagicha aniqlanadi. 1 ⁄ 12 atomning massasi 12 C. Boshqa barcha hollarda atom massasi massa sonidan farqli ravishda butun son emas. Shunday qilib, 35 Cl xlor izotopining massa soni 35 ga, atom massasi esa 34,96885 amuga teng.
Muayyan nuklidni (atom yadrolarining turi) belgilashdagi massa soni yuqori chap indeks bilan yoziladi, masalan, 232 Th. Massa soni bir xil bo'lgan nuklidlar izobarlar deyiladi (masalan, 14 C va 14 N nuklidlari izobarlar).
Massa sonini bilish yadro va atomning massasini taxmin qilish imkonini beradi. Agar massa soni ma'lum bo'lsa, u holda massa M atom va uning yadrosi quyidagi munosabat asosida baholanadi M ≈ A m N, Qayerda m N ≈ 1,67·10 −27 kg - nuklon, ya'ni proton yoki neytronning massasi. Masalan, alyuminiy-27 atomi va uning yadrosida 27 ta nuklon (13 proton va 14 neytron) mavjud. Uning massasi taxminan 27·1,67·10−27 kg ≈ 4,5·10−26 kg. Agar yadroning massasini kattaroq aniqlik bilan olish zarur bo'lsa, yadrodagi nuklonlar yadro tortishish kuchlari bilan bog'langanligini hisobga olish kerak va shuning uchun munosabatlarga muvofiq. E=mc 2 yadroning massasi kamayadi. Yadro atrofidagi orbitalardagi elektronlarning umumiy massasi ham atom massasiga qo'shilishi kerak. Biroq, bu tuzatishlarning barchasi 1% dan oshmaydi.
| 238 92 U | → | 234 90 Th | + | 4 2 U |
chap tomonda boshlang'ich yadroning massa soni 238, reaksiyaning o'ng tomonida massa raqamlari 234 va 4 bo'lgan ikkita yadro joylashgan bo'lib, ular jami 238 tani beradi. Alfa massa raqamini hisobga olgan holda. zarracha (geliy-4 yadrosi) 4, alfa-parchalanish parchalanuvchi yadroning massa sonini 4 birlikka kamaytiradi. Beta-yemirilishning har qanday turlari (beta-minus yemirilish, pozitron yemirilishi, elektronni tutib olish, qoʻshaloq beta-yemirilishning barcha turlari) massa sonini oʻzgartirmaydi, chunki bu jarayonda yadroning faqat baʼzi nuklonlari bir turdan ikkinchi turga (protonlar) aylanadi. neytronlar yoki orqaga). Izomerik o'tish ham yadroning massa sonini o'zgartirmaydi.
"Ommaviy raqam" maqolasi haqida sharh yozing
Eslatmalar
Shuningdek qarang
Massa raqamini tavsiflovchi parcha
- Ayting-chi, siz Moskvada qolganingizda grafinyaning o'limi haqida bilmasmidingiz? - dedi malika Marya va uning ozod bo'lgan so'zlaridan keyin bu savolni qo'yib, uning so'zlariga, ehtimol, ularda bo'lmagan ma'noni berganini payqab, darhol qizarib ketdi."Yo'q", deb javob berdi Per, malika Marya o'zining erkinligi haqida aytgan talqinni noqulay deb topmadi. "Men buni Orelda o'rgandim va bu menga qanday ta'sir qilganini tasavvur qila olmaysiz." Biz namunali turmush o'rtoqlar emas edik, - dedi u tezda Natashaga qarab va uning yuzida xotiniga qanday munosabatda bo'lishi haqidagi qiziqishni payqadi. "Ammo bu o'lim meni qattiq hayratda qoldirdi." Ikki kishi janjallashsa, har doim ikkalasi ham aybdor. Va endi yo'q bo'lgan odamning oldida o'z aybi birdaniga og'irlashadi. Keyin shunday o'lim... do'stlarsiz, tasallisiz. "Men undan juda afsusdaman", deb tugatdi u va Natashaning yuzidagi quvonchli ma'qulni payqaganidan xursand bo'ldi.
"Ha, siz yana bakalavr va kuyovsiz", dedi malika Marya.
Per to'satdan qip-qizil qizarib ketdi va uzoq vaqt Natashaga qaramaslikka harakat qildi. U unga qarashga qaror qilganida, uning yuzi sovuq, qo'pol va hatto nafratlangan edi.
- Lekin biz aytganidek, siz haqiqatan ham Napoleonni ko'rganmisiz va u bilan gaplashdingizmi? - dedi malika Marya.
Per kulib yubordi.
- Hech qachon, hech qachon. Har doim hammaga asir bo'lish Napoleonning mehmoni bo'lish deganidek tuyuladi. Men uni nafaqat ko'rmaganman, balki u haqida eshitmaganman ham. Men ancha yomon kompaniyada edim.
Kechki ovqat tugadi va dastlab asirligi haqida gapirishdan bosh tortgan Per asta-sekin bu voqeaga aralashdi.
- Lekin Napoleonni o'ldirish uchun qolganingiz rostmi? – so‘radi Natasha undan biroz jilmayib. “Sizni Suxarev minorasida uchratganimizda taxmin qildim; esingizdami?
Per bu haqiqat ekanligini tan oldi va bu savoldan asta-sekin malika Maryaning va ayniqsa Natashaning savollariga asoslanib, batafsil hikoya sarguzashtlaringiz haqida.
Avvaliga u odamlarga, ayniqsa, o'ziga nisbatan masxara, muloyim nigoh bilan gapirdi; lekin keyin o‘zi ko‘rgan dahshat va iztiroblar haqidagi hikoyaga kelganda, o‘zi ham sezdirmay, o‘zini tutib qoldi va xotirasida kuchli taassurotlarni boshdan kechirayotgan odamdek tutilgan hayajon bilan gapira boshladi.