Płomień z przodu. Płomień może złożyć się w akordeon pod wpływem własnego echa Perkolacja frontu płomienia
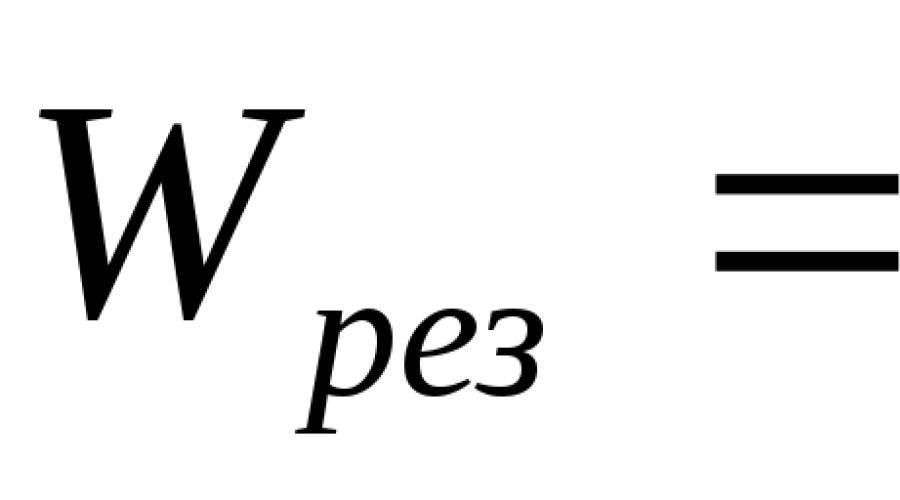
Gdy pali się poruszająca się mieszanina, wynikowa prędkość propagacji płomienia będzie sumą sum  .
.
Warunkiem, aby front płomienia był nieruchomy (tj. nieruchomy) jest  - prędkość wynikowa wynosi zero,
- prędkość wynikowa wynosi zero,  .
.
Jako model rozważ palnik Buzin.
Gdy gaz i powietrze są dostarczane do wylotu rurki z dużą prędkością W, utworzy się stożek, a wzrost prędkości doprowadzi do wzrostu wysokości (powierzchni) stożka i zmniejszenia kąta u góry. Albo odwrotnie.
4.3. Procesy w płaskim froncie płomienia.
R  Spójrzmy na front płomienia. Będzie to wąski obszar, na którym h f
to grubość frontu, a h X
to grubość strefy reakcji chemicznej. Jednocześnie można go podzielić na 2 strefy: strefę grzania i strefę reakcji.
Spójrzmy na front płomienia. Będzie to wąski obszar, na którym h f
to grubość frontu, a h X
to grubość strefy reakcji chemicznej. Jednocześnie można go podzielić na 2 strefy: strefę grzania i strefę reakcji.
Świeża mieszanina gazu i powietrza wchodzi do strefy 1, stężenie gazu w powietrzu pozostaje stałe, ponieważ reakcja chemiczna jeszcze się nie rozpoczęła, ale trwa tylko ogrzewanie ze względu na ciepło uwalniane w strefie reakcji. Rozpoczyna się tam, gdzie dopływ ciepła staje się równy mocy cieplnej, czyli w języku matematyki  , co odpowiada temperaturze zapłonu T B. W strefie grzewczej dopływ ciepła jest większy niż odprowadzanie
, co odpowiada temperaturze zapłonu T B. W strefie grzewczej dopływ ciepła jest większy niż odprowadzanie  , oraz w strefie reakcji
, oraz w strefie reakcji  . Transport ciepła w czole płomienia odbywa się poprzez przewodnictwo cieplne. A maksymalne wydzielanie ciepła leży w strefie reakcyjnej i spada do 0 na końcu frontu.
. Transport ciepła w czole płomienia odbywa się poprzez przewodnictwo cieplne. A maksymalne wydzielanie ciepła leży w strefie reakcyjnej i spada do 0 na końcu frontu.
Na propagację frontu płomienia ma wpływ nie tylko szybkość reakcji chemicznej, ale także transport substancji i produktów spalania.
4.4 Stabilizacja laminarnego frontu płomienia.
P 
 Gdy do palnika podawany jest gaz rzeczywisty, prędkość propagacji zmienia się od maksymalnej w środku do jej minimalnej wartości na obwodzie. Front płomienia jest zatem zakrzywiony w kształcie stożka. A normalną prędkość propagacji płomienia można skompensować tylko
Gdy do palnika podawany jest gaz rzeczywisty, prędkość propagacji zmienia się od maksymalnej w środku do jej minimalnej wartości na obwodzie. Front płomienia jest zatem zakrzywiony w kształcie stożka. A normalną prędkość propagacji płomienia można skompensować tylko  , a drugi składnik
, a drugi składnik  zniszczy punkt na szczycie pochodni. na obrzeżach ze względu na zdolność chłodzenia ścian U n znacznie spada w stosunku do wartości średniej, powstaje możliwość bezpośredniej kompensacji prędkości przepływu W
prędkość U n. Dzięki temu czoło płomienia na krawędzi zamienia się w płaszczyznę poziomą i powstaje stabilna strefa spalania - pierścień zapalający. Ten obszar może istnieć niezależnie.
zniszczy punkt na szczycie pochodni. na obrzeżach ze względu na zdolność chłodzenia ścian U n znacznie spada w stosunku do wartości średniej, powstaje możliwość bezpośredniej kompensacji prędkości przepływu W
prędkość U n. Dzięki temu czoło płomienia na krawędzi zamienia się w płaszczyznę poziomą i powstaje stabilna strefa spalania - pierścień zapalający. Ten obszar może istnieć niezależnie.
Front płomienia określany jest generalnie przez prawo cosinusów, ao jego stabilności decyduje stabilizacja pierścienia zapłonowego. Dlatego określamy główne zależności stabilnego płomienia.
Ponieważ wszystkie palniki pracują w różnych trybach, możliwe są sytuacje, w których natężenie przepływu przekroczy U n lub możliwa jest sytuacja odwrotna.
Oderwanie się płomienia wiąże się z istnieniem pierścienia zapalającego i jego zniszczeniem. Separacja nastąpi, jeśli prędkość przepływu przekroczy krytyczną prędkość separacji (strefa II na rysunku 8).
Na prędkość startu wpływa kilka czynników. Z zwiększyćśrednica palnik jego wydajność chłodnicza maleje oraz limit łamania płomieniawzrasta(linie proste 3,2,1). Z ubogą mieszanką (zwiększone powietrze pierwotne) spadkowy prędkość ucieczki. A wraz ze spadkiem ilości powietrza pierwotnego (płomień dyfuzyjny) prędkości graniczne wzrosną.
Przełom następuje, gdy U n przekracza natężenie przepływu płomienia (strefa 3 na rys. 8).
Cofanie się płomienia jest związane z wydajnością chłodzenia ścianek palnika. Brak warunku poślizgu  . Wraz ze wzrostem średnicy wzrasta normalne tempo spalania, im bardziej ceteris paribus wzrasta prawdopodobieństwo przebicia, tym większe powinno być natężenie przepływu zapobiegające przebiciu płomienia (krzywe 1,2,3 na rys. 8) 1 . Maksymalne prędkości bezpoślizgowe będą obserwowane przy wartościach nadmiaru powietrza nieco mniejszych niż stechiometryczne. Chłodzenie ust palnika służy do zmniejszenia ryzyka wystąpienia rozgorzenia.
. Wraz ze wzrostem średnicy wzrasta normalne tempo spalania, im bardziej ceteris paribus wzrasta prawdopodobieństwo przebicia, tym większe powinno być natężenie przepływu zapobiegające przebiciu płomienia (krzywe 1,2,3 na rys. 8) 1 . Maksymalne prędkości bezpoślizgowe będą obserwowane przy wartościach nadmiaru powietrza nieco mniejszych niż stechiometryczne. Chłodzenie ust palnika służy do zmniejszenia ryzyka wystąpienia rozgorzenia.
Istnieją również metody stabilizacji płomienia.


ryc. 9. Stabilizacja za pomocą ryc. 10. Stabilizacja płomienia
zapalający pierścień z korpusem w kształcie litery V.
H  i ryc. 9 przedstawia urządzenie, które stabilizuje się dzięki temu, że gaz przez kanały 2 wchodzi do pierścieniowej szczeliny 3. Tworzy to stabilny pierścień zapłonowy, który zapobiega zerwaniu płomienia. Na ryc. 10 przedstawia stabilizację przepływu przez korpus w kształcie litery V. Z powodu turbulencji powstaje pozory pierścienia zapalającego, a prawdopodobieństwo oddzielenia płomienia maleje (wzrasta maksymalna prędkość).
i ryc. 9 przedstawia urządzenie, które stabilizuje się dzięki temu, że gaz przez kanały 2 wchodzi do pierścieniowej szczeliny 3. Tworzy to stabilny pierścień zapłonowy, który zapobiega zerwaniu płomienia. Na ryc. 10 przedstawia stabilizację przepływu przez korpus w kształcie litery V. Z powodu turbulencji powstaje pozory pierścienia zapalającego, a prawdopodobieństwo oddzielenia płomienia maleje (wzrasta maksymalna prędkość).
Stabilizator tunelu pokazano na ryc. 11. Mieszanina gazowo-powietrzna opuszcza palnik 1 do tunelu 3, gdzie powstaje płomień 2. Produkty spalania są zasysane do podstawy płomienia, tworzy się strefa ich ruchu powrotnego, tworząc stabilny pierścień zapłonowy. Ponieważ zassanie zimnego powietrza znacznie pogorszyłoby warunki zapłonu.
Struktura płomienia dyfuzyjnego zależy zasadniczo od przekroju przepływu palnych par i gazów oraz jego prędkości. W zależności od charakteru przepływu rozróżnia się laminarne i turbulentne płomienie dyfuzyjne.
burzliwy nazywa się niespokojnym, wirującym płomieniem o ciągle zmieniającej się formie.
wraz ze wzrostem przepływu płomień zmienia swój kształt i staje się niespokojny, wirując wirami, stale zmieniając kształt, jest to płomień burzliwy.
Takie zachowanie płomienia w reżimie turbulentnym tłumaczy się tym, że do strefy spalania zaczyna wchodzić znacznie większa ilość gazu palnego, to znaczy coraz więcej paliwa musi być jednorazowo utlenione, co prowadzi do wzrostu wielkość płomienia i jego dalsze turbulencje.
przód płomienia- cienka warstwa powierzchniowa ograniczająca płomień, w której bezpośrednio zachodzą reakcje redoks.
Grubość czoła płomienia jest niewielka, zależy od parametrów gazodynamicznych oraz mechanizmu propagacji płomienia (deflagracji lub detonacji) i może wynosić od dziesiątych części milimetra do kilku centymetrów. Wewnątrz płomienia prawie całą objętość zajmują gazy palne (GH) i opary. Produkty spalania (PG) znajdują się na froncie płomienia. W środowisku znajduje się środek utleniający.
Schemat płomienia dyfuzyjnego palnika gazowego oraz zmiany stężeń substancji palnych, środka utleniającego i produktów spalania w przekroju płomienia przedstawiono na ryc. 1.2.
Grubość czoła płomienia różnych mieszanin gazów w reżimie laminarnym wynosi 0,5 - 10 -3 cm Średni czas całkowitej konwersji paliwa na produkty spalania w tej wąskiej strefie wynosi 10 -3 -10 -6 s.
Strefa maksymalnej temperatury znajduje się 5-10 mm nad świecącym stożkiem płomienia, a dla mieszaniny propan-powietrze wynosi około 1600 K.
Płomień dyfuzyjny powstaje podczas spalania, kiedy procesy spalania i mieszania przebiegają jednocześnie.
Jak zauważono wcześniej, główna różnica między spalaniem dyfuzyjnym a spalaniem wstępnie zmieszanych mieszanin palnych polega na tym, że szybkość przemian chemicznych podczas spalania dyfuzyjnego jest ograniczona przez mieszanie utleniacza i paliwa, nawet jeśli szybkość reakcji chemicznej jest bardzo wysoka, intensywność spalania jest ograniczona warunkami mieszania.
Istotną konsekwencją tej koncepcji jest fakt, że w czole płomienia paliwo i utleniacz są w stosunek stechiometryczny. Niezależnie od stosunków oddzielnie dostarczanych przepływów utleniacza i paliwa, front płomienia jest zawsze ustawiony w takim położeniu, że przepływ reagentów zachodzi w stosunkach stechiometrycznych. Zostało to potwierdzone w wielu eksperymentach.
Siłą napędową dyfuzji tlenu do strefy spalania jest różnica między jego stężeniami wewnątrz płomienia (СО = 0) iw powietrzu otoczenia (początkowe СО = 21%). Wraz ze spadkiem tej różnicy zmniejsza się szybkość dyfuzji tlenu, a przy określonych stężeniach tlenu w otaczającym powietrzu - poniżej 14-16% spalanie ustaje. Takie zjawisko samoistnego tłumienia (samogaśnięcia) obserwuje się podczas spalania w zamkniętych objętościach.
Każdy płomień zajmuje określoną objętość w przestrzeni, której zewnętrzne granice mogą być wyraźnie lub niewyraźnie ograniczone. Podczas spalania gazów kształt i wielkość powstałego płomienia zależą od rodzaju mieszanki wyjściowej, kształtu palnika i urządzeń stabilizujących. Wpływ składu paliwa na kształt płomienia determinowany jest jego wpływem na szybkość spalania.
Wysokość płomienia jest jedną z głównych cech wielkości płomienia. Jest to szczególnie ważne przy rozważaniu spalania i gaszenia fontann gazowych, spalania produktów naftowych w otwartych zbiornikach.
Wysokość płomienia jest tym większa, im większa średnica rury i większa prędkość wypływu, a im mniejsza, tym większa normalna prędkość propagacji płomienia.
Dla danej mieszanki paliwa i utleniacza wysokość płomienia jest proporcjonalna do prędkości przepływu i kwadratu średnicy strumienia:
gdzie jest natężenie przepływu;
średnica strumienia;
współczynnik dyfuzji.
Jednak kształt płomienia pozostaje nieznany i zależy od naturalnej konwekcji i rozkładu temperatury na froncie płomienia.
Ta zależność jest utrzymywana do określonej wartości natężenia przepływu. Wraz ze wzrostem prędkości przepływu płomień turbulizuje się, po czym zatrzymuje się dalszy wzrost jego wysokości. To przejście następuje, jak już wspomniano, dla pewnych wartości kryterium Reynoldsa.
W przypadku płomieni, gdy następuje znaczne uwolnienie niespalonych cząstek w postaci dymu, pojęcie wysokości płomienia traci swoją pewność, ponieważ. trudno jest określić granicę spalania produktów gazowych na szczycie płomienia.
Ponadto w płomieniach zawierających cząstki stałe, w porównaniu z płomieniami zawierającymi tylko gazy spalinowe, promieniowanie znacznie wzrasta.
Temat 7. ROZKŁAD PŁOMIENIA.
7.1. Termiczna teoria spalania.
Dla adiabatycznych, tj. spalaniu, któremu nie towarzyszą straty cieplne, cały dopływ energii chemicznej układu palnego zamieniany jest na energię cieplną produktów reakcji. Temperatura produktów spalania adiabatycznego nie zależy od szybkości reakcji zachodzących w płomieniu, a jedynie od ich całkowitego efektu cieplnego i pojemności cieplnej produktów końcowych. Wartość ta nazywana jest adiabatyczną temperaturą spalania Tg i jest ważną cechą czynnika palnego. Dla większości palnych mieszanin wartość Tg mieści się w zakresie 1500-3000 ° K. Oczywiste jest, że Tg jest maksymalną temperaturą produktów reakcji przy braku zewnętrznego ogrzewania. Rzeczywista temperatura produktów spalania może być tylko niższa niż T g w przypadku utraty ciepła.
Zgodnie z termiczną teorią spalania opracowaną przez radzieckich naukowców Ya.B. Zeldovich i D.A. Frank-Kamenetsky'ego, rozprzestrzenianie się płomienia odbywa się poprzez przenoszenie ciepła z produktów spalania do niespalonej (świeżej) mieszanki. Na ryc. 26.
Płomień frontu, czyli strefa, w której zachodzi reakcja spalania i intensywne samonagrzewanie się palącego się gazu, rozpoczyna się w temperaturze samozapłonu T st i kończy w temperaturze T g.
Przed rozprzestrzeniającym się w prawo frontem płomienia znajduje się świeża mieszanka, a za nią produkty spalania. Uważa się, że w strefie grzewczej reakcja przebiega tak wolno, że zaniedbuje się wydzielanie ciepła.
Proces wymiany ciepła podczas stacjonarnego propagacji płomienia nie prowadzi do strat ciepła i spadku temperatury w stosunku do Tg bezpośrednio za frontem płomienia. Odprowadzanie ciepła z każdej płonącej warstwy gazu podczas zapłonu sąsiedniej, jeszcze nie ogrzanej warstwy jest kompensowane taką samą ilością ciepła, jaką uzyskano wcześniej w warstwie zapłonowej podczas jej własnego zapłonu. Ciepło dodatkowe początkowego impulsu zapłonowego nie zakłóca w sposób zauważalny stacjonarnego reżimu spalania, ponieważ jego rola maleje wraz ze wzrostem ilości spalanego gazu.
Produkty spalania tracą ciepło tylko w wyniku promieniowania iw kontakcie z twardą powierzchnią. Jeśli promieniowanie jest znikome, spalanie takie jest praktycznie adiabatyczne. Znaczne straty ciepła są możliwe dopiero w pewnej odległości za frontem płomienia.
Tak więc zainicjowanie spalania mieszaniny gazowej w jednym punkcie prowadzi do nagrzania sąsiedniej warstwy, która jest ogrzewana przez przewodzenie ciepła z produktów reakcji do samozapłonu. Spalanie tej warstwy pociąga za sobą zapłon kolejnej i tak dalej. aż do całkowitego spalenia mieszanki palnej. Ciepło odprowadzone ze strefy reakcji do świeżej mieszaniny jest całkowicie kompensowane przez uwolnienie ciepła reakcji i powstaje stabilny front płomienia. W wyniku spalania warstwowego czoło płomienia przemieszcza się przez mieszankę, zapewniając propagację płomienia.
Jeżeli świeża mieszanina porusza się w kierunku czoła płomienia z prędkością równą prędkości propagacji płomienia, to płomień będzie nieruchomy (stacjonarny).
Teoretyczne uzasadnienie warunków propagacji płomienia można podać biorąc pod uwagę płomień stacjonarny, gdy prędkość jego propagacji U pl jest równa szybkości dostarczania mieszaniny gazowej υ g: U pl = υ g (rys. 27). W tym przypadku stosunek normalnej szybkości spalania U n do szybkości propagacji płomienia U pl wyraża się równaniem:
Un = Upl* grzech. (7.1)


Ilość ciepła jest dostarczana do świeżej mieszanki z jednostki powierzchni płomienia w jednostce czasu przez przewodnictwo cieplne:
![]() (7.2)
(7.2)
gdzie: - współczynnik przewodności cieplnej;
Szerokość przodu płomienia.
Ciepło to jest zużywane na podgrzanie świeżej mieszanki od temperatury początkowej T o do temperatury spalania T g:
gdzie: z jest jednostkową pojemnością cieplną;
Gęstość mieszaniny.
Uwzględniając równania (7.2) i (7.3) z U pl = υ g, prędkość propagacji płomienia wyznacza się z zależności:
![]() (7.4)
(7.4)
gdzie: - współczynnik przenikania ciepła.
Ponieważ szybkość spalania jest bardzo zależna od temperatury, spalanie większości gazu zachodzi w strefie, której temperatura jest zbliżona do Tg.
Szybkość reakcji chemicznej, o której mowa w § 6.1., określa równanie:
![]() . (7.5)
. (7.5)
Wtedy prędkość propagacji płomienia wynosi:
gdzie: b jest wskaźnikiem zależnym od właściwości mieszanki, .
Zatem płomień nie będzie mógł rozprzestrzeniać się przez mieszankę palną, jeśli jej temperatura będzie niższa od teoretycznej temperatury spalania o wartość większą niż (patrz § 9.3).
![]() jest charakterystycznym przedziałem temperatur w kinetyce chemicznej. Zmiana temperatury o tę wartość prowadzi do zmiany szybkości reakcji o współczynnik „e”.
jest charakterystycznym przedziałem temperatur w kinetyce chemicznej. Zmiana temperatury o tę wartość prowadzi do zmiany szybkości reakcji o współczynnik „e”.
Wartość graniczną prędkości propagacji płomienia U LIMIT określa stosunek:
![]() (7.7)
(7.7)
W przeciwieństwie do rozpatrywanego przypadku normalnego spalania, w rzeczywistych warunkach wybuchów w przestrzeni zamkniętej, proces spalania deflagracji ulega samoprzyspieszeniu. Wynika to z rozszerzania się powierzchni spalania, występowania ruchu gazu oraz wzrostu ciśnienia podczas spalania.
7.2. Spalanie w zamkniętej objętości.
Podczas spalania gazów w otwartej rurze iw strumieniu produkty reakcji rozszerzają się swobodnie, ciśnienie pozostaje prawie stałe. Spalanie w zamkniętym naczyniu wiąże się ze wzrostem ciśnienia. Ma to ogromne znaczenie dla rozwiązywania problemów bezpieczeństwa wybuchowego. Wzrost ciśnienia podczas spalania w aparatach zamkniętych, a także w pomieszczeniach może prowadzić do zniszczeń i wypadków.
Podczas spalania bez strat ciepła (spalanie adiabatyczne) w objętości zamkniętej, w wyniku wzrostu temperatury od T o do temperatury spalania T g oraz zmiany liczby cząsteczek gramowych podczas reakcji, ciśnienie wzrasta od P o do Rg:
![]() (7.8)
(7.8)
gdzie: m, n - liczba moli substancji przed i po eksplozji stechiometrycznej
skład mieszaniny.
Jednak największe ciśnienie powstaje nie dla mieszanin stechiometrycznych, chociaż mają one najwyższą kaloryczność i tworzą maksymalną Tg, ale dla mieszanin wzbogaconych w substancję palną, które mają maksymalną szybkość spalania. Podczas spalania deflagracyjnego ciśnienie osiąga 7-10 atm., podczas detonacji jest znacznie wyższe.
Cechą charakterystyczną procesu spalania w zamkniętej objętości jest nierównomierny rozkład temperatury produktów reakcji bezpośrednio po spaleniu. Wstępnie palna część mieszaniny palnej, znajdująca się w środku naczynia, reaguje przy ciśnieniu początkowym po; ostatnia warstwa płonąca przy ścianie reaguje pod skończonym ciśnieniem R.
Nagrzewanie każdej warstwy gazu przebiega dwuetapowo: podczas przemiany chemicznej i kompresji adiabatycznej. Chociaż skład produktów spalania i ciśnienie są takie same we wszystkich punktach objętości, ostateczna temperatura zależy zasadniczo od kolejności obu procesów ogrzewania. Pod ciśnieniem adiabatycznym kompresja po do ciśnienia R wzrost temperatury od T o do T jest określony równaniem Poissona
![]() , (7.9)
, (7.9)
gdzie: g = s r / sv.
Temperatura końcowa produktów spalania będzie wyższa, jeśli gaz zostanie najpierw podgrzany podczas przemiany chemicznej, a następnie wzrośnie jego temperatura podczas sprężania zgodnie z równaniem (7.9), niż w przypadku odwrotnej kolejności obu procesów.
7.3. Ruch gazów podczas spalania.
Rozprężanie gazów w płomieniu (zgodnie z prawem Gay-Lussaca) prowadzi do tego, że spalaniu zawsze towarzyszy ruch gazów. Oznaczmy przez ρ g - gęstość ośrodka początkowego, ρ pr - gęstość produktów spalania, ich prędkość względem stacjonarnego frontu płomienia wynosi u pr. Na każdy centymetr kwadratowy powierzchni czołowej przepływ przynosi co sekundę un cm 3 palnej mieszaniny, jej masa wynosi odpowiednio u n * ρ g, z tej sekcji płomienia usuwa się w ciągu 1 s u pr cm 3 produktów reakcji o masie u pr * ρ pr. Ponieważ masy paląca się mieszanina i produkty reakcji są równe, to
u н* ρ г = u pr* ρ pr (7.10)
Równanie (7.10) wyraża prawo zachowania masy podczas spalania.
Wartość u pr przekracza normalną prędkość płomienia tyle razy, o ile gęstość medium wyjściowego jest większa od gęstości produktów spalania. Wzrost natężenia przepływu gazu podczas spalania jest konsekwencją rozszerzania się gazów.
Temperatura bezwzględna podczas spalania wzrasta 5–10 razy. Jeżeli spalanie zachodzi przy stałym ciśnieniu, gaz rozszerza się w r o / r pr raz. Rozważmy spalanie stacjonarnego frontu płomienia w otwartej rurze, pokazanego na rysunku 28.

Ryż. 28. Schemat wyjaśniający prawo obszarów: S – przekrój rury, F – powierzchnia czoła płomienia, ω – prędkość początkowej mieszanki palnej, T 0, – temperatura i gęstość mieszanki początkowej, U H – normalna szybkość spalania, U PL - prędkość rozprzestrzeniania się płomienia, U PR - prędkość produktów spalania, T PR, - temperatura i gęstość produktów spalania.
Ponieważ płomień jest nieruchomy, ω = U PR. Wtedy np. na 1 cm 2 powierzchni frontu płomienia F przepływ przynosi ω cm 3 /s mieszanki palnej. Jego masa to ω. W związku z tym U PR cm 3 /s produktów spalania o masie U PR jest usuwany z tego miejsca. Wtedy zgodnie z prawem zachowania mas (równanie 7.10) przy ω = U PL:
![]() (7.11)
(7.11)
Zatem prędkość objętościowa produktów spalania przewyższa prędkość spalania tyle razy, ile gęstość początkowego ośrodka jest większa niż gęstość produktów spalania.
Z drugiej strony, jeśli U H cm 3 /s mieszanki pali się na 1 cm 2 powierzchni czołowej płomienia, to U H * F cm 3 / s spala się na całej powierzchni F. Jednocześnie objętość palącego się gazu jest równa prędkości objętościowej przepływu gazu ω * S cm 3 / s. Wtedy U H * F = ω * S lub ω = U H * F / S.
Z równością ω \u003d U PL:
UPL= U H* F / S. (7.12)
dostajemy prawo obszarowe: prędkość rozprzestrzeniania się płomienia w rurze będzie tyle razy większa niż normalnie, im powierzchnia płomienia przekroczy przekrój rury.
Jeśli weźmiemy pod uwagę stacjonarną mieszankę palną, to gdy front płomienia się rozprzestrzenia, ostro podgrzane gazy nie mają czasu na rozszerzenie się, a w strefie spalania ciśnienie gwałtownie wzrasta, co „pęka” i wypycha gazy w obu kierunkach z płomienia , a nie tylko produkty spalania są wypychane, ale także następuje ruch początkowej mieszanki przed front płomienia, jak na rysunku 29:

Prędkość gazów wzrasta wraz ze spalaniem początkowej mieszanki i odpowiednio ciśnienia gazów. Jednocześnie z jednego końca rury wyrzucane są sprężone gorące spalone gazy, a z drugiego wypychana jest sprężona mieszanina początkowa, która wybuchowo zapala się od wyrzuconego płomienia do atmosfery pomieszczenia, a następnie następuje fala uderzeniowa , ogień i zniszczenie.
7.4. Współczynniki przyspieszenia spalania.
Poszczególne tryby spalania deflagracji różnią się jedynie prędkością rozprzestrzeniania się płomienia ze względu na nierównomierny rozwój powierzchni czoła płomienia. Spalanie początkowo nieruchomego gazu jest zawsze komplikowane przez zewnętrzne wpływy zakłócające, które zniekształcają kształt płomienia. Najważniejsze z nich to grawitacja, tarcie i turbulencja palącej się mieszanki.
Tak więc podczas zapalania w środku pionowej rury, jak pokazano na rysunku 30, ciężka mieszanina początkowa znajduje się nad lekkimi produktami spalania. W tym przypadku konwekcyjne przepływy mieszaniny początkowej przesuwają się w dół, a produkty spalania w górę. Pod ich wpływem front płomienia rozciąga się i spalanie przyspiesza.
Gdy płomień rozprzestrzenia się w dół, czynnik palny jest nieruchomy, a zakłócenie czoła płomienia jest nieznaczne. Przy małych szybkościach spalania i długości rury kształt płomienia jest zbliżony do płaskiego.
Jednak w tym przypadku gaz przemieszcza się również w dół rury z powodu rozszerzania się podczas spalania. Tarcie poruszającego się gazu o ścianki prowadzi do zmniejszenia jego prędkości na obwodzie i rozciągnięcia frontu płomienia, a profil prędkości frontu płomienia również przyjmuje postać kopuły. Powierzchnia płomienia stopniowo się zwiększa, a spalanie przyspiesza.
Dostatecznie szybkie spalanie, przy którym prędkość płomienia dochodzi do setek m/s, zachodzi podczas turbulizacji mieszaniny gazów i odpowiednio podczas turbulencji czoła płomienia. Turbulizacja powoduje znaczne rozszerzenie frontu płomienia, przyspieszenie wymiany ciepła między produktami spalania a mieszanką początkową i odpowiednio spalanie. Takie spalanie jest często nazywane wybuchem.
7.5. Warunki wybuchu.
Jak dowiedzieliśmy się wcześniej, eksplozja to chemiczna lub fizyczna przemiana substancji, której towarzyszy niezwykle szybkie przejście jej energii w energię ściskania i ruchu substancji wyjściowych, produktów ich przemian oraz środowiska. Wychodząc z tego wybuch chemiczny jest niezwykle szybką reakcją spalania, której towarzyszy gwałtowne przejście uwolnionej energii cieplnej w energię kompresji i ruchu substancji wyjściowych, produktów spalania i środowiska.
Eksplozja składa się z trzech etapów:
1) zamiana energii chemicznej reakcji na energię cieplną;
2) konwersję energii cieplnej na energię gazu wysokosprężonego;
3) rozchodzenie się sprężonego gazu w postaci fali uderzeniowej.
Głównymi warunkami wystąpienia reakcji chemicznej w postaci wybuchu są:
1. egzoterma, co wynika z faktu, że siła wiązań między atomami w produktach reakcji jest znacznie wyższa niż w substancjach wyjściowych, a więc uwalniana jest „dodatkowa” energia. W przypadku reakcji endotermicznych nie dochodzi do wybuchu.
2. Powstawanie gazu, ponieważ:
Po pierwsze, przejście do stanu gazowego podczas reakcji chemicznej dowolnych substancji w stałej objętości prowadzi do wzrostu ciśnienia;
Po drugie, gazy mają bardzo wysoki współczynnik rozszerzalności objętościowej po podgrzaniu. Bez obecności gazów nastąpi tylko ogrzewanie substancji.
3. Wysoka szybkość reakcji i jej zdolność do samopropagacji i samoakceleracji. Samopropagacja następuje w wyniku „fali” termicznej wywołanej przewodnictwem cieplnym (wybuch deflagracji) lub fali uderzeniowej sprężonych gazów (detonacja).
„Fala” termiczna jest podtrzymywana przez ciepło uwalniane podczas spalania, a fala uderzeniowa jest podtrzymywana przez sam sprężony gaz.
Autoprzyspieszenie reakcji i wystąpienie wybuchu następuje w wyniku wzrostu temperatury reagujących substancji pod wpływem ciepła reakcji lub wzrostu aktywnych rodników lub wzrostu ciśnienia fali uderzeniowej.
Spalanie mieszaniny gazów w zamkniętych rurach generuje echo, które prowadzi do całkowitego przestawienia czoła płomienia. Szczegóły tego zjawiska zostały po raz pierwszy odtworzone w symulacjach numerycznych.
Płomień wchodzący w interakcję z potężną falą dźwiękową może generować ciekawe struktury przestrzenne (patrz na przykład imponujący film z „wizualizacją ognia” fal dźwiękowych). W tym przypadku fala dźwiękowa nie musi być zewnętrzna: intensywne spalanie mieszanki gazowej paliwa i utleniacza w zamkniętej objętości np. w rurach generuje echo, które może zniekształcić front płomienia i zmienić tryb reakcji spalania .
Zniekształcenie kształtu płomienia podczas spalania w rurach znane jest od ponad stu lat, ale dopiero w klasycznych eksperymentach Jeffreya Sirby'ego (G. Searby) z 1992 roku przeprowadzono systematyczne badanie tego procesu. W szczególności Sirby obserwował turbulencje płomienia pod wpływem własnego echa. Samo w sobie zjawisko to nie wydaje się zaskakujące, ale teoretyczny opis tego procesu nie został jeszcze zaproponowany. Pytania, na które należało odpowiedzieć, brzmiały: „Jak dokładnie zachodzi przejście w turbulencje?”, „Jakie oscylacje płomienia zaczynają się najpierw?” itd. Wszystko to z kolei skutkowało skrępowaniem rąk badaczy poszukujących praktycznych zastosowań tego efektu w technice (ogólnie rzecz biorąc, turbulencja płomieni ma ogromne znaczenie dla przemysłu rakietowego).
Niedawny artykuł rosyjsko-szwedzkiego zespołu badawczego A. Petchenko i in., Physical Review Letters, 97, 164501 (19 października 2006) zrobił pierwszy krok w kierunku skonstruowania takiej teorii. Autorzy niniejszej pracy przeprowadzili szczegółową symulację numeryczną procesu spalania mieszanki gazowej w długiej i bardzo wąskiej rurze zamkniętej z jednej strony (mieszanina zapalała się od otwartego końca, a płomień rozprzestrzeniał się w głąb rury ). Dla uproszczenia obliczeń rozwiązano problem dwuwymiarowy, a nie trójwymiarowy, mieszaninę gazową uznano za gaz doskonały, a proces spalania modelowano za pomocą hipotetycznej jednostopniowej i nieodwracalnej reakcji chemicznej z zadanym wydzielaniem ciepła i aktywacją energia. Ale wszystkie gazy i termodynamika - sprężanie i rozszerzanie, przepływy gazu, wymiana ciepła, struktura czoła płomienia - zostały w pełni uwzględnione.
Wyniki symulacji jednoznacznie wykazały, że w miarę zbliżania się do zamkniętego końca front płomienia zaczął „drżeć”. Z tego drżenia wyrosło echo dźwiękowe o tej samej częstotliwości, które jeszcze bardziej „rozkołysało” płomień. W bezpośrednim sąsiedztwie końca rury oscylacje płomienia stały się tak silne, że czoło płomienia dosłownie złożyło się w akordeon. W każdym okresie tych oscylacji czoło płomienia gwałtownie destabilizowało, uwalniając wąski i bardzo długi strumień zimnego gazu do obszaru zajmowanego przez gorące produkty spalania. Strumień szybko się wypalił, front płomieni zamienił się w trąbę powietrzną, a następnie ponownie się wyrównał. Prędkość prądów generowanych przez te oscylacje wynosi dziesięć razy przekroczył „normalną” prędkość rozprzestrzeniania się płomienia w otwartej przestrzeni.
Silne oscylacje i generowane przez nie zawirowania są zwykle pierwszym etapem przejścia w turbulencje. Autorzy artykułu nie spieszą się jednak z ogłoszeniem odkrycia mechanizmu turbulencji płomienia. Faktem jest, że dostępna dziś moc obliczeniowa pozwala na przeprowadzenie tak szczegółowego modelowania tylko w bardzo wąskich rurach, a raczej w kapilarach. Jak ten proces będzie się zmieniał w rurach szerokich, dla których uzyskano dane eksperymentalne i w których wpływ ścian na przepływ jest znacznie słabszy, pozostaje do zbadania. Interesujące jest również sprawdzenie, czy zniekształcenia płomienia znalezione w symulacji są tym samym „płomieniem tulipana”, który był obserwowany od dłuższego czasu, ale nadal pozostaje niewyjaśniony (patrz C. Clanet i G. Searby. O „Płomieniu tulipana” Zjawisko (PDF, 1,3 Mb) // Spalanie i płomień, 1996. V. 105. P. 225-238).