ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು. ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳ ವಿಧಗಳು ಬೆಂಜೀನ್ ರಿಂಗ್ನಲ್ಲಿನ ಬದಲಿಗಳ ವಿಭಾಗವನ್ನು ಎರಡು ವಿಧಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ
ಇದನ್ನೂ ಓದಿ
) ಮತ್ತೊಂದು ರಾಸಾಯನಿಕ ಸಂಯುಕ್ತದ ಬಂಧಗಳು. ಸಂಪರ್ಕದ ಮೂಲಕ ಸಂಪರ್ಕವನ್ನು ಕೈಗೊಳ್ಳಬಹುದು ಕಾರ್ಬನ್-ಕಾರ್ಬನ್, ಮತ್ತು ಸಂವಹನದ ಮೂಲಕ ಕಾರ್ಬನ್ ಹೆಟೆರೊಟಾಮ್. ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಇಂಗ್ಲಿಷ್ ಅಕ್ಷರಗಳಿಂದ ಸೂಚಿಸಲಾಗುತ್ತದೆ "ಜಾಹೀರಾತು".
ಬಾಂಡ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಾಮಾನ್ಯ ನೋಟ ಕಾರ್ಬನ್-ಕಾರ್ಬನ್:
ಬಾಂಡ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಾಮಾನ್ಯ ನೋಟ ಇಂಗಾಲ-ಆಮ್ಲಜನಕ:
ವಿಶಿಷ್ಟವಾಗಿ, ಸೇರ್ಪಡೆ ಸಂಭವಿಸುವ ಕಾರಕವನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ತಲಾಧಾರ, ಮತ್ತು ಇತರ ( "X-Y") - ಆಕ್ರಮಣಕಾರಿ ಕಾರಕ.
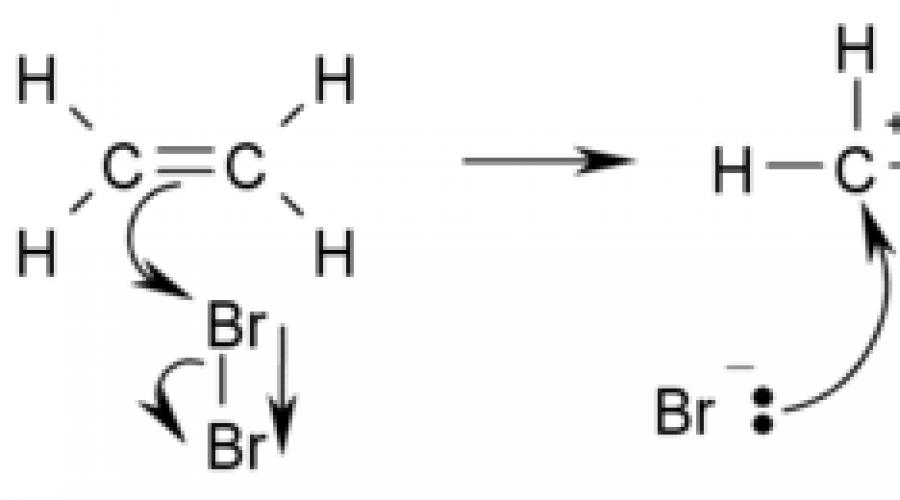
ಎಥಿಲೀನ್ನ ಬ್ರೋಮಿನೇಷನ್ ಒಂದು ಸಂಕಲನ ಕ್ರಿಯೆಯ ಉದಾಹರಣೆಯಾಗಿದೆ:

ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳೊಂದಿಗೆ ಜೋಡಿಸಿದಾಗ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಹಿಂತಿರುಗಿಸಲ್ಪಡುತ್ತವೆ, ಆದ್ದರಿಂದ ಅಂತಹ "ಜೋಡಿ" ಸೇರ್ಪಡೆ-ನಿರ್ಮೂಲನ ಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನವು ಸಾಮಾನ್ಯವಾಗಿದೆ ಎಂದು ನೆನಪಿನಲ್ಲಿಡಬೇಕು.
ಆಕ್ರಮಣಕಾರಿ ಕಣದ ಸ್ವರೂಪ ಮತ್ತು ಪ್ರತಿಕ್ರಿಯೆ ಕಾರ್ಯವಿಧಾನವನ್ನು ಅವಲಂಬಿಸಿ, ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್, ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್, ರಾಡಿಕಲ್ ಅಥವಾ ಸಿಂಕ್ರೊನಸ್ ಸೇರ್ಪಡೆಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗುತ್ತದೆ.
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಆಕ್ರಮಣಕಾರಿ ಕಣವು ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ ಆಗಿದೆ, ಅಂದರೆ ಋಣಾತ್ಮಕ ಆವೇಶದ ಕಣ ಅಥವಾ ಉಚಿತ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿ ಹೊಂದಿರುವ ಕಣ.
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಾಮಾನ್ಯ ನೋಟ:
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಗೊತ್ತುಪಡಿಸಲಾಗಿದೆ "ಆಡ್ ಎನ್".
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಬಂಧ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು C=Cಸಾಕಷ್ಟು ಅಪರೂಪ, ಅತ್ಯಂತ ವ್ಯಾಪಕ ಮತ್ತು ಪ್ರಾಯೋಗಿಕ ಮಹತ್ವವು ಸಂವಹನದ ಮೂಲಕ ಸಂಪರ್ಕವಾಗಿದೆ C=O :
ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಮೇಲಿನ ಎರಡು-ಹಂತದ ಬೈಮೋಲಿಕ್ಯುಲರ್ ಕಾರ್ಯವಿಧಾನವು ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿದೆ ಜಾಹೀರಾತು ಎನ್ 2: ಮೊದಲನೆಯದಾಗಿ, ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ ನಿಧಾನವಾಗಿ ಬಹು ಬಂಧದ ಜೊತೆಗೆ ಕಾರ್ಬನಿಯನ್ ಅನ್ನು ರೂಪಿಸುತ್ತದೆ, ಇದು ಎರಡನೇ ಹಂತದಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಜಾತಿಯಿಂದ ತ್ವರಿತವಾಗಿ ಆಕ್ರಮಣಗೊಳ್ಳುತ್ತದೆ.
ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಆಕ್ರಮಣಕಾರಿ ಕಣವಾಗಿದೆ ಎಲೆಕ್ಟ್ರೋಫೈಲ್, ಅಂದರೆ, ಧನಾತ್ಮಕ ಆವೇಶದ ಕಣ, ಹೆಚ್ಚಾಗಿ ಪ್ರೋಟಾನ್ H+, ಅಥವಾ ಎಲೆಕ್ಟ್ರಾನ್ ಕೊರತೆಯ ಕಣ.
ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಸಾಮಾನ್ಯ ನೋಟ:
ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಗೊತ್ತುಪಡಿಸಲಾಗಿದೆ "ಜಾಹೀರಾತು ಇ".
ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಅಪರ್ಯಾಪ್ತ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳಲ್ಲಿ ವ್ಯಾಪಕವಾಗಿ ಹರಡಿವೆ: ಆಲ್ಕೀನ್ಗಳು, ಆಲ್ಕೈನ್ಗಳು ಮತ್ತು ಡೈನ್ಗಳು.
ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಉದಾಹರಣೆಯೆಂದರೆ ಆಲ್ಕೀನ್ಗಳ ಜಲಸಂಚಯನ:
ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಬಂಧ ಕಾರ್ಬನ್ ಹೆಟೆರೊಟಾಮ್ಇದು ತುಂಬಾ ಸಾಮಾನ್ಯವಾಗಿದೆ ಮತ್ತು ಹೆಚ್ಚಾಗಿ ಅಂತಹ ಸಂಪರ್ಕವಾಗಿದೆ C=O:



ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಮೇಲಿನ ಎರಡು-ಹಂತದ ಬೈಮೋಲಿಕ್ಯುಲರ್ ಕಾರ್ಯವಿಧಾನವು ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿದೆ. ಜಾಹೀರಾತು ಇ 2: ಮೊದಲನೆಯದಾಗಿ, ಎಲೆಕ್ಟ್ರೋಫೈಲ್ ನಿಧಾನವಾಗಿ ಬಹು ಬಂಧದಲ್ಲಿ ಸೇರಿಕೊಂಡು ಕಾರ್ಬೋಕೇಶನ್ ಅನ್ನು ರೂಪಿಸುತ್ತದೆ, ಇದು ಎರಡನೇ ಹಂತದಲ್ಲಿ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ದಾಳಿಗೆ ಒಳಗಾಗುತ್ತದೆ.
ಆಮೂಲಾಗ್ರ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಆಮೂಲಾಗ್ರ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಆಕ್ರಮಣಕಾರಿ ಕಣವು ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಆಗಿದೆ.
ಆಮೂಲಾಗ್ರ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಗೊತ್ತುಪಡಿಸಲಾಗಿದೆ "ಜಾಹೀರಾತು ಆರ್".
ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಮೂಲದ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಬದಲಿಗೆ ಮೂಲಭೂತ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಸಂಭವಿಸುತ್ತವೆ:

ಸಿಂಕ್ರೊನಸ್ ಸೇರುವ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಕೆಲವು ಸಂದರ್ಭಗಳಲ್ಲಿ, ಬಹು ಬಂಧದ ಮೂಲಕ ಸೇರುವುದು ಎರಡೂ ಪರಮಾಣುಗಳ ಮೇಲೆ ಏಕಕಾಲಿಕ ದಾಳಿಯೊಂದಿಗೆ ಸಂಭವಿಸುತ್ತದೆ, ಇದು ದಾಳಿಯ ಆದ್ಯತೆಯನ್ನು ನಿರ್ಧರಿಸಲು ಅಸಾಧ್ಯವಾಗುತ್ತದೆ. ಈ ಕಾರ್ಯವಿಧಾನವನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ಸಿಂಕ್ರೊನಸ್ ಸಂಪರ್ಕ. ಸಿಂಕ್ರೊನಸ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಆವರ್ತಕ ಉತ್ಪನ್ನಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತವೆ, ಅದಕ್ಕಾಗಿಯೇ ಅವುಗಳನ್ನು ಹೆಚ್ಚಾಗಿ ಕರೆಯಲಾಗುತ್ತದೆ ಸೈಕ್ಲೋಡಿಷನ್.
ಟಿಪ್ಪಣಿಗಳು
| ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು | |
|---|---|
| ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು | ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಮೂಲಭೂತ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು |
| ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು | ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಮೂಲಭೂತ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸಿಂಕ್ರೊನಸ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು |
| ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು | ಹೆಟೆರೊಲೈಟಿಕ್ ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಪೆರಿಸೈಕ್ಲಿಕ್ ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಆಮೂಲಾಗ್ರ ನಿರ್ಮೂಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳು |
| ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಮರುಸಂಘಟಿಸುವುದು | ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಮರುಜೋಡಣೆಗಳು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಮರುಜೋಡಣೆಗಳು ಮೂಲಭೂತ ಮರುಜೋಡಣೆಗಳು |
| ಆಕ್ಸಿಡೀಕರಣ ಮತ್ತು ಕಡಿತ ಪ್ರತಿಕ್ರಿಯೆಗಳು | ಆಕ್ಸಿಡೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಕಡಿತ ಪ್ರತಿಕ್ರಿಯೆಗಳು |
| ಇತರೆ | ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಹೆಸರಿಸಲಾಗಿದೆ |
ವಿಕಿಮೀಡಿಯಾ ಫೌಂಡೇಶನ್. 2010.
ಇತರ ನಿಘಂಟುಗಳಲ್ಲಿ "ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು" ಏನೆಂದು ನೋಡಿ:
ಸೇರ್ಪಡೆ ಕ್ರಿಯೆಯಿಂದ ಉತ್ಪತ್ತಿಯಾಗುವ ಪಾಲಿಮರ್- — EN ಸಂಕಲನ ಪಾಲಿಮರ್ ಒಲೆಫಿನ್ಗಳಂತಹ ಅಪರ್ಯಾಪ್ತ ಮಾನೋಮರ್ ಅಣುಗಳ ಸರಪಳಿ ಸೇರ್ಪಡೆಯಿಂದ ರೂಪುಗೊಂಡ ಪಾಲಿಮರ್, ಒಂದು ಉತ್ಪನ್ನದ ರಚನೆಯಿಲ್ಲದೆ ಒಂದಕ್ಕೊಂದು ನೀರಿನಂತೆ;... ... ತಾಂತ್ರಿಕ ಅನುವಾದಕರ ಮಾರ್ಗದರ್ಶಿ
- (ಇಂಗ್ಲಿಷ್ ಸೇರ್ಪಡೆ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ರಿಯಾಕ್ಷನ್) ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಇದರಲ್ಲಿ ಆರಂಭಿಕ ಹಂತದಲ್ಲಿ ದಾಳಿಯನ್ನು ಧನಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ ಮಾಡಲಾದ ಅಥವಾ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಕೊರತೆಯನ್ನು ಹೊಂದಿರುವ ಎಲೆಕ್ಟ್ರೋಫೈಲ್ ಕಣದಿಂದ ನಡೆಸಲಾಗುತ್ತದೆ. ಅಂತಿಮ ಹಂತದಲ್ಲಿ, ಪರಿಣಾಮವಾಗಿ... ... ವಿಕಿಪೀಡಿಯಾ
- (ಇಂಗ್ಲಿಷ್ ಸೇರ್ಪಡೆ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಪ್ರತಿಕ್ರಿಯೆ) ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಇದರಲ್ಲಿ ಆರಂಭಿಕ ಹಂತದಲ್ಲಿ ದಾಳಿಯನ್ನು ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ ಕಣದಿಂದ ನಡೆಸಲಾಗುತ್ತದೆ, ಅದು ಋಣಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ ಆಗಿರುತ್ತದೆ ಅಥವಾ ಉಚಿತ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯನ್ನು ಹೊಂದಿರುತ್ತದೆ. ಅಂತಿಮ ಹಂತದಲ್ಲಿ, ಪರಿಣಾಮವಾಗಿ... ... ವಿಕಿಪೀಡಿಯಾ
- (ಇಂಗ್ಲಿಷ್ ಸೇರ್ಪಡೆ ಆಮೂಲಾಗ್ರ ಪ್ರತಿಕ್ರಿಯೆ) ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಇದರಲ್ಲಿ ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳು, ಒಂದು ಅಥವಾ ಹೆಚ್ಚು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಕಣಗಳಿಂದ ದಾಳಿಯನ್ನು ನಡೆಸಲಾಗುತ್ತದೆ. ಅದೇ ಸಮಯದಲ್ಲಿ, ರಾಡಿಕಲ್ಗಳು ಇತರ ರಾಡಿಕಲ್ಗಳ ಮೇಲೆ ದಾಳಿ ಮಾಡಬಹುದು ಮತ್ತು... ... ವಿಕಿಪೀಡಿಯಾ
ಬಹು ಬಂಧದ ಎರಡೂ ಪರಮಾಣುಗಳು ಏಕಕಾಲದಲ್ಲಿ ದಾಳಿ ಮಾಡುವ ಸಂಕಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳು. ಈ ರೀತಿಯ ಪ್ರತಿಕ್ರಿಯೆಯ ಮತ್ತೊಂದು ಹೆಸರು ಸೈಕ್ಲೋಡಿಷನ್ ಪ್ರತಿಕ್ರಿಯೆ, ಏಕೆಂದರೆ ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಅಂತಿಮ ಉತ್ಪನ್ನವು ಆವರ್ತಕ ತಲಾಧಾರಗಳು. ಎರಡು ಇವೆ... ... ವಿಕಿಪೀಡಿಯಾ
- (eng. ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಬದಲಿ ಪ್ರತಿಕ್ರಿಯೆ) ಬದಲಿ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಇದರಲ್ಲಿ ಏಕಾಂಗಿ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯನ್ನು ಹೊತ್ತಿರುವ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಕಾರಕದಿಂದ ದಾಳಿಯನ್ನು ನಡೆಸಲಾಗುತ್ತದೆ. ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ ಹೊರಹೋಗುವ ಗುಂಪನ್ನು ನ್ಯೂಕ್ಲಿಯೊಫ್ಯೂಜ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಎಲ್ಲವೂ... ವಿಕಿಪೀಡಿಯಾ
ಸಾವಯವ ಪದಾರ್ಥಗಳ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಔಪಚಾರಿಕವಾಗಿ ನಾಲ್ಕು ಮುಖ್ಯ ವಿಧಗಳಾಗಿ ವಿಂಗಡಿಸಬಹುದು: ಪರ್ಯಾಯ, ಸೇರ್ಪಡೆ, ನಿರ್ಮೂಲನೆ (ನಿರ್ಮೂಲನೆ) ಮತ್ತು ಮರುಜೋಡಣೆ (ಐಸೋಮರೈಸೇಶನ್). ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಸಂಪೂರ್ಣ ವೈವಿಧ್ಯಮಯ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಪ್ರಸ್ತಾವಿತ ವರ್ಗೀಕರಣಕ್ಕೆ ಕಡಿಮೆ ಮಾಡಲಾಗುವುದಿಲ್ಲ ಎಂಬುದು ಸ್ಪಷ್ಟವಾಗಿದೆ (ಉದಾಹರಣೆಗೆ, ದಹನ ಪ್ರತಿಕ್ರಿಯೆಗಳು). ಆದಾಗ್ಯೂ, ಅಂತಹ ವರ್ಗೀಕರಣವು ನಿಮಗೆ ಈಗಾಗಲೇ ತಿಳಿದಿರುವ ಅಜೈವಿಕ ಪದಾರ್ಥಗಳ ನಡುವೆ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಗಳೊಂದಿಗೆ ಸಾದೃಶ್ಯಗಳನ್ನು ಸ್ಥಾಪಿಸಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ.
ವಿಶಿಷ್ಟವಾಗಿ, ಪ್ರತಿಕ್ರಿಯೆಯಲ್ಲಿ ಒಳಗೊಂಡಿರುವ ಮುಖ್ಯ ಸಾವಯವ ಸಂಯುಕ್ತವನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ತಲಾಧಾರ, ಮತ್ತು ಇತರ ಪ್ರತಿಕ್ರಿಯೆ ಘಟಕವನ್ನು ಸಾಂಪ್ರದಾಯಿಕವಾಗಿ ಪರಿಗಣಿಸಲಾಗುತ್ತದೆ ಕಾರಕ.
ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು- ಇವುಗಳು ಮೂಲ ಅಣುವಿನಲ್ಲಿ (ತಲಾಧಾರ) ಒಂದು ಪರಮಾಣು ಅಥವಾ ಪರಮಾಣುಗಳ ಗುಂಪನ್ನು ಇತರ ಪರಮಾಣುಗಳು ಅಥವಾ ಪರಮಾಣುಗಳ ಗುಂಪುಗಳೊಂದಿಗೆ ಬದಲಾಯಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಗಳಾಗಿವೆ.
ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸ್ಯಾಚುರೇಟೆಡ್ ಮತ್ತು ಆರೊಮ್ಯಾಟಿಕ್ ಸಂಯುಕ್ತಗಳಾದ ಆಲ್ಕೇನ್ಗಳು, ಸೈಕ್ಲೋಲ್ಕೇನ್ಗಳು ಅಥವಾ ಅರೀನ್ಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತವೆ. ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಉದಾಹರಣೆಗಳನ್ನು ನೀಡೋಣ.
ಬೆಳಕಿನ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ, ಮೀಥೇನ್ ಅಣುವಿನಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣುಗಳಿಂದ ಬದಲಾಯಿಸಬಹುದು, ಉದಾಹರಣೆಗೆ, ಕ್ಲೋರಿನ್ ಪರಮಾಣುಗಳಿಂದ:
ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಹ್ಯಾಲೊಜೆನ್ನೊಂದಿಗೆ ಬದಲಿಸುವ ಇನ್ನೊಂದು ಉದಾಹರಣೆಯೆಂದರೆ ಬೆಂಜೀನ್ ಅನ್ನು ಬ್ರೋಮೊಬೆಂಜೀನ್ ಆಗಿ ಪರಿವರ್ತಿಸುವುದು:

ಈ ಪ್ರತಿಕ್ರಿಯೆಯ ಸಮೀಕರಣವನ್ನು ವಿಭಿನ್ನವಾಗಿ ಬರೆಯಬಹುದು:
![]()
ಈ ರೀತಿಯ ಬರವಣಿಗೆಯೊಂದಿಗೆ, ಕಾರಕಗಳು, ವೇಗವರ್ಧಕ ಮತ್ತು ಪ್ರತಿಕ್ರಿಯೆ ಪರಿಸ್ಥಿತಿಗಳನ್ನು ಬಾಣದ ಮೇಲೆ ಬರೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ಅಜೈವಿಕ ಪ್ರತಿಕ್ರಿಯೆ ಉತ್ಪನ್ನಗಳನ್ನು ಅದರ ಕೆಳಗೆ ಬರೆಯಲಾಗುತ್ತದೆ.
ಪ್ರತಿಕ್ರಿಯೆಗಳ ಪರಿಣಾಮವಾಗಿ ಸಾವಯವ ಪದಾರ್ಥಗಳಲ್ಲಿನ ಪರ್ಯಾಯಗಳು ಸರಳ ಮತ್ತು ಸಂಕೀರ್ಣವಾಗಿಲ್ಲ ಅಜೈವಿಕ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿರುವಂತೆ ಪದಾರ್ಥಗಳು ಮತ್ತು ಎರಡು ಸಂಕೀರ್ಣ ಪದಾರ್ಥಗಳು.
ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು- ಇವುಗಳು ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕ ಪದಾರ್ಥಗಳ ಎರಡು ಅಥವಾ ಹೆಚ್ಚಿನ ಅಣುಗಳನ್ನು ಒಂದಾಗಿ ಸಂಯೋಜಿಸುವ ಪರಿಣಾಮವಾಗಿ ಪ್ರತಿಕ್ರಿಯೆಗಳಾಗಿವೆ.
ಆಲ್ಕೀನ್ಗಳು ಅಥವಾ ಆಲ್ಕೈನ್ಗಳಂತಹ ಅಪರ್ಯಾಪ್ತ ಸಂಯುಕ್ತಗಳು ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುತ್ತವೆ. ಯಾವ ಅಣುವು ಕಾರಕವಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ ಎಂಬುದರ ಆಧಾರದ ಮೇಲೆ, ಹೈಡ್ರೋಜನೀಕರಣ (ಅಥವಾ ಕಡಿತ), ಹ್ಯಾಲೊಜೆನೇಶನ್, ಹೈಡ್ರೊಹಾಲೊಜೆನೇಶನ್, ಜಲಸಂಚಯನ ಮತ್ತು ಇತರ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗುತ್ತದೆ. ಅವುಗಳಲ್ಲಿ ಪ್ರತಿಯೊಂದಕ್ಕೂ ಕೆಲವು ಷರತ್ತುಗಳು ಬೇಕಾಗುತ್ತವೆ.
1.ಹೈಡ್ರೋಜನೀಕರಣ- ಬಹು ಬಂಧದ ಮೂಲಕ ಹೈಡ್ರೋಜನ್ ಅಣುವಿನ ಸೇರ್ಪಡೆಯ ಪ್ರತಿಕ್ರಿಯೆ:
2. ಹೈಡ್ರೋಹಲೋಜೆನೇಶನ್- ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆ (ಹೈಡ್ರೋಕ್ಲೋರಿನೇಶನ್):
3. ಹ್ಯಾಲೊಜೆನೇಶನ್- ಹ್ಯಾಲೊಜೆನ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆ:
![]()
4.ಪಾಲಿಮರೀಕರಣ- ಒಂದು ವಿಶೇಷ ರೀತಿಯ ಸಂಕಲನ ಕ್ರಿಯೆ, ಇದರಲ್ಲಿ ಸಣ್ಣ ಆಣ್ವಿಕ ತೂಕವನ್ನು ಹೊಂದಿರುವ ವಸ್ತುವಿನ ಅಣುಗಳು ಒಂದಕ್ಕೊಂದು ಸೇರಿಕೊಂಡು ಅತಿ ಹೆಚ್ಚಿನ ಆಣ್ವಿಕ ತೂಕವನ್ನು ಹೊಂದಿರುವ ವಸ್ತುವಿನ ಅಣುಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ - ಮ್ಯಾಕ್ರೋಮಾಲಿಕ್ಯೂಲ್ಗಳು.
ಪಾಲಿಮರೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಕಡಿಮೆ ಆಣ್ವಿಕ ತೂಕದ ವಸ್ತುವಿನ (ಮೊನೊಮರ್) ಅನೇಕ ಅಣುಗಳನ್ನು ಪಾಲಿಮರ್ನ ದೊಡ್ಡ ಅಣುಗಳಾಗಿ (ಮ್ಯಾಕ್ರೋಮಾಲಿಕ್ಯೂಲ್ಗಳು) ಸಂಯೋಜಿಸುವ ಪ್ರಕ್ರಿಯೆಗಳಾಗಿವೆ.
ಪಾಲಿಮರೀಕರಣ ಕ್ರಿಯೆಯ ಒಂದು ಉದಾಹರಣೆಯೆಂದರೆ, ನೇರಳಾತೀತ ವಿಕಿರಣದ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ಎಥಿಲೀನ್ (ಇಥೀನ್) ನಿಂದ ಪಾಲಿಎಥಿಲಿನ್ ಉತ್ಪಾದನೆ ಮತ್ತು ಆಮೂಲಾಗ್ರ ಪಾಲಿಮರೀಕರಣ ಇನಿಶಿಯೇಟರ್ ಆರ್.
ಪರಮಾಣು ಕಕ್ಷೆಗಳು ಅತಿಕ್ರಮಿಸಿದಾಗ ಮತ್ತು ಹಂಚಿಕೆಯ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಗಳ ರಚನೆಯಾದಾಗ ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಅತ್ಯಂತ ವಿಶಿಷ್ಟವಾದ ಕೋವೆಲನ್ಸಿಯ ಬಂಧವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ. ಇದರ ಪರಿಣಾಮವಾಗಿ, ಎರಡು ಪರಮಾಣುಗಳಿಗೆ ಸಾಮಾನ್ಯವಾದ ಕಕ್ಷೆಯು ರೂಪುಗೊಳ್ಳುತ್ತದೆ, ಇದರಲ್ಲಿ ಸಾಮಾನ್ಯ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿ ಇದೆ. ಬಂಧವನ್ನು ಮುರಿದಾಗ, ಈ ಹಂಚಿಕೆಯ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಭವಿಷ್ಯವು ವಿಭಿನ್ನವಾಗಿರುತ್ತದೆ.
ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕ ಕಣಗಳ ವಿಧಗಳು
ಒಂದು ಪರಮಾಣುವಿಗೆ ಸೇರಿದ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ನೊಂದಿಗಿನ ಕಕ್ಷೆಯು ಮತ್ತೊಂದು ಪರಮಾಣುವಿನ ಕಕ್ಷೆಯೊಂದಿಗೆ ಅತಿಕ್ರಮಿಸಬಹುದು, ಅದು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಸಹ ಹೊಂದಿರುತ್ತದೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನದ ಪ್ರಕಾರ ಕೋವೆಲನ್ಸಿಯ ಬಂಧವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ:
ವಿಭಿನ್ನ ಪರಮಾಣುಗಳಿಗೆ ಸೇರಿದ ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ಸಾಮಾನ್ಯ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯು ರೂಪುಗೊಂಡರೆ ಕೋವೆಲನ್ಸಿಯ ಬಂಧದ ರಚನೆಗೆ ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನವನ್ನು ಅರಿತುಕೊಳ್ಳಲಾಗುತ್ತದೆ.
ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನದಿಂದ ಕೋವೆಲನ್ಸಿಯ ಬಂಧದ ರಚನೆಗೆ ವಿರುದ್ಧವಾದ ಪ್ರಕ್ರಿಯೆಯು ಬಂಧದ ಸೀಳಾಗಿದೆ, ಇದರಲ್ಲಿ ಪ್ರತಿ ಪರಮಾಣುವಿಗೆ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಕಳೆದುಹೋಗುತ್ತದೆ (). ಇದರ ಪರಿಣಾಮವಾಗಿ, ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಎರಡು ಚಾರ್ಜ್ ಆಗದ ಕಣಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ:
![]()
ಅಂತಹ ಕಣಗಳನ್ನು ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಮುಕ್ತ ಮೂಲಭೂತಗಳು- ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಪರಮಾಣುಗಳು ಅಥವಾ ಪರಮಾಣುಗಳ ಗುಂಪುಗಳು.
ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಪ್ರತಿಕ್ರಿಯೆಗಳು- ಇವುಗಳು ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಮತ್ತು ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳ ಭಾಗವಹಿಸುವಿಕೆಯೊಂದಿಗೆ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಗಳಾಗಿವೆ.
ಅಜೈವಿಕ ರಸಾಯನಶಾಸ್ತ್ರದ ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ, ಇವುಗಳು ಆಮ್ಲಜನಕ, ಹ್ಯಾಲೊಜೆನ್ಗಳು ಮತ್ತು ದಹನ ಕ್ರಿಯೆಗಳೊಂದಿಗೆ ಹೈಡ್ರೋಜನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳಾಗಿವೆ. ಈ ಪ್ರಕಾರದ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಹೆಚ್ಚಿನ ವೇಗ ಮತ್ತು ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದ ಶಾಖದ ಬಿಡುಗಡೆಯಿಂದ ನಿರೂಪಿಸಲ್ಪಡುತ್ತವೆ.
ದಾನಿ-ಸ್ವೀಕರಿಸುವ ಕಾರ್ಯವಿಧಾನದಿಂದ ಕೋವೆಲನ್ಸಿಯ ಬಂಧವನ್ನು ಸಹ ರಚಿಸಬಹುದು. ಒಂಟಿಯಾದ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಪರಮಾಣುವಿನ (ಅಥವಾ ಅಯಾನ್) ಕಕ್ಷೆಗಳಲ್ಲಿ ಒಂದಾದ ಮತ್ತೊಂದು ಪರಮಾಣುವಿನ (ಅಥವಾ ಕ್ಯಾಶನ್) ಆಕ್ರಮಿಸದ ಕಕ್ಷೆಯೊಂದಿಗೆ ಅತಿಕ್ರಮಿಸುತ್ತದೆ ಮತ್ತು ಅದು ಆಕ್ರಮಿಸದ ಕಕ್ಷೆಯನ್ನು ಹೊಂದಿದೆ ಮತ್ತು ಕೋವೆಲನ್ಸಿಯ ಬಂಧವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ, ಉದಾಹರಣೆಗೆ:
![]()
ಕೋವೆಲನ್ಸಿಯ ಬಂಧದ ಛಿದ್ರವು ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ ಆವೇಶದ ಕಣಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ (); ಈ ಸಂದರ್ಭದಲ್ಲಿ ಸಾಮಾನ್ಯ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯಿಂದ ಎರಡೂ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಒಂದು ಪರಮಾಣುಗಳೊಂದಿಗೆ ಉಳಿಯುತ್ತವೆ, ಇನ್ನೊಂದು ಪರಮಾಣು ತುಂಬದ ಕಕ್ಷೆಯನ್ನು ಹೊಂದಿರುತ್ತದೆ:
![]()
ಆಮ್ಲಗಳ ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಘಟನೆಯನ್ನು ಪರಿಗಣಿಸೋಣ:
![]()
ಒಂಟಿ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಕಣ R: -, ಅಂದರೆ ಋಣಾತ್ಮಕ ಆವೇಶದ ಅಯಾನು, ಧನಾತ್ಮಕ ಆವೇಶದ ಪರಮಾಣುಗಳಿಗೆ ಅಥವಾ ಕನಿಷ್ಠ ಭಾಗಶಃ ಅಥವಾ ಪರಿಣಾಮಕಾರಿ ಧನಾತ್ಮಕ ಚಾರ್ಜ್ ಇರುವ ಪರಮಾಣುಗಳಿಗೆ ಆಕರ್ಷಿತವಾಗುತ್ತದೆ ಎಂದು ಸುಲಭವಾಗಿ ಊಹಿಸಬಹುದು.
ಒಂಟಿ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಕಣಗಳನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಏಜೆಂಟ್ (ನ್ಯೂಕ್ಲಿಯಸ್- “ನ್ಯೂಕ್ಲಿಯಸ್”, ಪರಮಾಣುವಿನ ಧನಾತ್ಮಕ ಆವೇಶದ ಭಾಗ), ಅಂದರೆ ನ್ಯೂಕ್ಲಿಯಸ್ನ “ಸ್ನೇಹಿತರು”, ಧನಾತ್ಮಕ ಆವೇಶ.
ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಸ್(ನು) - ಪರಿಣಾಮಕಾರಿ ಧನಾತ್ಮಕ ಆವೇಶವನ್ನು ಹೊಂದಿರುವ ಅಣುಗಳ ಭಾಗಗಳೊಂದಿಗೆ ಸಂವಹನ ನಡೆಸುವ ಏಕೈಕ ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಅಯಾನುಗಳು ಅಥವಾ ಅಣುಗಳು.
ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳ ಉದಾಹರಣೆಗಳು: Cl - (ಕ್ಲೋರೈಡ್ ಅಯಾನ್), OH - (ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನ್), CH 3 O - (ಮೆಥಾಕ್ಸೈಡ್ ಅಯಾನ್), CH 3 COO - (ಅಸಿಟೇಟ್ ಅಯಾನ್).
ತುಂಬದ ಕಕ್ಷೆಯನ್ನು ಹೊಂದಿರುವ ಕಣಗಳು, ಇದಕ್ಕೆ ವಿರುದ್ಧವಾಗಿ, ಅದನ್ನು ತುಂಬಲು ಒಲವು ತೋರುತ್ತವೆ ಮತ್ತು ಆದ್ದರಿಂದ, ಹೆಚ್ಚಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಂದ್ರತೆ, ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ ಮತ್ತು ಒಂಟಿ ಎಲೆಕ್ಟ್ರಾನ್ ಜೋಡಿಯನ್ನು ಹೊಂದಿರುವ ಅಣುಗಳ ಭಾಗಗಳಿಗೆ ಆಕರ್ಷಿತವಾಗುತ್ತವೆ. ಅವು ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳು, ಎಲೆಕ್ಟ್ರಾನ್ನ "ಸ್ನೇಹಿತರು", ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ ಅಥವಾ ಹೆಚ್ಚಿದ ಎಲೆಕ್ಟ್ರಾನ್ ಸಾಂದ್ರತೆಯೊಂದಿಗೆ ಕಣಗಳು.
ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಸ್- ತುಂಬದ ಎಲೆಕ್ಟ್ರಾನ್ ಕಕ್ಷೆಯನ್ನು ಹೊಂದಿರುವ ಕ್ಯಾಟಯಾನುಗಳು ಅಥವಾ ಅಣುಗಳು, ಅದನ್ನು ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಲು ಒಲವು ತೋರುತ್ತವೆ, ಏಕೆಂದರೆ ಇದು ಪರಮಾಣುವಿನ ಹೆಚ್ಚು ಅನುಕೂಲಕರ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಸಂರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ.
ಯಾವುದೇ ಕಣವು ತುಂಬದ ಕಕ್ಷೆಯನ್ನು ಹೊಂದಿರುವ ಎಲೆಕ್ಟ್ರೋಫೈಲ್ ಅಲ್ಲ. ಉದಾಹರಣೆಗೆ, ಕ್ಷಾರೀಯ ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳು ಜಡ ಅನಿಲಗಳ ಸಂರಚನೆಯನ್ನು ಹೊಂದಿವೆ ಮತ್ತು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಪಡೆಯಲು ಒಲವು ಹೊಂದಿರುವುದಿಲ್ಲ, ಏಕೆಂದರೆ ಅವುಗಳು ಕಡಿಮೆ ಎಲೆಕ್ಟ್ರಾನ್ ಬಾಂಧವ್ಯ.
ಇದರಿಂದ ನಾವು ತುಂಬದ ಕಕ್ಷೆಯ ಉಪಸ್ಥಿತಿಯ ಹೊರತಾಗಿಯೂ, ಅಂತಹ ಕಣಗಳು ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳಾಗಿರುವುದಿಲ್ಲ ಎಂದು ನಾವು ತೀರ್ಮಾನಿಸಬಹುದು.
ಮೂಲ ಪ್ರತಿಕ್ರಿಯೆ ಕಾರ್ಯವಿಧಾನಗಳು
ಮೂರು ಮುಖ್ಯ ರೀತಿಯ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಕಣಗಳನ್ನು ಗುರುತಿಸಲಾಗಿದೆ - ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳು, ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳು, ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳು - ಮತ್ತು ಮೂರು ಅನುಗುಣವಾದ ಪ್ರತಿಕ್ರಿಯೆ ಕಾರ್ಯವಿಧಾನಗಳು:
- ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್;
- ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್;
- ಝೀರೋಫಿಲಿಕ್.
ಪ್ರತಿಕ್ರಿಯಿಸುವ ಕಣಗಳ ಪ್ರಕಾರದ ಪ್ರಕಾರ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ವರ್ಗೀಕರಿಸುವುದರ ಜೊತೆಗೆ, ಸಾವಯವ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಅಣುಗಳ ಸಂಯೋಜನೆಯನ್ನು ಬದಲಾಯಿಸುವ ತತ್ತ್ವದ ಪ್ರಕಾರ ನಾಲ್ಕು ರೀತಿಯ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ: ಸೇರ್ಪಡೆ, ಪರ್ಯಾಯ, ಬೇರ್ಪಡುವಿಕೆ ಅಥವಾ ಹೊರಹಾಕುವಿಕೆ (ಇಂಗ್ಲಿಷ್ನಿಂದ. ಗೆ ತೊಡೆದುಹಾಕಲು- ತೆಗೆದುಹಾಕಿ, ವಿಭಜಿಸಿ) ಮತ್ತು ಮರುಜೋಡಣೆ. ಎಲ್ಲಾ ಮೂರು ರೀತಿಯ ಪ್ರತಿಕ್ರಿಯಾತ್ಮಕ ಜಾತಿಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಸೇರ್ಪಡೆ ಮತ್ತು ಪರ್ಯಾಯವು ಸಂಭವಿಸಬಹುದು, ಹಲವಾರು ಪ್ರತ್ಯೇಕಿಸಬಹುದು ಮುಖ್ಯಪ್ರತಿಕ್ರಿಯೆಗಳ ಕಾರ್ಯವಿಧಾನಗಳು.


ಹೆಚ್ಚುವರಿಯಾಗಿ, ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಕಣಗಳ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಸಂಭವಿಸುವ ಎಲಿಮಿನೇಷನ್ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ನಾವು ಪರಿಗಣಿಸುತ್ತೇವೆ - ಬೇಸ್ಗಳು.
6. ನಿವಾರಣೆ:
ಆಲ್ಕೀನ್ಗಳ (ಅಪರ್ಯಾಪ್ತ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು) ಒಂದು ವಿಶಿಷ್ಟ ಲಕ್ಷಣವೆಂದರೆ ಅವುಗಳ ಸಂಕಲನ ಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುವ ಸಾಮರ್ಥ್ಯ. ಈ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ ಹೆಚ್ಚಿನವು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಕಾರ್ಯವಿಧಾನದಿಂದ ಮುಂದುವರಿಯುತ್ತದೆ.
ಹೈಡ್ರೊಹಾಲೊಜೆನೇಶನ್ (ಹ್ಯಾಲೊಜೆನ್ ಸೇರ್ಪಡೆ ಜಲಜನಕ):
ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ ಅನ್ನು ಆಲ್ಕೀನ್ಗೆ ಸೇರಿಸಿದಾಗ ಹೈಡ್ರೋಜನ್ ಹೆಚ್ಚು ಹೈಡ್ರೋಜನೀಕರಿಸಿದ ಒಂದಕ್ಕೆ ಸೇರಿಸುತ್ತದೆ ಕಾರ್ಬನ್ ಪರಮಾಣು, ಅಂದರೆ ಹೆಚ್ಚು ಪರಮಾಣುಗಳಿರುವ ಪರಮಾಣು ಹೈಡ್ರೋಜನ್, ಮತ್ತು ಹ್ಯಾಲೊಜೆನ್ - ಕಡಿಮೆ ಹೈಡ್ರೋಜನೀಕರಿಸಿದ ಗೆ.
ಆಲ್ಕೇನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಆಲ್ಕೇನ್ಗಳು (ಪ್ಯಾರಾಫಿನ್ಗಳು) ಸೈಕ್ಲಿಕ್ ಅಲ್ಲದ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳಾಗಿದ್ದು, ಅದರ ಅಣುಗಳಲ್ಲಿ ಎಲ್ಲಾ ಇಂಗಾಲದ ಪರಮಾಣುಗಳು ಒಂದೇ ಬಂಧಗಳಿಂದ ಮಾತ್ರ ಸಂಪರ್ಕ ಹೊಂದಿವೆ. ಬೇರೆ ರೀತಿಯಲ್ಲಿ ಹೇಳುವುದಾದರೆ, ಆಲ್ಕೇನ್ ಅಣುಗಳಲ್ಲಿ ಯಾವುದೇ ಬಹು - ಡಬಲ್ ಅಥವಾ ಟ್ರಿಪಲ್ ಬಂಧಗಳಿಲ್ಲ. ವಾಸ್ತವವಾಗಿ, ಆಲ್ಕೇನ್ಗಳು ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಗರಿಷ್ಠ ಸಂಭವನೀಯ ಸಂಖ್ಯೆಯ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ ಮತ್ತು ಆದ್ದರಿಂದ ಅವುಗಳನ್ನು ಸೀಮಿತಗೊಳಿಸುವಿಕೆ (ಸ್ಯಾಚುರೇಟೆಡ್) ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಶುದ್ಧತ್ವದಿಂದಾಗಿ, ಆಲ್ಕೇನ್ಗಳು ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುವುದಿಲ್ಲ.
ಇಂಗಾಲ ಮತ್ತು ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳು ತಕ್ಕಮಟ್ಟಿಗೆ ಎಲೆಕ್ಟ್ರೋನೆಜಿಟಿವಿಟಿಯನ್ನು ಹೊಂದಿರುವುದರಿಂದ, ಅವುಗಳ ಅಣುಗಳಲ್ಲಿನ C-H ಬಂಧಗಳು ಅತ್ಯಂತ ಕಡಿಮೆ-ಧ್ರುವೀಯವಾಗಿವೆ ಎಂಬ ಅಂಶಕ್ಕೆ ಇದು ಕಾರಣವಾಗುತ್ತದೆ. ಈ ನಿಟ್ಟಿನಲ್ಲಿ, ಆಲ್ಕೇನ್ಗಳಿಗೆ, S R ಚಿಹ್ನೆಯಿಂದ ಸೂಚಿಸಲಾದ ಆಮೂಲಾಗ್ರ ಪರ್ಯಾಯ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಮುಂದುವರಿಯುವ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಹೆಚ್ಚು ವಿಶಿಷ್ಟವಾಗಿರುತ್ತವೆ.
1. ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಈ ರೀತಿಯ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಕಾರ್ಬನ್-ಹೈಡ್ರೋಜನ್ ಬಂಧಗಳು ಮುರಿದುಹೋಗುತ್ತವೆ
RH + XY → RX + HY
ಹ್ಯಾಲೊಜೆನೇಶನ್
ನೇರಳಾತೀತ ಬೆಳಕು ಅಥವಾ ಹೆಚ್ಚಿನ ಶಾಖಕ್ಕೆ ಒಡ್ಡಿಕೊಂಡಾಗ ಆಲ್ಕೇನ್ಗಳು ಹ್ಯಾಲೊಜೆನ್ಗಳೊಂದಿಗೆ (ಕ್ಲೋರಿನ್ ಮತ್ತು ಬ್ರೋಮಿನ್) ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳ ಪರ್ಯಾಯದ ವಿವಿಧ ಹಂತಗಳೊಂದಿಗೆ ಹ್ಯಾಲೊಜೆನ್ ಉತ್ಪನ್ನಗಳ ಮಿಶ್ರಣವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ - ಮೊನೊ-, ಡಿಟ್ರಿ-, ಇತ್ಯಾದಿ. ಹ್ಯಾಲೊಜೆನ್-ಬದಲಿ ಆಲ್ಕೇನ್ಗಳು.
ಮೀಥೇನ್ ಅನ್ನು ಉದಾಹರಣೆಯಾಗಿ ಬಳಸಿ, ಇದು ಈ ರೀತಿ ಕಾಣುತ್ತದೆ:
ಪ್ರತಿಕ್ರಿಯೆ ಮಿಶ್ರಣದಲ್ಲಿ ಹ್ಯಾಲೊಜೆನ್/ಮೀಥೇನ್ ಅನುಪಾತವನ್ನು ಬದಲಾಯಿಸುವ ಮೂಲಕ, ಉತ್ಪನ್ನಗಳ ಸಂಯೋಜನೆಯಲ್ಲಿ ಮೀಥೇನ್ನ ನಿರ್ದಿಷ್ಟ ಹ್ಯಾಲೊಜೆನ್ ಉತ್ಪನ್ನವು ಮೇಲುಗೈ ಸಾಧಿಸುತ್ತದೆ ಎಂದು ಖಚಿತಪಡಿಸಿಕೊಳ್ಳಲು ಸಾಧ್ಯವಿದೆ.
ಪ್ರತಿಕ್ರಿಯೆ ಯಾಂತ್ರಿಕತೆ
ಮೀಥೇನ್ ಮತ್ತು ಕ್ಲೋರಿನ್ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಉದಾಹರಣೆಯನ್ನು ಬಳಸಿಕೊಂಡು ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಪರ್ಯಾಯ ಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನವನ್ನು ನಾವು ವಿಶ್ಲೇಷಿಸೋಣ. ಇದು ಮೂರು ಹಂತಗಳನ್ನು ಒಳಗೊಂಡಿದೆ:
- ಪ್ರಾರಂಭ (ಅಥವಾ ಚೈನ್ ನ್ಯೂಕ್ಲಿಯೇಶನ್) ಬಾಹ್ಯ ಶಕ್ತಿಯ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳ ರಚನೆಯ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ - UV ಬೆಳಕು ಅಥವಾ ತಾಪನದೊಂದಿಗೆ ವಿಕಿರಣ. ಈ ಹಂತದಲ್ಲಿ, ಕ್ಲೋರಿನ್ ಅಣುವು ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳ ರಚನೆಯೊಂದಿಗೆ Cl-Cl ಬಂಧದ ಹೋಮೋಲಿಟಿಕ್ ಸೀಳನ್ನು ಒಳಗೊಳ್ಳುತ್ತದೆ:
ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳು, ಮೇಲಿನ ಚಿತ್ರದಿಂದ ನೋಡಬಹುದಾದಂತೆ, ಒಂದು ಅಥವಾ ಹೆಚ್ಚು ಜೋಡಿಯಾಗದ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಪರಮಾಣುಗಳು ಅಥವಾ ಪರಮಾಣುಗಳ ಗುಂಪುಗಳು (Cl, H, CH 3, CH 2, ಇತ್ಯಾದಿ);
2. ಚೈನ್ ಅಭಿವೃದ್ಧಿ
ಈ ಹಂತವು ನಿಷ್ಕ್ರಿಯ ಅಣುಗಳೊಂದಿಗೆ ಸಕ್ರಿಯ ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಹೊಸ ರಾಡಿಕಲ್ಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ನಿರ್ದಿಷ್ಟವಾಗಿ ಹೇಳುವುದಾದರೆ, ಕ್ಲೋರಿನ್ ರಾಡಿಕಲ್ಗಳು ಆಲ್ಕೇನ್ ಅಣುಗಳ ಮೇಲೆ ಕಾರ್ಯನಿರ್ವಹಿಸಿದಾಗ, ಆಲ್ಕೈಲ್ ರಾಡಿಕಲ್ ಮತ್ತು ಹೈಡ್ರೋಜನ್ ಕ್ಲೋರೈಡ್ ರಚನೆಯಾಗುತ್ತದೆ. ಪ್ರತಿಯಾಗಿ, ಆಲ್ಕೈಲ್ ರಾಡಿಕಲ್, ಕ್ಲೋರಿನ್ ಅಣುಗಳೊಂದಿಗೆ ಡಿಕ್ಕಿಹೊಡೆದು, ಕ್ಲೋರಿನ್ ಉತ್ಪನ್ನವನ್ನು ಮತ್ತು ಹೊಸ ಕ್ಲೋರಿನ್ ರಾಡಿಕಲ್ ಅನ್ನು ರೂಪಿಸುತ್ತದೆ:
3) ಸರ್ಕ್ಯೂಟ್ನ ಬ್ರೇಕ್ (ಸಾವು):
ನಿಷ್ಕ್ರಿಯ ಅಣುಗಳಾಗಿ ಪರಸ್ಪರ ಎರಡು ರಾಡಿಕಲ್ಗಳ ಮರುಸಂಯೋಜನೆಯ ಪರಿಣಾಮವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ:
2. ಆಕ್ಸಿಡೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಸಾಂದ್ರೀಕೃತ ಸಲ್ಫ್ಯೂರಿಕ್ ಮತ್ತು ನೈಟ್ರಿಕ್ ಆಮ್ಲಗಳು, ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ ಮತ್ತು ಡೈಕ್ರೋಮೇಟ್ (KMnO 4, K 2 Cr 2 O 7) ನಂತಹ ಬಲವಾದ ಆಕ್ಸಿಡೈಸಿಂಗ್ ಏಜೆಂಟ್ಗಳ ಕಡೆಗೆ ಆಲ್ಕೇನ್ಗಳು ಜಡವಾಗಿರುತ್ತವೆ.
ಆಮ್ಲಜನಕದಲ್ಲಿ ದಹನ
ಎ) ಹೆಚ್ಚುವರಿ ಆಮ್ಲಜನಕದೊಂದಿಗೆ ಸಂಪೂರ್ಣ ದಹನ. ಇಂಗಾಲದ ಡೈಆಕ್ಸೈಡ್ ಮತ್ತು ನೀರಿನ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
CH 4 + 2O 2 = CO 2 + 2H 2 O
ಬಿ) ಆಮ್ಲಜನಕದ ಕೊರತೆಯಿಂದಾಗಿ ಅಪೂರ್ಣ ದಹನ:
2CH 4 + 3O 2 = 2CO + 4H 2 O
CH 4 + O 2 = C + 2H 2 O
ಆಮ್ಲಜನಕದೊಂದಿಗೆ ವೇಗವರ್ಧಕ ಆಕ್ಸಿಡೀಕರಣ
ವೇಗವರ್ಧಕಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಆಮ್ಲಜನಕದೊಂದಿಗೆ (~ 200 o C) ಆಲ್ಕೇನ್ಗಳನ್ನು ಬಿಸಿ ಮಾಡುವ ಪರಿಣಾಮವಾಗಿ, ಅವುಗಳಿಂದ ವಿವಿಧ ರೀತಿಯ ಸಾವಯವ ಉತ್ಪನ್ನಗಳನ್ನು ಪಡೆಯಬಹುದು: ಆಲ್ಡಿಹೈಡ್ಗಳು, ಕೀಟೋನ್ಗಳು, ಆಲ್ಕೋಹಾಲ್ಗಳು, ಕಾರ್ಬಾಕ್ಸಿಲಿಕ್ ಆಮ್ಲಗಳು.
ಉದಾಹರಣೆಗೆ, ವೇಗವರ್ಧಕದ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿ ಮೀಥೇನ್ ಅನ್ನು ಮೀಥೈಲ್ ಆಲ್ಕೋಹಾಲ್, ಫಾರ್ಮಾಲ್ಡಿಹೈಡ್ ಅಥವಾ ಫಾರ್ಮಿಕ್ ಆಮ್ಲವಾಗಿ ಆಕ್ಸಿಡೀಕರಿಸಬಹುದು:
3. ಅಲ್ಕೇನ್ಗಳ ಉಷ್ಣ ರೂಪಾಂತರಗಳು
ಕ್ರ್ಯಾಕಿಂಗ್
ಕ್ರ್ಯಾಕಿಂಗ್ (ಇಂಗ್ಲಿಷ್ ನಿಂದ ಕ್ರ್ಯಾಕ್ - ಹರಿದು) ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲಿ ಸಂಭವಿಸುವ ರಾಸಾಯನಿಕ ಪ್ರಕ್ರಿಯೆಯಾಗಿದೆ, ಇದರ ಪರಿಣಾಮವಾಗಿ ಅಲ್ಕೇನ್ ಅಣುಗಳ ಇಂಗಾಲದ ಅಸ್ಥಿಪಂಜರವು ಮೂಲ ಆಲ್ಕೇನ್ಗಳಿಗೆ ಹೋಲಿಸಿದರೆ ಕಡಿಮೆ ಆಣ್ವಿಕ ತೂಕದೊಂದಿಗೆ ಆಲ್ಕೇನ್ ಮತ್ತು ಆಲ್ಕೇನ್ಗಳ ಅಣುಗಳನ್ನು ರೂಪಿಸಲು ಒಡೆಯುತ್ತದೆ. ಉದಾಹರಣೆಗೆ:
CH 3 -CH 2 -CH 2 -CH 2 -CH 2 -CH 2 -CH 3 → CH 3 -CH 2 -CH 2 -CH 3 + CH 3 -CH=CH 2
ಬಿರುಕುಗಳು ಉಷ್ಣ ಅಥವಾ ವೇಗವರ್ಧಕವಾಗಿರಬಹುದು. ವೇಗವರ್ಧಕ ಕ್ರ್ಯಾಕಿಂಗ್ ಅನ್ನು ಕೈಗೊಳ್ಳಲು, ವೇಗವರ್ಧಕಗಳ ಬಳಕೆಗೆ ಧನ್ಯವಾದಗಳು, ಉಷ್ಣ ಕ್ರ್ಯಾಕಿಂಗ್ಗೆ ಹೋಲಿಸಿದರೆ ಗಮನಾರ್ಹವಾಗಿ ಕಡಿಮೆ ತಾಪಮಾನವನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
ನಿರ್ಜಲೀಕರಣ
C-H ಬಂಧಗಳ ಸೀಳಿನ ಪರಿಣಾಮವಾಗಿ ಹೈಡ್ರೋಜನ್ ನಿರ್ಮೂಲನೆ ಸಂಭವಿಸುತ್ತದೆ; ಎತ್ತರದ ತಾಪಮಾನದಲ್ಲಿ ವೇಗವರ್ಧಕಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ನಡೆಸಲಾಗುತ್ತದೆ. ಮೀಥೇನ್ ನಿರ್ಜಲೀಕರಣಗೊಂಡಾಗ, ಅಸಿಟಿಲೀನ್ ರೂಪುಗೊಳ್ಳುತ್ತದೆ:
2CH 4 → C 2 H 2 + 3H 2
ಮೀಥೇನ್ ಅನ್ನು 1200 °C ಗೆ ಬಿಸಿಮಾಡುವುದು ಅದರ ವಿಭಜನೆಗೆ ಸರಳ ಪದಾರ್ಥಗಳಾಗಿ ಕಾರಣವಾಗುತ್ತದೆ:
CH 4 → C + 2H 2
ಉಳಿದ ಆಲ್ಕೇನ್ಗಳನ್ನು ನಿರ್ಜಲೀಕರಣಗೊಳಿಸಿದಾಗ, ಆಲ್ಕೀನ್ಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ:
C 2 H 6 → C 2 H 4 + H 2
ನಿರ್ಜಲೀಕರಣಗೊಳಿಸುವಾಗ ಎನ್-ಬ್ಯುಟೇನ್, ಬ್ಯೂಟಿನ್ -1 ಮತ್ತು ಬ್ಯುಟೆನ್ -2 ರೂಪುಗೊಳ್ಳುತ್ತವೆ (ಎರಡನೆಯದು ರೂಪದಲ್ಲಿ ಸಿಸ್-ಮತ್ತು ಟ್ರಾನ್ಸ್-ಐಸೋಮರ್ಗಳು):
ಡಿಹೈಡ್ರೊಸೈಕ್ಲೈಸೇಶನ್
ಐಸೋಮರೈಸೇಶನ್
ಸೈಕ್ಲೋಆಲ್ಕೇನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಅವುಗಳ ಉಂಗುರಗಳಲ್ಲಿ ನಾಲ್ಕಕ್ಕಿಂತ ಹೆಚ್ಚು ಇಂಗಾಲದ ಪರಮಾಣುಗಳನ್ನು ಹೊಂದಿರುವ ಸೈಕ್ಲೋಆಲ್ಕೇನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಆಲ್ಕೇನ್ಗಳ ಗುಣಲಕ್ಷಣಗಳಿಗೆ ಹೋಲುತ್ತವೆ. ವಿಚಿತ್ರವೆಂದರೆ, ಸೈಕ್ಲೋಪ್ರೊಪೇನ್ ಮತ್ತು ಸೈಕ್ಲೋಬ್ಯುಟೇನ್ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಂದ ನಿರೂಪಿಸಲ್ಪಟ್ಟಿದೆ. ಇದು ಚಕ್ರದೊಳಗಿನ ಹೆಚ್ಚಿನ ಒತ್ತಡದಿಂದಾಗಿ, ಈ ಚಕ್ರಗಳು ಮುರಿಯಲು ಒಲವು ತೋರುತ್ತವೆ ಎಂಬ ಅಂಶಕ್ಕೆ ಕಾರಣವಾಗುತ್ತದೆ. ಆದ್ದರಿಂದ ಸೈಕ್ಲೋಪ್ರೊಪೇನ್ ಮತ್ತು ಸೈಕ್ಲೋಬುಟೇನ್ ಸುಲಭವಾಗಿ ಬ್ರೋಮಿನ್, ಹೈಡ್ರೋಜನ್ ಅಥವಾ ಹೈಡ್ರೋಜನ್ ಕ್ಲೋರೈಡ್ ಅನ್ನು ಸೇರಿಸುತ್ತವೆ:
ಆಲ್ಕೀನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
1. ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಆಲ್ಕೀನ್ ಅಣುಗಳಲ್ಲಿನ ಡಬಲ್ ಬಂಧವು ಒಂದು ಬಲವಾದ ಸಿಗ್ಮಾ ಮತ್ತು ಒಂದು ದುರ್ಬಲ ಪೈ ಬಂಧವನ್ನು ಒಳಗೊಂಡಿರುವುದರಿಂದ, ಅವುಗಳು ಸುಲಭವಾಗಿ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುವ ಸಾಕಷ್ಟು ಸಕ್ರಿಯ ಸಂಯುಕ್ತಗಳಾಗಿವೆ. ಆಲ್ಕೀನ್ಗಳು ಸಾಮಾನ್ಯವಾಗಿ ಸೌಮ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿಯೂ ಸಹ ಇಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುತ್ತವೆ - ಶೀತದಲ್ಲಿ, ಜಲೀಯ ದ್ರಾವಣಗಳು ಮತ್ತು ಸಾವಯವ ದ್ರಾವಕಗಳಲ್ಲಿ.
ಆಲ್ಕೀನ್ಗಳ ಹೈಡ್ರೋಜನೀಕರಣ
ವೇಗವರ್ಧಕಗಳ (ಪ್ಲಾಟಿನಂ, ಪಲ್ಲಾಡಿಯಮ್, ನಿಕಲ್) ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಆಲ್ಕೀನ್ಗಳು ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಸೇರಿಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿವೆ:
CH 3 -CH = CH 2 + H 2 → CH 3 -CH 2 -CH 3
ಆಲ್ಕೀನ್ಗಳ ಹೈಡ್ರೋಜನೀಕರಣವು ಸಾಮಾನ್ಯ ಒತ್ತಡ ಮತ್ತು ಸ್ವಲ್ಪ ತಾಪದಲ್ಲಿಯೂ ಸುಲಭವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ. ಒಂದು ಕುತೂಹಲಕಾರಿ ಸಂಗತಿಯೆಂದರೆ, ಆಲ್ಕೇನ್ಗಳಿಗೆ ಆಲ್ಕೇನ್ಗಳ ನಿರ್ಜಲೀಕರಣಕ್ಕೆ ಅದೇ ವೇಗವರ್ಧಕಗಳನ್ನು ಬಳಸಬಹುದು, ಹೆಚ್ಚಿನ ತಾಪಮಾನ ಮತ್ತು ಕಡಿಮೆ ಒತ್ತಡದಲ್ಲಿ ಡಿಹೈಡ್ರೋಜನೀಕರಣ ಪ್ರಕ್ರಿಯೆ ಮಾತ್ರ ಸಂಭವಿಸುತ್ತದೆ.
ಹ್ಯಾಲೊಜೆನೇಶನ್
ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ ಮತ್ತು ಸಾವಯವ ದ್ರಾವಕಗಳಲ್ಲಿ ಬ್ರೋಮಿನ್ನೊಂದಿಗೆ ಆಲ್ಕೀನ್ಗಳು ಸುಲಭವಾಗಿ ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುತ್ತವೆ. ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಪರಿಣಾಮವಾಗಿ, ಆರಂಭದಲ್ಲಿ ಹಳದಿ ಬ್ರೋಮಿನ್ ದ್ರಾವಣಗಳು ತಮ್ಮ ಬಣ್ಣವನ್ನು ಕಳೆದುಕೊಳ್ಳುತ್ತವೆ, ಅಂದರೆ. ಬಣ್ಣಬಣ್ಣವಾಗುತ್ತದೆ.
CH 2 =CH 2 + Br 2 → CH 2 Br-CH 2 Br
ಹೈಡ್ರೋಹಲೋಜೆನೇಶನ್
ನೋಡಲು ಸುಲಭವಾಗುವಂತೆ, ಅಸಮಪಾರ್ಶ್ವದ ಆಲ್ಕೀನ್ನ ಅಣುವಿಗೆ ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ನ ಸೇರ್ಪಡೆಯು ಸೈದ್ಧಾಂತಿಕವಾಗಿ ಎರಡು ಐಸೋಮರ್ಗಳ ಮಿಶ್ರಣಕ್ಕೆ ಕಾರಣವಾಗಬೇಕು. ಉದಾಹರಣೆಗೆ, ಪ್ರೋಪೀನ್ಗೆ ಹೈಡ್ರೋಜನ್ ಬ್ರೋಮೈಡ್ ಅನ್ನು ಸೇರಿಸಿದಾಗ, ಈ ಕೆಳಗಿನ ಉತ್ಪನ್ನಗಳನ್ನು ಪಡೆಯಬೇಕು:
ಆದಾಗ್ಯೂ, ನಿರ್ದಿಷ್ಟ ಪರಿಸ್ಥಿತಿಗಳ ಅನುಪಸ್ಥಿತಿಯಲ್ಲಿ (ಉದಾಹರಣೆಗೆ, ಪ್ರತಿಕ್ರಿಯೆ ಮಿಶ್ರಣದಲ್ಲಿ ಪೆರಾಕ್ಸೈಡ್ಗಳ ಉಪಸ್ಥಿತಿ), ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ ಅಣುವಿನ ಸೇರ್ಪಡೆಯು ಮಾರ್ಕೊವ್ನಿಕೋವ್ ಅವರ ನಿಯಮಕ್ಕೆ ಅನುಗುಣವಾಗಿ ಕಟ್ಟುನಿಟ್ಟಾಗಿ ಆಯ್ದವಾಗಿ ಸಂಭವಿಸುತ್ತದೆ:
ಆಲ್ಕೀನ್ಗೆ ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ನ ಸೇರ್ಪಡೆಯು ಹೆಚ್ಚಿನ ಸಂಖ್ಯೆಯ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳೊಂದಿಗೆ (ಹೆಚ್ಚು ಹೈಡ್ರೋಜನೀಕರಿಸಿದ) ಕಾರ್ಬನ್ ಪರಮಾಣುವಿಗೆ ಹೈಡ್ರೋಜನ್ ಅನ್ನು ಸೇರಿಸುವ ರೀತಿಯಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ ಮತ್ತು ಕಡಿಮೆ ಸಂಖ್ಯೆಯ ಹೈಡ್ರೋಜನ್ ಹೊಂದಿರುವ ಕಾರ್ಬನ್ ಪರಮಾಣುವಿಗೆ ಹ್ಯಾಲೊಜೆನ್ ಅನ್ನು ಸೇರಿಸಲಾಗುತ್ತದೆ. ಪರಮಾಣುಗಳು (ಕಡಿಮೆ ಹೈಡ್ರೋಜನೀಕರಿಸಿದ).
ಜಲಸಂಚಯನ
ಈ ಪ್ರತಿಕ್ರಿಯೆಯು ಆಲ್ಕೋಹಾಲ್ಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ ಮತ್ತು ಮಾರ್ಕೊವ್ನಿಕೋವ್ನ ನಿಯಮಕ್ಕೆ ಅನುಗುಣವಾಗಿ ಮುಂದುವರಿಯುತ್ತದೆ:
ನೀವು ಸುಲಭವಾಗಿ ಊಹಿಸುವಂತೆ, ಮಾರ್ಕೊವ್ನಿಕೋವ್ನ ನಿಯಮದ ಪ್ರಕಾರ ಆಲ್ಕೀನ್ ಅಣುವಿಗೆ ನೀರಿನ ಸೇರ್ಪಡೆ ಸಂಭವಿಸುತ್ತದೆ ಎಂಬ ಅಂಶದಿಂದಾಗಿ, ಪ್ರಾಥಮಿಕ ಆಲ್ಕೋಹಾಲ್ ರಚನೆಯು ಎಥಿಲೀನ್ ಜಲಸಂಚಯನದ ಸಂದರ್ಭದಲ್ಲಿ ಮಾತ್ರ ಸಾಧ್ಯ:
CH 2 =CH 2 + H 2 O → CH 3 -CH 2 -OH
ಈ ಪ್ರತಿಕ್ರಿಯೆಯ ಮೂಲಕವೇ ದೊಡ್ಡ ಪ್ರಮಾಣದ ಉದ್ಯಮದಲ್ಲಿ ಈಥೈಲ್ ಆಲ್ಕೋಹಾಲ್ನ ಬೃಹತ್ ಪ್ರಮಾಣವನ್ನು ನಡೆಸಲಾಗುತ್ತದೆ.
ಪಾಲಿಮರೀಕರಣ
ಸಂಕಲನ ಕ್ರಿಯೆಯ ಒಂದು ನಿರ್ದಿಷ್ಟ ಪ್ರಕರಣವೆಂದರೆ ಪಾಲಿಮರೀಕರಣ ಕ್ರಿಯೆ, ಇದು ಹ್ಯಾಲೊಜೆನೇಶನ್, ಹೈಡ್ರೊಹಾಲೊಜೆನೇಶನ್ ಮತ್ತು ಜಲಸಂಚಯನಕ್ಕಿಂತ ಭಿನ್ನವಾಗಿ, ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಮುಂದುವರಿಯುತ್ತದೆ:
ಆಕ್ಸಿಡೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಎಲ್ಲಾ ಇತರ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳಂತೆ, ಆಲ್ಕೀನ್ಗಳು ಆಮ್ಲಜನಕದಲ್ಲಿ ಸುಲಭವಾಗಿ ಉರಿಯುತ್ತವೆ ಮತ್ತು ಇಂಗಾಲದ ಡೈಆಕ್ಸೈಡ್ ಮತ್ತು ನೀರನ್ನು ರೂಪಿಸುತ್ತವೆ. ಹೆಚ್ಚುವರಿ ಆಮ್ಲಜನಕದಲ್ಲಿ ಆಲ್ಕೀನ್ಗಳ ದಹನದ ಸಮೀಕರಣವು ರೂಪವನ್ನು ಹೊಂದಿದೆ:
C n H 2n + (3/2) nO 2 → nCO 2 + nH 2 O
ಆಲ್ಕೇನ್ಗಳಿಗಿಂತ ಭಿನ್ನವಾಗಿ, ಆಲ್ಕೀನ್ಗಳು ಸುಲಭವಾಗಿ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತವೆ. ಆಲ್ಕೀನ್ಗಳು KMnO 4 ರ ಜಲೀಯ ದ್ರಾವಣಕ್ಕೆ ಒಡ್ಡಿಕೊಂಡಾಗ, ಬಣ್ಣಬಣ್ಣವು ಸಂಭವಿಸುತ್ತದೆ, ಇದು ಸಾವಯವ ಪದಾರ್ಥಗಳ ಅಣುಗಳಲ್ಲಿ ಡಬಲ್ ಮತ್ತು ಟ್ರಿಪಲ್ CC ಬಂಧಗಳಿಗೆ ಗುಣಾತ್ಮಕ ಪ್ರತಿಕ್ರಿಯೆಯಾಗಿದೆ.
ತಟಸ್ಥ ಅಥವಾ ಸ್ವಲ್ಪ ಕ್ಷಾರೀಯ ದ್ರಾವಣದಲ್ಲಿ ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನೊಂದಿಗೆ ಆಲ್ಕೆನ್ಗಳ ಆಕ್ಸಿಡೀಕರಣವು ಡಯೋಲ್ಗಳ (ಡೈಹೈಡ್ರಿಕ್ ಆಲ್ಕೋಹಾಲ್ಗಳು) ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
C 2 H 4 + 2KMnO 4 + 2H 2 O → CH 2 OH–CH 2 OH + 2MnO 2 + 2KOH (ಕೂಲಿಂಗ್)
ಆಮ್ಲೀಯ ವಾತಾವರಣದಲ್ಲಿ, ಡಬಲ್ ಬಾಂಡ್ ಸಂಪೂರ್ಣವಾಗಿ ಮುರಿದುಹೋಗುತ್ತದೆ ಮತ್ತು ಡಬಲ್ ಬಂಧವನ್ನು ರೂಪಿಸಿದ ಕಾರ್ಬನ್ ಪರಮಾಣುಗಳನ್ನು ಕಾರ್ಬಾಕ್ಸಿಲ್ ಗುಂಪುಗಳಾಗಿ ಪರಿವರ್ತಿಸಲಾಗುತ್ತದೆ:
5CH 3 CH=CHCH 2 CH 3 + 8KMnO 4 + 12H 2 SO 4 → 5CH 3 COOH + 5C 2 H 5 COOH + 8MnSO 4 + 4K 2 SO 4 + 17H 2 O (ತಾಪನ)
ಡಬಲ್ C=C ಬಂಧವು ಆಲ್ಕೀನ್ ಅಣುವಿನ ಕೊನೆಯಲ್ಲಿ ನೆಲೆಗೊಂಡಿದ್ದರೆ, ನಂತರ ಕಾರ್ಬನ್ ಡೈಆಕ್ಸೈಡ್ ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಹೊರಗಿನ ಕಾರ್ಬನ್ ಪರಮಾಣುವಿನ ಆಕ್ಸಿಡೀಕರಣದ ಉತ್ಪನ್ನವಾಗಿ ರೂಪುಗೊಳ್ಳುತ್ತದೆ. ಮಧ್ಯಂತರ ಆಕ್ಸಿಡೀಕರಣ ಉತ್ಪನ್ನವಾದ ಫಾರ್ಮಿಕ್ ಆಮ್ಲವು ಹೆಚ್ಚಿನ ಆಕ್ಸಿಡೈಸಿಂಗ್ ಏಜೆಂಟ್ನಲ್ಲಿ ಸುಲಭವಾಗಿ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುತ್ತದೆ ಎಂಬುದು ಇದಕ್ಕೆ ಕಾರಣ:
5CH 3 CH=CH 2 + 10KMnO 4 + 15H 2 SO 4 → 5CH 3 COOH + 5CO 2 + 10MnSO 4 + 5K 2 SO 4 + 20H 2 O (ತಾಪನ)
ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿರುವ C ಪರಮಾಣು ಎರಡು ಹೈಡ್ರೋಕಾರ್ಬನ್ ಪರ್ಯಾಯಗಳನ್ನು ಹೊಂದಿರುವ ಆಲ್ಕೀನ್ಗಳ ಆಕ್ಸಿಡೀಕರಣವು ಕೀಟೋನ್ ಅನ್ನು ಉತ್ಪಾದಿಸುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, 2-ಮೀಥೈಲ್ಬುಟೀನ್-2 ರ ಆಕ್ಸಿಡೀಕರಣವು ಅಸಿಟೋನ್ ಮತ್ತು ಅಸಿಟಿಕ್ ಆಮ್ಲವನ್ನು ಉತ್ಪಾದಿಸುತ್ತದೆ.
ಕಾರ್ಬನ್ ಅಸ್ಥಿಪಂಜರವು ಡಬಲ್ ಬಾಂಡ್ನಲ್ಲಿ ಮುರಿದುಹೋಗುವ ಆಲ್ಕೀನ್ಗಳ ಆಕ್ಸಿಡೀಕರಣವನ್ನು ಅವುಗಳ ರಚನೆಯನ್ನು ನಿರ್ಧರಿಸಲು ಬಳಸಲಾಗುತ್ತದೆ.
ಅಲ್ಕಾಡಿಯನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಉದಾಹರಣೆಗೆ, ಹ್ಯಾಲೊಜೆನ್ಗಳ ಸೇರ್ಪಡೆ:
ಬ್ರೋಮಿನ್ ನೀರು ಬಣ್ಣಕ್ಕೆ ತಿರುಗುತ್ತದೆ.
ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ, ಹ್ಯಾಲೊಜೆನ್ ಪರಮಾಣುಗಳ ಸೇರ್ಪಡೆಯು 1,3-ಬ್ಯುಟಾಡೀನ್ ಅಣುವಿನ ತುದಿಗಳಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ, ಆದರೆ π-ಬಂಧಗಳು ಮುರಿದುಹೋಗಿವೆ, ಬ್ರೋಮಿನ್ ಪರಮಾಣುಗಳನ್ನು ಹೊರಗಿನ ಇಂಗಾಲದ ಪರಮಾಣುಗಳಿಗೆ ಸೇರಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಮುಕ್ತ ವೇಲೆನ್ಸ್ಗಳು ಹೊಸ π-ಬಂಧವನ್ನು ರೂಪಿಸುತ್ತವೆ. . ಹೀಗಾಗಿ, ಡಬಲ್ ಬಾಂಡ್ನ "ಚಲನೆ" ಸಂಭವಿಸುತ್ತದೆ. ಬ್ರೋಮಿನ್ ಅಧಿಕವಾಗಿದ್ದರೆ, ರೂಪುಗೊಂಡ ಡಬಲ್ ಬಂಧದ ಸ್ಥಳದಲ್ಲಿ ಮತ್ತೊಂದು ಅಣುವನ್ನು ಸೇರಿಸಬಹುದು.
ಪಾಲಿಮರೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಆಲ್ಕಿನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಆಲ್ಕಿನ್ಗಳು ಅಪರ್ಯಾಪ್ತ (ಅಪರ್ಯಾಪ್ತ) ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳು ಮತ್ತು ಆದ್ದರಿಂದ ಸಂಕಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿರುತ್ತವೆ. ಆಲ್ಕೈನ್ಗಳಿಗೆ ಸಂಕಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳಲ್ಲಿ, ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಸೇರ್ಪಡೆ ಅತ್ಯಂತ ಸಾಮಾನ್ಯವಾಗಿದೆ.
ಹ್ಯಾಲೊಜೆನೇಶನ್
ಆಲ್ಕಿನ್ ಅಣುಗಳ ಟ್ರಿಪಲ್ ಬಂಧವು ಒಂದು ಬಲವಾದ ಸಿಗ್ಮಾ ಬಂಧ ಮತ್ತು ಎರಡು ದುರ್ಬಲ ಪೈ ಬಂಧಗಳನ್ನು ಒಳಗೊಂಡಿರುವುದರಿಂದ, ಅವು ಒಂದು ಅಥವಾ ಎರಡು ಹ್ಯಾಲೊಜೆನ್ ಅಣುಗಳನ್ನು ಜೋಡಿಸಲು ಸಮರ್ಥವಾಗಿವೆ. ಒಂದು ಆಲ್ಕಿನ್ ಅಣುವಿನಿಂದ ಎರಡು ಹ್ಯಾಲೊಜೆನ್ ಅಣುಗಳ ಸೇರ್ಪಡೆಯು ಎರಡು ಹಂತಗಳಲ್ಲಿ ಅನುಕ್ರಮವಾಗಿ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಮುಂದುವರಿಯುತ್ತದೆ:
ಹೈಡ್ರೋಹಲೋಜೆನೇಶನ್
ಹೈಡ್ರೋಜನ್ ಹಾಲೈಡ್ ಅಣುಗಳ ಸೇರ್ಪಡೆಯು ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಮತ್ತು ಎರಡು ಹಂತಗಳಲ್ಲಿ ಸಂಭವಿಸುತ್ತದೆ. ಎರಡೂ ಹಂತಗಳಲ್ಲಿ, ಪ್ರವೇಶವು ಮಾರ್ಕೊವ್ನಿಕೋವ್ ಅವರ ನಿಯಮಕ್ಕೆ ಅನುಗುಣವಾಗಿ ಮುಂದುವರಿಯುತ್ತದೆ:
ಜಲಸಂಚಯನ
ಆಮ್ಲೀಯ ಮಾಧ್ಯಮದಲ್ಲಿ ರೂಟಿ ಲವಣಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಆಲ್ಕಿನ್ಗಳಿಗೆ ನೀರಿನ ಸೇರ್ಪಡೆ ಸಂಭವಿಸುತ್ತದೆ ಮತ್ತು ಇದನ್ನು ಕುಚೆರೋವ್ ಪ್ರತಿಕ್ರಿಯೆ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಜಲಸಂಚಯನದ ಪರಿಣಾಮವಾಗಿ, ಅಸಿಟಿಲೀನ್ಗೆ ನೀರನ್ನು ಸೇರಿಸುವುದರಿಂದ ಅಸಿಟಾಲ್ಡಿಹೈಡ್ (ಅಸಿಟಿಕ್ ಆಲ್ಡಿಹೈಡ್) ಉತ್ಪತ್ತಿಯಾಗುತ್ತದೆ:
ಅಸಿಟಿಲೀನ್ ಹೋಮೊಲಾಗ್ಗಳಿಗೆ, ನೀರಿನ ಸೇರ್ಪಡೆಯು ಕೀಟೋನ್ಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
ಆಲ್ಕೈನ್ಗಳ ಹೈಡ್ರೋಜನೀಕರಣ
ಅಲ್ಕಿನ್ಗಳು ಹೈಡ್ರೋಜನ್ನೊಂದಿಗೆ ಎರಡು ಹಂತಗಳಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತವೆ. ಪ್ಲಾಟಿನಮ್, ಪಲ್ಲಾಡಿಯಮ್ ಮತ್ತು ನಿಕಲ್ನಂತಹ ಲೋಹಗಳನ್ನು ವೇಗವರ್ಧಕಗಳಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ:
ಆಲ್ಕೈನ್ಗಳ ಟ್ರೈಮರೀಕರಣ
ಅಸಿಟಿಲೀನ್ ಅನ್ನು ಹೆಚ್ಚಿನ ತಾಪಮಾನದಲ್ಲಿ ಸಕ್ರಿಯ ಇಂಗಾಲದ ಮೇಲೆ ಹಾದುಹೋದಾಗ, ಅದರಿಂದ ವಿವಿಧ ಉತ್ಪನ್ನಗಳ ಮಿಶ್ರಣವು ರೂಪುಗೊಳ್ಳುತ್ತದೆ, ಅದರಲ್ಲಿ ಮುಖ್ಯವಾದ ಬೆಂಜೀನ್, ಅಸಿಟಿಲೀನ್ ಟ್ರಿಮರೈಸೇಶನ್ ಉತ್ಪನ್ನವಾಗಿದೆ:
ಆಲ್ಕೈನ್ಗಳ ಡೈಮರೈಸೇಶನ್
ಅಸಿಟಿಲೀನ್ ಸಹ ಡೈಮರೈಸೇಶನ್ ಕ್ರಿಯೆಗೆ ಒಳಗಾಗುತ್ತದೆ. ವೇಗವರ್ಧಕವಾಗಿ ತಾಮ್ರದ ಲವಣಗಳ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಪ್ರಕ್ರಿಯೆಯು ನಡೆಯುತ್ತದೆ:
ಆಲ್ಕಿನ್ ಆಕ್ಸಿಡೀಕರಣ
ಆಲ್ಕಿನ್ಗಳು ಆಮ್ಲಜನಕದಲ್ಲಿ ಉರಿಯುತ್ತವೆ:
C nH 2n-2 + (3n-1)/2 O 2 → nCO 2 + (n-1)H 2 O
ಬೇಸ್ಗಳೊಂದಿಗೆ ಅಲ್ಕಿನ್ಗಳ ಪ್ರತಿಕ್ರಿಯೆ
ಅಣುವಿನ ಅಂತ್ಯದಲ್ಲಿ ಟ್ರಿಪಲ್ C≡C ಹೊಂದಿರುವ ಆಲ್ಕಿನ್ಗಳು, ಇತರ ಆಲ್ಕಿನ್ಗಳಿಗಿಂತ ಭಿನ್ನವಾಗಿ, ಟ್ರಿಪಲ್ ಬಂಧದಲ್ಲಿರುವ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣು ಲೋಹದಿಂದ ಬದಲಾಯಿಸಲ್ಪಟ್ಟ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಪ್ರವೇಶಿಸಲು ಸಾಧ್ಯವಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಅಸಿಟಿಲೀನ್ ದ್ರವ ಅಮೋನಿಯದಲ್ಲಿ ಸೋಡಿಯಂ ಅಮೈಡ್ನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ:
HC≡CH + 2NaNH 2 → NaC≡CNa + 2NH 3 ,
ಮತ್ತು ಸಿಲ್ವರ್ ಆಕ್ಸೈಡ್ನ ಅಮೋನಿಯ ದ್ರಾವಣದೊಂದಿಗೆ, ಅಸಿಟಿಲೀನೈಡ್ಗಳು ಎಂಬ ಕರಗದ ಉಪ್ಪಿನಂತಹ ಪದಾರ್ಥಗಳನ್ನು ರೂಪಿಸುತ್ತದೆ:
ಈ ಪ್ರತಿಕ್ರಿಯೆಗೆ ಧನ್ಯವಾದಗಳು, ಟರ್ಮಿನಲ್ ಟ್ರಿಪಲ್ ಬಾಂಡ್ನೊಂದಿಗೆ ಅಲ್ಕಿನ್ಗಳನ್ನು ಗುರುತಿಸಲು ಸಾಧ್ಯವಿದೆ, ಹಾಗೆಯೇ ಇತರ ಆಲ್ಕೈನ್ಗಳೊಂದಿಗೆ ಮಿಶ್ರಣದಿಂದ ಅಂತಹ ಅಲ್ಕಿನ್ ಅನ್ನು ಪ್ರತ್ಯೇಕಿಸಲು.
ಎಲ್ಲಾ ಬೆಳ್ಳಿ ಮತ್ತು ತಾಮ್ರದ ಅಸಿಟಿಲೆನೈಡ್ಗಳು ಸ್ಫೋಟಕ ಪದಾರ್ಥಗಳಾಗಿವೆ ಎಂದು ಗಮನಿಸಬೇಕು.
ಅಸಿಟಿಲೆನೈಡ್ಗಳು ಹ್ಯಾಲೊಜೆನ್ ಉತ್ಪನ್ನಗಳೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿವೆ, ಇದನ್ನು ಟ್ರಿಪಲ್ ಬಂಧದೊಂದಿಗೆ ಹೆಚ್ಚು ಸಂಕೀರ್ಣ ಸಾವಯವ ಸಂಯುಕ್ತಗಳ ಸಂಶ್ಲೇಷಣೆಯಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ:
CH 3 -C≡CH + NaNH 2 → CH 3 -C≡CNa + NH 3
CH 3 -C≡CNa + CH 3 Br → CH 3 -C≡C-CH 3 + NaBr
ಆರೊಮ್ಯಾಟಿಕ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಬಂಧದ ಆರೊಮ್ಯಾಟಿಕ್ ಸ್ವಭಾವವು ಬೆಂಜೀನ್ಗಳು ಮತ್ತು ಇತರ ಆರೊಮ್ಯಾಟಿಕ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಪ್ರಭಾವಿಸುತ್ತದೆ.
ಏಕೀಕೃತ 6pi ಎಲೆಕ್ಟ್ರಾನ್ ವ್ಯವಸ್ಥೆಯು ಸಾಮಾನ್ಯ ಪೈ ಬಂಧಗಳಿಗಿಂತ ಹೆಚ್ಚು ಸ್ಥಿರವಾಗಿರುತ್ತದೆ. ಆದ್ದರಿಂದ, ಆರೊಮ್ಯಾಟಿಕ್ ಹೈಡ್ರೋಕಾರ್ಬನ್ಗಳಿಗೆ ಸಂಕಲನ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗಿಂತ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಹೆಚ್ಚು ವಿಶಿಷ್ಟವಾಗಿದೆ. ಅರೆನೆಸ್ ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಯಾಂತ್ರಿಕತೆಯ ಮೂಲಕ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳಿಗೆ ಒಳಗಾಗುತ್ತದೆ.
ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಹ್ಯಾಲೊಜೆನೇಶನ್
ನೈಟ್ರೇಶನ್
ನೈಟ್ರೇಶನ್ ಕ್ರಿಯೆಯು ಶುದ್ಧ ನೈಟ್ರಿಕ್ ಆಮ್ಲದ ಪ್ರಭಾವದ ಅಡಿಯಲ್ಲಿ ಉತ್ತಮವಾಗಿ ಮುಂದುವರಿಯುತ್ತದೆ, ಆದರೆ ನೈಟ್ರೇಟಿಂಗ್ ಮಿಶ್ರಣ ಎಂದು ಕರೆಯಲ್ಪಡುವ ಕೇಂದ್ರೀಕೃತ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲದೊಂದಿಗೆ ಅದರ ಮಿಶ್ರಣವಾಗಿದೆ:
ಆಲ್ಕೈಲೇಶನ್
ಆರೊಮ್ಯಾಟಿಕ್ ರಿಂಗ್ನಲ್ಲಿರುವ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳಲ್ಲಿ ಒಂದನ್ನು ಹೈಡ್ರೋಕಾರ್ಬನ್ ರಾಡಿಕಲ್ನಿಂದ ಬದಲಾಯಿಸುವ ಪ್ರತಿಕ್ರಿಯೆ:
ಹ್ಯಾಲೊಜೆನೇಟೆಡ್ ಆಲ್ಕೇನ್ಗಳ ಬದಲಿಗೆ ಆಲ್ಕೆನ್ಗಳನ್ನು ಸಹ ಬಳಸಬಹುದು. ಅಲ್ಯೂಮಿನಿಯಂ ಹಾಲೈಡ್ಗಳು, ಫೆರಿಕ್ ಹಾಲೈಡ್ಗಳು ಅಥವಾ ಅಜೈವಿಕ ಆಮ್ಲಗಳನ್ನು ವೇಗವರ್ಧಕಗಳಾಗಿ ಬಳಸಬಹುದು.<
ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಹೈಡ್ರೋಜನೀಕರಣ
ಕ್ಲೋರಿನ್ ಸೇರ್ಪಡೆ
ನೇರಳಾತೀತ ಬೆಳಕಿನೊಂದಿಗೆ ತೀವ್ರವಾದ ವಿಕಿರಣದ ಮೇಲೆ ಆಮೂಲಾಗ್ರ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಆದಾಯ:
ಇದೇ ರೀತಿಯ ಪ್ರತಿಕ್ರಿಯೆಯು ಕ್ಲೋರಿನ್ನೊಂದಿಗೆ ಮಾತ್ರ ಸಂಭವಿಸಬಹುದು.
ಆಕ್ಸಿಡೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ದಹನ
2C 6 H 6 + 15O 2 = 12CO 2 + 6H 2 O + Q
ಅಪೂರ್ಣ ಆಕ್ಸಿಡೀಕರಣ
ಬೆಂಜೀನ್ ಉಂಗುರವು KMnO 4 ಮತ್ತು K 2 Cr 2 O 7 ನಂತಹ ಆಕ್ಸಿಡೈಸಿಂಗ್ ಏಜೆಂಟ್ಗಳಿಗೆ ನಿರೋಧಕವಾಗಿದೆ. ಯಾವುದೇ ಪ್ರತಿಕ್ರಿಯೆ ಇಲ್ಲ.
ಬೆಂಜೀನ್ ಉಂಗುರದ ಬದಲಿಗಳನ್ನು ಎರಡು ವಿಧಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ:
ಟೊಲ್ಯೂನ್ ಅನ್ನು ಉದಾಹರಣೆಯಾಗಿ ಬಳಸಿಕೊಂಡು ಬೆಂಜೀನ್ ಹೋಮೋಲೋಗ್ಸ್ನ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ನಾವು ಪರಿಗಣಿಸೋಣ.
ಟೊಲ್ಯೂನ್ನ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು
ಹ್ಯಾಲೊಜೆನೇಶನ್
ಟೊಲ್ಯೂನ್ ಅಣುವನ್ನು ಬೆಂಜೀನ್ ಮತ್ತು ಮೀಥೇನ್ ಅಣುಗಳ ತುಣುಕುಗಳನ್ನು ಒಳಗೊಂಡಿದೆ ಎಂದು ಪರಿಗಣಿಸಬಹುದು. ಆದ್ದರಿಂದ, ಟೊಲುಯೆನ್ನ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳು ಈ ಎರಡು ಪದಾರ್ಥಗಳ ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಪ್ರತ್ಯೇಕವಾಗಿ ತೆಗೆದುಕೊಂಡ ಸ್ವಲ್ಪ ಮಟ್ಟಿಗೆ ಸಂಯೋಜಿಸಬೇಕು ಎಂದು ಊಹಿಸುವುದು ತಾರ್ಕಿಕವಾಗಿದೆ. ಇದರ ಹ್ಯಾಲೊಜೆನೇಶನ್ ಸಮಯದಲ್ಲಿ ಇದನ್ನು ಹೆಚ್ಚಾಗಿ ಗಮನಿಸಬಹುದು. ಎಲೆಕ್ಟ್ರೋಫಿಲಿಕ್ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಬೆಂಜೀನ್ ಕ್ಲೋರಿನ್ನೊಂದಿಗೆ ಪರ್ಯಾಯ ಪ್ರತಿಕ್ರಿಯೆಗೆ ಒಳಗಾಗುತ್ತದೆ ಎಂದು ನಮಗೆ ಈಗಾಗಲೇ ತಿಳಿದಿದೆ ಮತ್ತು ಈ ಪ್ರತಿಕ್ರಿಯೆಯನ್ನು ಕೈಗೊಳ್ಳಲು ವೇಗವರ್ಧಕಗಳನ್ನು (ಅಲ್ಯೂಮಿನಿಯಂ ಅಥವಾ ಫೆರಿಕ್ ಹ್ಯಾಲೈಡ್ಗಳು) ಬಳಸುವುದು ಅವಶ್ಯಕ. ಅದೇ ಸಮಯದಲ್ಲಿ, ಮೀಥೇನ್ ಕ್ಲೋರಿನ್ನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುವ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೊಂದಿದೆ, ಆದರೆ ಸ್ವತಂತ್ರ ರಾಡಿಕಲ್ ಯಾಂತ್ರಿಕತೆಯ ಮೂಲಕ, ಇದು ಯುವಿ ಬೆಳಕಿನೊಂದಿಗೆ ಆರಂಭಿಕ ಪ್ರತಿಕ್ರಿಯೆ ಮಿಶ್ರಣದ ವಿಕಿರಣದ ಅಗತ್ಯವಿರುತ್ತದೆ. ಟೊಲ್ಯೂನ್, ಕ್ಲೋರಿನೀಕರಣಕ್ಕೆ ಒಳಪಡುವ ಪರಿಸ್ಥಿತಿಗಳನ್ನು ಅವಲಂಬಿಸಿ, ಬೆಂಜೀನ್ ರಿಂಗ್ನಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳ ಪರ್ಯಾಯ ಉತ್ಪನ್ನಗಳನ್ನು ನೀಡಬಹುದು - ಇದಕ್ಕಾಗಿ ನೀವು ಬೆಂಜೀನ್ನ ಕ್ಲೋರಿನೇಶನ್ ಅಥವಾ ಹೈಡ್ರೋಜನ್ ಪರ್ಯಾಯ ಉತ್ಪನ್ನಗಳಂತೆಯೇ ಅದೇ ಷರತ್ತುಗಳನ್ನು ಬಳಸಬೇಕಾಗುತ್ತದೆ. ಮೀಥೈಲ್ ರಾಡಿಕಲ್ನಲ್ಲಿನ ಪರಮಾಣುಗಳು, ನೇರಳಾತೀತ ವಿಕಿರಣದ ಅಡಿಯಲ್ಲಿ ಕ್ಲೋರಿನ್ ಮೀಥೇನ್ ಮೇಲೆ ಹೇಗೆ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ:
ನೀವು ನೋಡುವಂತೆ, ಅಲ್ಯೂಮಿನಿಯಂ ಕ್ಲೋರೈಡ್ನ ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಟೊಲುಯೆನ್ನ ಕ್ಲೋರಿನೀಕರಣವು ಎರಡು ವಿಭಿನ್ನ ಉತ್ಪನ್ನಗಳಿಗೆ ಕಾರಣವಾಯಿತು - ಆರ್ಥೋ- ಮತ್ತು ಪ್ಯಾರಾ-ಕ್ಲೋರೊಟೊಲ್ಯೂನ್. ಮೀಥೈಲ್ ರಾಡಿಕಲ್ ಮೊದಲ ವಿಧದ ಬದಲಿಯಾಗಿರುವುದು ಇದಕ್ಕೆ ಕಾರಣ.
AlCl 3 ಉಪಸ್ಥಿತಿಯಲ್ಲಿ ಟೊಲುಯೆನ್ನ ಕ್ಲೋರಿನೀಕರಣವನ್ನು ಕ್ಲೋರಿನ್ಗಿಂತ ಹೆಚ್ಚಿನ ಪ್ರಮಾಣದಲ್ಲಿ ನಡೆಸಿದರೆ, ಟ್ರೈಕ್ಲೋರೋ-ಬದಲಿ ಟೊಲುಯೆನ್ ರಚನೆಯು ಸಾಧ್ಯ:
ಅದೇ ರೀತಿ, ಹೆಚ್ಚಿನ ಕ್ಲೋರಿನ್/ಟೊಲ್ಯೂನ್ ಅನುಪಾತದಲ್ಲಿ ಬೆಳಕಿನಲ್ಲಿ ಟೊಲುಯಿನ್ ಅನ್ನು ಕ್ಲೋರಿನೇಟ್ ಮಾಡಿದಾಗ, ಡೈಕ್ಲೋರೋಮೆಥೈಲ್ಬೆಂಜೀನ್ ಅಥವಾ ಟ್ರೈಕ್ಲೋರೋಮೆಥೈಲ್ಬೆಂಜೀನ್ ಪಡೆಯಬಹುದು:
ನೈಟ್ರೇಶನ್
ಸಾಂದ್ರೀಕೃತ ನೈಟ್ರಿಕ್ ಮತ್ತು ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲಗಳ ಮಿಶ್ರಣದೊಂದಿಗೆ ಟೊಲುಯೆನ್ನ ನೈಟ್ರೇಶನ್ ಸಮಯದಲ್ಲಿ ಹೈಡ್ರೋಜನ್ ಪರಮಾಣುಗಳನ್ನು ನೈಟ್ರೊ ಗುಂಪಿನೊಂದಿಗೆ ಬದಲಾಯಿಸುವುದು ಮೀಥೈಲ್ ರಾಡಿಕಲ್ ಬದಲಿಗೆ ಆರೊಮ್ಯಾಟಿಕ್ ರಿಂಗ್ನಲ್ಲಿ ಪರ್ಯಾಯ ಉತ್ಪನ್ನಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
ಆಲ್ಕೈಲೇಶನ್
ಈಗಾಗಲೇ ಹೇಳಿದಂತೆ, ಮೀಥೈಲ್ ರಾಡಿಕಲ್ ಮೊದಲ ವಿಧದ ಓರಿಯೆಂಟಿಂಗ್ ಏಜೆಂಟ್, ಆದ್ದರಿಂದ ಫ್ರೈಡೆಲ್-ಕ್ರಾಫ್ಟ್ಸ್ ಪ್ರಕಾರ ಅದರ ಆಲ್ಕೈಲೇಶನ್ ಆರ್ಥೋ- ಮತ್ತು ಪ್ಯಾರಾ-ಸ್ಥಾನಗಳಲ್ಲಿ ಪರ್ಯಾಯ ಉತ್ಪನ್ನಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
ಸೇರ್ಪಡೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು
ಲೋಹದ ವೇಗವರ್ಧಕಗಳನ್ನು (Pt, Pd, Ni) ಬಳಸಿಕೊಂಡು ಟೊಲ್ಯೂನ್ ಅನ್ನು ಮೀಥೈಲ್ಸೈಕ್ಲೋಹೆಕ್ಸೇನ್ಗೆ ಹೈಡ್ರೋಜನೀಕರಿಸಬಹುದು:
C 6 H 5 CH 3 + 9O 2 → 7CO 2 + 4H 2 O
ಅಪೂರ್ಣ ಆಕ್ಸಿಡೀಕರಣ
ಪೊಟ್ಯಾಸಿಯಮ್ ಪರ್ಮಾಂಗನೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದಂತಹ ಆಕ್ಸಿಡೈಸಿಂಗ್ ಏಜೆಂಟ್ಗೆ ಒಡ್ಡಿಕೊಂಡಾಗ, ಅಡ್ಡ ಸರಪಳಿಯು ಆಕ್ಸಿಡೀಕರಣಕ್ಕೆ ಒಳಗಾಗುತ್ತದೆ. ಅಂತಹ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ಆರೊಮ್ಯಾಟಿಕ್ ಕೋರ್ ಆಕ್ಸಿಡೀಕರಣಗೊಳ್ಳುವುದಿಲ್ಲ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ದ್ರಾವಣದ pH ಅನ್ನು ಅವಲಂಬಿಸಿ, ಕಾರ್ಬಾಕ್ಸಿಲಿಕ್ ಆಮ್ಲ ಅಥವಾ ಅದರ ಉಪ್ಪು ರೂಪುಗೊಳ್ಳುತ್ತದೆ.
; ಈ ಸಂದರ್ಭದಲ್ಲಿ, ಒಂದು p-ಬಂಧವು ಮುರಿದುಹೋಗುತ್ತದೆ ಮತ್ತು ಒಂದು ಅಥವಾ ಎರಡು s-ಬಂಧಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ಸೇರುವುದನ್ನು ಸೂಚಿಸಲು ಪ್ರತಿಕ್ರಿಯೆಗಳುಜಾಹೀರಾತು ಚಿಹ್ನೆಯನ್ನು ಬಳಸಿ (ಇಂಗ್ಲಿಷ್ ಸೇರ್ಪಡೆಯಿಂದ - ಪ್ರವೇಶ); ಸೈಕ್ಲೋಡಿಶನ್ಗಳಿಗಾಗಿ, ಅಂತಹ ಚಿಹ್ನೆಯನ್ನು ಬಳಸಲಾಗುವುದಿಲ್ಲ.
ಪ್ರಕೃತಿಯನ್ನು ಅವಲಂಬಿಸಿ ತಲಾಧಾರಸೇರ್ಪಡೆಗಳ ನಡುವೆ ವ್ಯತ್ಯಾಸವನ್ನು ಗುರುತಿಸಿ ಪ್ರತಿಕ್ರಿಯೆಗಳುಪ್ರತ್ಯೇಕವಾಗಿ ಅಥವಾ ಸಂಯೋಜಿತವಾಗಿ ಬಹು ಬಂಧಗಳು, ಉದಾ: C=C, C=C, C=C-C=C, C=O, C=N, C=N ಹೋಮೋಲಿಟಿಕ್ ಪರಿಹಾರಗಳಿವೆ. (Ad R) ಮತ್ತು ಹೆಟೆರೊಲೈಟಿಕ್. ಸೇರ್ಪಡೆ. ಆಕ್ರಮಣಕಾರರ ಆರೋಪವನ್ನು ಅವಲಂಬಿಸಿ ಎರಡನೆಯದು ಕಾರಕಎಲೆಕ್ಟ್ರೋಫ್ ಜಿಲ್ಲೆಗಳಾಗಿ ವಿಂಗಡಿಸಲಾಗಿದೆ. (ಆಡ್ ಇ) ಮತ್ತು ನ್ಯೂಕ್ಲಿಯೋಫ್. (ಜಾಹೀರಾತು) ಲಗತ್ತುಗಳು. ನಡವಳಿಕೆ ಕಾರಕಪ್ರಕಾರವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ ತಲಾಧಾರಮತ್ತು r-tion ಅನ್ನು ಕೈಗೊಳ್ಳಲು ಷರತ್ತುಗಳು (r-ನಿವಾಸಿ, ಉಪಸ್ಥಿತಿ ವೇಗವರ್ಧಕ, UV ವಿಕಿರಣದ ಪರಿಣಾಮ, ಇತ್ಯಾದಿ). ಎಂ.ಎನ್. ಕಾರಕಗಳುವಿಭಿನ್ನ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ ವಿಭಿನ್ನವಾಗಿ ಪ್ರದರ್ಶಿಸಬಹುದು ಪ್ರತಿಕ್ರಿಯೆಯ ವಿಧಗಳು ಸಾಮರ್ಥ್ಯಗಳು, ಉದಾ. ಹ್ಯಾಲೊಜೆನ್ಗಳುಆಮೂಲಾಗ್ರ, ಎಲೆಕ್ಟ್ರೋಫ್ ಆಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸಬಹುದು. ಮತ್ತು ನ್ಯೂಕ್ಲಿಯೋಫ್ ಕೂಡ. ಏಜೆಂಟ್ಗಳು.
ನಾಯಬ್. ಪ್ರವೇಶಗಳನ್ನು ಅಧ್ಯಯನ ಮಾಡಲಾಗಿದೆ ಪ್ರತಿಕ್ರಿಯೆಗಳುಮೂಲಕ ಬಹು ಬಂಧಗಳುಕಾರ್ಬನ್-ಕಾರ್ಬನ್. ಈ ಪ್ರಕ್ರಿಯೆಗಳು ಹಂತಹಂತವಾಗಿ (ಹಂತದ) ಅಥವಾ ಸಿಂಕ್ರೊನಸ್ (ಸಂಯೋಜಿತ) ಕಾರ್ಯವಿಧಾನದ ಪ್ರಕಾರ ಮುಂದುವರಿಯುತ್ತದೆ. ಒಂದು ಹಂತ ಹಂತದ ಕಾರ್ಯವಿಧಾನದೊಂದಿಗೆ, ಮೊದಲ ಹಂತವು ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್, ಎಲೆಕ್ಟ್ರೋಫೈಲ್ ಅಥವಾ ಫ್ರೀ ದಾಳಿಯಾಗಿದೆ. ಆಮೂಲಾಗ್ರ, ಎರಡನೆಯದು - ಮರುಸಂಯೋಜನೆಪರಿಣಾಮವಾಗಿ ಮಧ್ಯಂತರಧನಾತ್ಮಕ, ಋಣಾತ್ಮಕ ಜೊತೆ ಅಥವಾ ತಟಸ್ಥ ಕಣ, ಉದಾಹರಣೆಗೆ:
ಎಲೆಕ್ಟ್ರೋಫ್. ಅಥವಾ ನ್ಯೂಕ್ಲಿಯೋಫ್. ಕಣಗಳು ಇರಬೇಕಾಗಿಲ್ಲ ಅಯಾನುಗಳು; ಅವು ಎಲೆಕ್ಟ್ರಾನ್-ಹಿಂತೆಗೆದುಕೊಳ್ಳುವ ಅಥವಾ ಎಲೆಕ್ಟ್ರಾನ್-ದಾನ ಮಾಡುವ ಭಾಗವಾಗಿರಬಹುದು (ಗುಂಪು) ಅಣುಗಳು. ಎಲೆಕ್ಟ್ರಾನ್-ಹಿಂತೆಗೆದುಕೊಳ್ಳುವ ಬದಲಿಗಳಿಂದ ಸಕ್ರಿಯಗೊಳಿಸಲಾದ C=C ಬಂಧಗಳೊಂದಿಗೆ ಮಾತ್ರ ಜಾಹೀರಾತು N ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸಾಧ್ಯ; ಜಾಹೀರಾತು E ಅನ್ನು ಕಾರ್ಯಗತಗೊಳಿಸಲು, ಬದಲಿಯಾಗದ C=C ಬಂಧಗಳು ಅಥವಾ ಎಲೆಕ್ಟ್ರಾನ್-ದಾನ ಮಾಡುವ ಬದಲಿಗಳಿಂದ ಸಕ್ರಿಯಗೊಳಿಸುವ ಅಗತ್ಯವಿದೆ. Ad R ಪರಿಹಾರಕ್ಕಾಗಿ, C=C ಬಾಂಡ್ನಲ್ಲಿನ ಬದಲಿ ಸ್ವರೂಪವು ಹೆಚ್ಚಿನ ಪ್ರಾಮುಖ್ಯತೆಯನ್ನು ಹೊಂದಿಲ್ಲ.
ಸ್ಟೀರಿಯೋಕೆಮ್. ಹಂತ ಹಂತದ ಸೇರ್ಪಡೆಯ ಫಲಿತಾಂಶವು ಕ್ರಿಯೆಯ ಕಾರ್ಯವಿಧಾನ ಮತ್ತು ಪ್ರತಿಕ್ರಿಯಿಸುವ ಸಂಯುಕ್ತಗಳ ಸ್ವರೂಪವನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ. ಹೌದು, ಎಲೆಕ್ಟ್ರೋಫ್. ಸೇರುವುದು ಓಲೆಫಿನ್ಗಳುಮಗ-ಬಾಂಧವ್ಯವಾಗಿ ಮುಂದುವರಿಯಬಹುದು - ಕಣಗಳು Y ಮತ್ತು W ದಾಳಿ ಅಣುವಿಮಾನದ ಒಂದು ಬದಿಯಲ್ಲಿ ಡಬಲ್ ಬಾಂಡ್ಅಥವಾ ವಿರೋಧಿ ಬಾಂಧವ್ಯವಾಗಿ - ಸಮತಲದ ವಿವಿಧ ಬದಿಗಳಿಂದ ಕಣಗಳು ದಾಳಿ ಮಾಡುತ್ತವೆ; ಕೆಲವು ಸಂದರ್ಭಗಳಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸ್ಟೀರಿಯೊಸ್ಪೆಸಿಫಿಕ್ ಅಲ್ಲ. ನ್ಯೂಕ್ಲಿಯೊಫ್. ಭಾಗವಹಿಸುವಿಕೆಯೊಂದಿಗೆ ಪ್ರವೇಶ ಕಾರ್ಬನಿಯನ್ಗಳುನಿಯಮದಂತೆ, ಸ್ಟೀರಿಯೊಸ್ಪೆಸಿಫಿಕಾಗಿ ಮುಂದುವರಿಯುತ್ತದೆ. ಸೇರಿದ ಮೇಲೆ ಪ್ರತಿಕ್ರಿಯೆಗಳುಮೂಲಕ ಟ್ರಿಪಲ್ ಬಾಂಡ್ಗಳುಸಿನ್ ಸೇರ್ಪಡೆಯು ಸಿಸ್ ಐಸೋಮರ್ಗೆ ಕಾರಣವಾಗುತ್ತದೆ, ವಿರೋಧಿ ಸೇರ್ಪಡೆಯು ಟ್ರಾನ್ಸ್ ಐಸೋಮರ್ಗೆ ಕಾರಣವಾಗುತ್ತದೆ.
ಸಿಂಕ್ರೊನಸ್ ಯಾಂತ್ರಿಕತೆಯ ಸಂದರ್ಭದಲ್ಲಿ, ಎರಡರ ಮೇಲೆ ದಾಳಿ ಪರಮಾಣು C ಅನ್ನು ಏಕಕಾಲದಲ್ಲಿ ನಡೆಸಲಾಗುತ್ತದೆ ಮತ್ತು ಪ್ರತಿಕ್ರಿಯೆಯು ದ್ವಿಧ್ರುವಿ ಸೇರ್ಪಡೆಯಾಗಿ ಮುಂದುವರಿಯುತ್ತದೆ (ಸೈಕ್ಲೋಡಿಶನ್ ನೋಡಿ), ಜೊತೆಗೆ ಪ್ರತಿಕ್ರಿಯೆಗಳುಡಬಲ್ ಅಥವಾ ಟ್ರಿಪಲ್ ಬಾಂಡ್ಮಗ-ಸೇರದಂತೆ ಹೋಗಿ (ನೋಡಿ, ಉದಾಹರಣೆಗೆ, ರೆಪ್ಪೆ ಪ್ರತಿಕ್ರಿಯೆಗಳು).
ಪ ಮರುಸಂಪರ್ಕಗಳು ಪ್ರತಿಕ್ರಿಯೆಗಳುಸಂಯೋಗದಿಂದ ಎರಡು ಬಂಧಗಳು, ಹಂತ ಹಂತದ ಕಾರ್ಯವಿಧಾನದ ಮೂಲಕ ಮುಂದುವರೆಯುವುದು, 1,2- ಮತ್ತು 1,4-ಸೇರ್ಪಡೆ ಉತ್ಪನ್ನಗಳ ರಚನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
ಗೆ ಸಿಂಕ್ರೊನಸ್ 1.4-ಸಂಪರ್ಕ ಡೈನ್ಸ್ಜಾಡು ಸೋರುತ್ತಿದೆ. ದಾರಿ:

ವಿಶೇಷ ರೀತಿಯ ಸಂಕಲನ ಕ್ರಿಯೆಯು ಸಂಯೋಜಿತ ಸೇರ್ಪಡೆಯಾಗಿದೆ. ಅಂತಹ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಹರಿವು ಪರಿಹಾರದ ಬಂಧಿಸುವಿಕೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ (ಅಥವಾ ವಿಶೇಷವಾಗಿ ಸೇರಿಸಲಾಗುತ್ತದೆ ಕಾರಕ) ಪ್ರಕ್ರಿಯೆಯ ಅಂತಿಮ ಹಂತದಲ್ಲಿ. ಉದಾಹರಣೆಗೆ, ಸಂಯೋಜಿತ ಎಲೆಕ್ಟ್ರೋಫ್. ಸೇರ್ಪಡೆ ಹ್ಯಾಲೊಜೆನ್ಗಳುಗೆ ಆಲ್ಕೀನ್ಗಳು CH 3 COOH ನಲ್ಲಿ 1,2-ಡೈಹಲೋಜೆನೈಡ್ಗಳ ಜೊತೆಗೆ b-ಅಸೆಟಾಕ್ಸಿಯಾಕೈಲ್ ಹ್ಯಾಲೈಡ್ಗಳಿಗೆ ಕಾರಣವಾಗುತ್ತದೆ:
ಸಂಯೋಜಿತ ನ್ಯೂಕ್ಲಿಯೊಫ್ ಉದಾಹರಣೆಗಳು. ಪ್ರವೇಶಗಳು - ಮೈಕೆಲ್ ಅವರ ಪ್ರತಿಕ್ರಿಯೆಮತ್ತು ಪರಸ್ಪರ ಕ್ರಿಯೆ ಸಕ್ರಿಯಗೊಳಿಸಲಾಗಿದೆ ಆಲ್ಕೀನ್ಗಳುಪ್ರೋಟಾನ್ ದ್ರಾವಣಗಳಲ್ಲಿ ಸೈನೈಡ್ ಅಯಾನ್ ಜೊತೆಗೆ SH:

ಸೇರುವ ಸಂದರ್ಭದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯೆಗಳುಮೂಲಕ ಬಹು ಬಂಧಗಳುಕಾರ್ಬನ್-ಹೆಟೆರೊ-ಪರಮಾಣು, ಅದರಲ್ಲಿ ಅದನ್ನು ಹಾಕಲಾಗುತ್ತದೆ. ಶುಲ್ಕವನ್ನು ಸ್ಥಳೀಯಗೊಳಿಸಲಾಗಿದೆ ಪರಮಾಣು C (C=O, C=N, C=N ಮತ್ತು C=S ಬಾಂಡ್ಗಳು), ನ್ಯೂಕ್ಲಿಯೊಫೈಲ್ಗಳು ಯಾವಾಗಲೂ ಲಗತ್ತಿಸುತ್ತವೆ ಪರಮಾಣುಸಿ, ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಫೈಲ್ಗಳು ಹೆಟೆರೊಟಾಮ್ಗೆ. ಗರಿಷ್ಠ. ನ್ಯೂಕ್ಲಿಯೊಫಿಲಿಕ್ ಸೇರ್ಪಡೆಗಳನ್ನು ಮಟ್ಟಿಗೆ ಅಧ್ಯಯನ ಮಾಡಲಾಗಿದೆ ಪ್ರತಿಕ್ರಿಯೆಗಳುಕಾರ್ಬೊನಿಲ್ ಗುಂಪಿನ ಮೇಲೆ:

ಪ ಮರುಸಂಪರ್ಕಗಳು ಪ್ರತಿಕ್ರಿಯೆಮೂಲಕ ಪರಮಾಣುಸಿ ಸುಗಂಧದಲ್ಲಿ ಪರ್ಯಾಯದ ಹಂತಗಳಲ್ಲಿ ಒಂದಾಗಿರಬಹುದು. ಸಾಲು, ಉದಾಹರಣೆಗೆ: